Clear Sky Science · ar
التقدّم البحثي في التداخل بين الخلايا الليفية المصاحبة للسرطان وخلايا الورم باستخدام العضويات المشتركة الزرع
لماذا يهم حيّ الورم
السرطان أكثر من مجرد كتلة من الخلايا المارقة؛ إنه ينمو داخل حيّ مزدحم من الخلايا الداعمة، والهياكل المساندة، والأوعية الدموية، ومدافعي المناعة. من بين هؤلاء الجيران، توجد مجموعة تُسمى الخلايا الليفية المصاحبة للسرطان (CAFs) التي تشكّل بهدوء الطريقة التي تنشأ بها الأورام وتنتشر وتستجيب للعلاج. توضح هذه المقالة الاستعراضية كيف يستخدم العلماء أورغانويدات ثلاثية الأبعاد صغيرة تُزرع مع الخلايا الليفية المصاحبة للسرطان لكشف هذا الحوار الخفي وتصميم علاجات أكثر ذكاءً ودقّة.
أورام صغيرة في طبق
اعتمدت أبحاث السرطان التقليدية غالبًا على طبقات مسطحة من الخلايا في أطباق بلاستيكية أو على نماذج حيوانية، وكلاهما يلتقط جزءًا فقط من واقع المرض. تغير العضويات هذا المشهد. فهي كتلات ثلاثية الأبعاد من خلايا الورم المستمدة من المريض تحافظ على قدر كبير من بنية الورم الأصلية وتركيبه الجيني وسلوكه. عندما تُزرع هذه العضويات مع الخلايا الليفية المصاحبة للسرطان، تبدأ بمحاكاة الأورام الصلبة الفعلية، بما في ذلك استجابتها للعلاج الكيميائي والإشعاعي. طوِّرت إعدادات زرع مختلفة: أنظمة بسيطة قائمة على الهلام حيث تشارك خلايا الورم والخلايا الليفية نفس المصفوفة، وطرق "التدلي المختلطة" التي تشكل أولًا كُريات مُدمجَة، ورقائق ميكروفلويديك متقدمة تتحكم في تدفق السوائل وحجم العضوية لاختبارات أدوية عالية الإنتاجية. كل نهج يوازن بين الواقعية والتكلفة والصعوبة التقنية.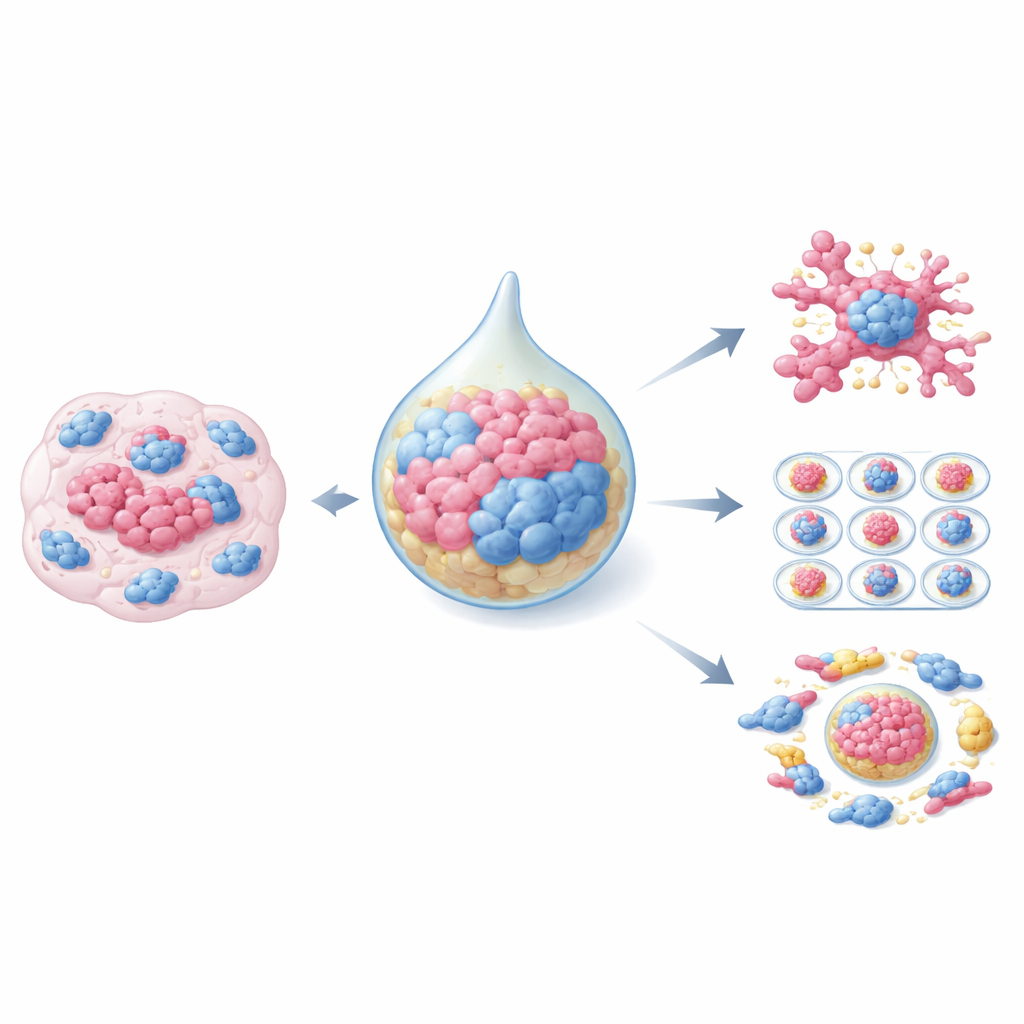
كيف تساعد الخلايا المساندة الأورام على الازدهار
الخلايا الليفية المصاحبة للسرطان ليست نوعًا واحدًا موحّدًا؛ بل تأتي بتنوّعات متعددة، لكل منها دورها الخاص. في العضويات المشتركة الزرع، تساعد CAFs في بناء وإعادة تشكيل الإطار الليفي حول خلايا السرطان، مغيرة الصلابة والبنية بطرق تُفضّل نمو الورم وغزوه. تفرز مزيجًا من الإشارات التي تحث الخلايا السرطانية على التكاثر والحركة والغزو الأنسجة المجاورة، ويمكنها حتى أن تحث خلايا عادية على اكتساب صفات شبيهة بالخلايا الجذعية التي تزرع أورامًا جديدة. تعيد CAFs أيضًا تشكيل كيفية إنتاج الخلايا السرطانية للطاقة واستخدامها، فتبادل المغذيات يحافظ على بقاء الشريكين تحت الضغوط. في العديد من النماذج، تجعل CAFs الأورام أكثر مقاومة للعلاج الكيميائي والأدوية المستهدفة، على سبيل المثال عن طريق درع الخلايا السرطانية داخل كولاجين كثيف، أو تشغيل مسارات بقاء، أو إرسال حويصلات صغيرة محمَّلة بجزيئات RNA تعزز إصلاح الحمض النووي.
الهروب المناعي وتزويد الدم
بعيدًا عن تغذية وإيواء الخلايا السرطانية، تؤثر CAFs بقوة على دفاعات الجسم. تبيّن العضويات المشتركة الزرع وأنظمة العضويات على رقاقة أن CAFs يمكن أن تصد الخلايا المناعية القاتلة، وتجذب شركاء مناعيين مثبطين، وتقود الخلايا المناعية إلى حالة لم تعد فيها قادرة على الهجوم. بعض مجموعات CAF تُثقل الخلايا القاتلة الطبيعية بالحديد وتدفعها نحو شكل من أشكال موت الخلايا، بينما تستدعي مجموعات أخرى البلعميات التي تدعم الورم. في الوقت نفسه، تشجع CAFs نمو أوعية دموية جديدة عن طريق إفراز عوامل تحث خلايا تكوّن الأوعية على النُّمو وبناء قنوات، مما يضمن تدفقًا ثابتًا من الأكسجين والمغذيات إلى الأورام. ومع ذلك، القصة ليست أحادية الجانب تمامًا: فأنواع نادرة من CAFs قد تدعم بالفعل المناعة المضادة للورم عبر المساعدة في تنشيط الخلايا التائية أو إعادة برمجة خلايا مناعية أخرى إلى حالة أكثر فاعلية.
حوار ذو اتجاهين مع خلايا الورم
العلاقة بين CAFs والخلايا السرطانية هي حلقة تغذية راجعة. ترسل الخلايا الورمية إشارات تحول الألياف الليفية الطبيعية القريبة إلى CAFs ثم تُشكلها إلى مجموعات فرعية مختلفة، مثل الخلايا القابضة المنتجة للمصفوفة أو الخلايا المدفوعة بالالتهاب التي تفرز العديد من السيتوكينات. عبر عوامل قابلة للذوبان وحويصلات صغيرة، يمكن للخلايا السرطانية دفع CAFs نحو حالات تُصلّب الأنسجة، وتُعزّز الغزو، وتدفع مقاومة الدواء. كشفت العضويات المشتركة الزرع كيف تعمل مسارات إشارات محددة كمقابض تُحوّل هوية CAFs، مما يسمح للأورام بالتكيف مع الظروف أو العلاجات المتغيرة. فهم هذا التبادل أمر حاسم لأن الأساليب الصارمة التي تهدف لمجرد القضاء على كل CAFs أدت، في بعض الدراسات الحيوانية والتجارب السريرية، إلى تسارع نمو الورم بشكل غير متوقع.
طرق جديدة لاستهداف حيّ الورم
مسلحَين بنماذج العضويات التي تحافظ على تداخل CAF–الورم، يستكشف الباحثون استراتيجيات علاجية أكثر دقة. بدلًا من القضاء على جميع الألياف، تهدف بعض النهج إلى حجب الإشارات الضارة بين CAFs والخلايا السرطانية، أو تعطيل التمثيل الغذائي المشترك، أو "إعادة تعليم" CAFs بلطف إلى حالات أكثر حميدة أو حتى مقيدة للورم. تشمل التكتيكات التجريبية جزيئات صغيرة تغير مسارات الإشارة في CAFs، وأدوية تليّن أو تُخفّف الغلاف الليفي للورم، وعلاجات خلوية متطورة مثل خلايا مناعية مُهندَسة للتعرف على مجموعات فرعية محددة من CAFs ومهاجمتها. تجعل منصات العضويات من الممكن اختبار هذه الأفكار على أنسجة مستمدة من المرضى في المختبر، مقدِّمة طريقًا نحو مجموعات علاجية مخصصة تستهدف كل من الخلايا السرطانية وجوارها الداعم.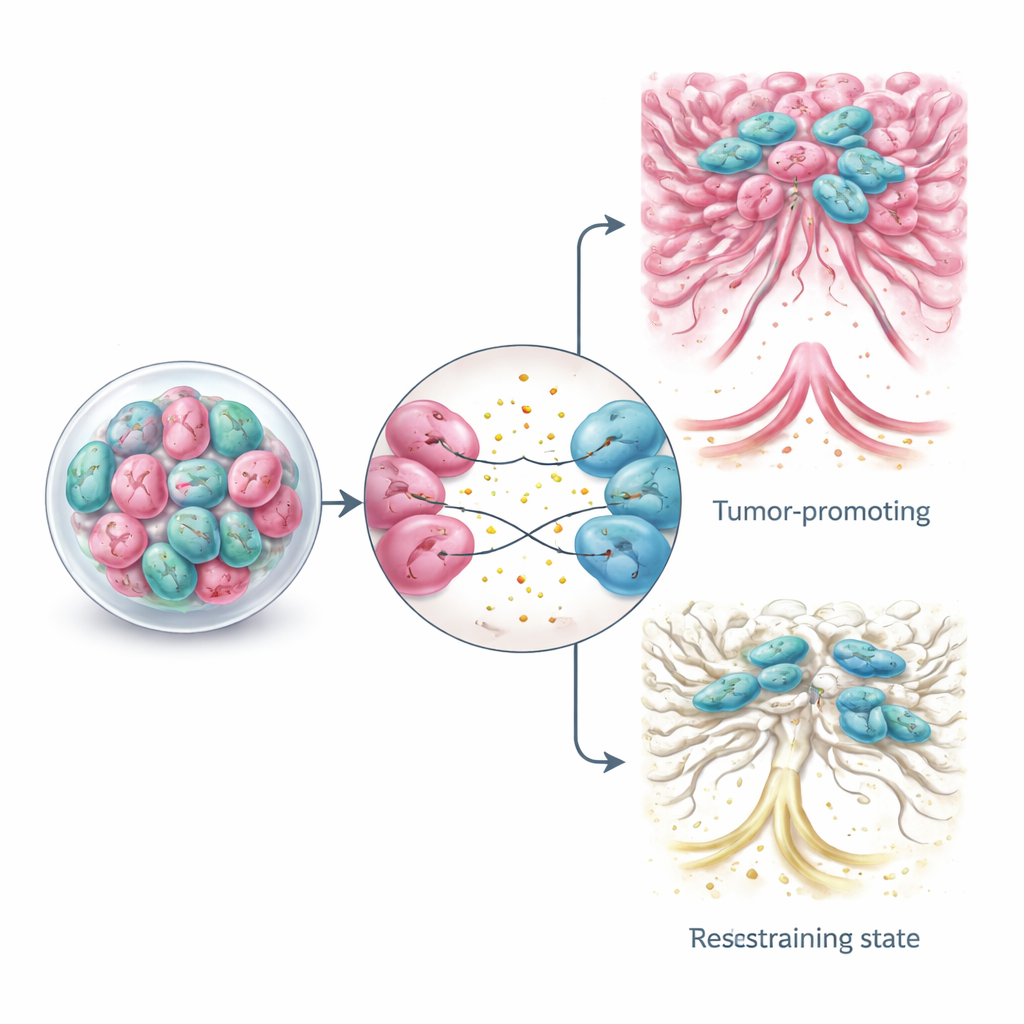
ماذا يعني هذا لرعاية السرطان في المستقبل
تخلص هذه المراجعة إلى أن CAFs هي مساعدات قوية وفي أحيانٍ خصوم هادئون للسرطان. تشرح تنوّعها ومرونتها لماذا فشلت علاجات "قَتل CAF" البسيطة في كثير من الأحيان وأحيانًا سببت ضررًا. باستخدام العضويات المشتركة الزرع كأرضيات اختبار واقعية، يمكن للعلماء الآن تمييز السلوكيات الضارة من المفيدة لدى CAFs، ورسم خرائط الإشارات التي تربطها بالخلايا السرطانية، وتصميم علاجات تحجب بانتقائية الأدوار المحفزة للورم مع الحفاظ على الأدوار الوقائية أو تعزيزها. بالنسبة للمرضى، تمهّد هذه الأعمال الطريق لاختبارات دوائية أكثر دقّة وتركيبات علاجية لا تهاجم الورم فحسب، بل تعيد تشكيل الحي الذي يسمح له بالازدهار.
الاستشهاد: Wang, M., Ding, X., Chen, L. et al. The research advances of crosstalk between cancer-associated fibroblasts and tumor cells using co-culture organoids. Cell Death Dis 17, 267 (2026). https://doi.org/10.1038/s41419-026-08512-8
الكلمات المفتاحية: الخلايا الليفية المصاحبة للسرطان, عضويات الورم, البيئة الدقيقة للورم, مقاومة العلاج, نماذج التعاون ثلاثية الأبعاد