Clear Sky Science · ar
يبنيمكس يتآزر مع حجب PD-L1 في سرطان المعدة عن طريق الارتباط التنافسي بـ LAP3 مع UBE3A
لماذا يهم هذا البحث
لدى العديد من المصابين بسرطان المعدة المتقدم، جلبت أدوية العلاج المناعي الحديثة التي «تخفف الكوابح» عن جهاز المناعة أملاً جديداً—لكنها لا تفيد سوى أقلية من المرضى. يطرح هذا البحث سؤالاً عملياً ذو أثر في العالم الحقيقي: هل يمكن إعادة توظيف دواء محسن للمناعة قديم، يبنيمكس، لجعل هذه الأدوية تعمل بشكل أفضل، ولماذا سيساعد ذلك؟ يكشف الباحثون عن حيلة جزيئية مخفية تستخدمها الأورام للهروب من الهجوم المناعي ويبينون كيف يمكن ليبنيمكس أن يلغيها، فاتحاً الباب أمام علاجات مركبة أكثر فعالية.
شريك جديد للعلاج المناعي من السرطان
يركز العمل على سرطان المعدة، وهو مرض لا يزال شائعاً ومميتاً، خاصة في الصين. تُعد الأدوية التي تحجب PD-1 أو PD-L1—البروتينات التي تخفف الاستجابات المناعية—حالياً دعامة في العلاج. ومع ذلك، فإن معظم المرضى إما لا يستجيبون أبداً أو ينتكسون في نهاية المطاف. لجأ المؤلفون إلى يبنيمكس، دواء معتمد منذ زمن يُستخدم كمكمل للعلاج الكيميائي والإشعاعي، ومعروف بقدرته على تحفيز خلايا المناعة. تساءلوا عما إذا كان اقتران يبنيمكس بالأجسام المضادة المحجوبة لـ PD-L1 يمكن أن يجعل الأورام أكثر عرضة لهجوم خلايا T القاتلة، وهي خلايا مناعية تدمر الخلايا السرطانية مباشرة.
اختبار تركيبة الدواء
باستخدام نموذج فأري لسرطان المعدة حيث تم تعديل الأورام لإنتاج مفرط لبروتين يسمى LAP3، عالج الفريق الحيوانات بيبنيمكس أو بمضاد PD-L1 أو بكليهما أو لم يعالجوا. كل علاج على حدة قلّص الأورام، لكن التركيبة تميزت: تراجعت الأورام تماماً في جميع الفئران المعالجة، وتحسنت البقاء على قيد الحياة أكثر مما هو عليه مع حجب PD-L1 وحده. أظهرت تحليلات الجهاز المناعي أن التركيبة عززت بشكل كبير عدد ونشاط خلايا CD8 «القاتلة»، التي أفرجت عن المزيد من الجزيئات السامة والرسل الالتهابية. والأهم من ذلك، أن العلاج لم يسبب أضراراً كبدية واضحة أو فقداناً في الوزن، مما يوحي بأن النهج قد يكون قوياً دون أن يكون قاسياً بشكل مفرط.
مفتاح مخفي يقي الأورام
لفهم سبب فائدة يبنيمكس، ركز الباحثون على LAP3، وهو إنزيم يثبطه الدواء. وجدوا أن مستويات LAP3 كانت أعلى في أورام المعدة البشرية مقارنةً بنسيج المعدة الطبيعي، وأن المرضى ذوي المستويات الأعلى من LAP3 كانوا يميلون إلى بقاء أسوأ. في كل من عينات المرضى وأورام الفئران، ارتبط ارتفاع LAP3 بعدم وجود خلايا CD8 داخل السرطان، رغم أن أنواع الخلايا المناعية الأخرى لم تتغير. عندما خُفض LAP3 تجريبياً في خلايا الورم، نمت الأورام أبطأ، وجذبت المزيد من خلايا CD8، وأصبحت أسهل لقتلها في اختبارات المختبر. تشير البيانات مجتمعة إلى أن LAP3 ليس مجرد متفرج بل منشط فعّال للهروب المناعي.
كيف تستخدم الأورام LAP3 للحفاظ على الكوابح
بالتعمق أكثر، كشف الفريق كيف يحمي LAP3 خلايا الورم من الهجوم المناعي. اكتشفوا أن LAP3 يساعد في استقرار PD-L1، وهو بروتين «الكبح» الرئيسي على خلايا السرطان الذي يثبط خلايا T. عادةً، يمكن تعليم PD-L1 بعلامات بروتينية صغيرة ترسله إلى آلية التخلص داخل الخلية. إنزيم يُدعى UBE3A يعلق هذه العلامات، مما يؤدي إلى تكسير PD-L1. يرتبط LAP3 فيزيائياً بـ UBE3A وبذلك يمنع UBE3A من وضع العلامات على PD-L1. نتيجة لذلك، يتراكم PD-L1 على سطح الورم، مكوناً درعاً يقي من خلايا CD8. عندما تُخفض مستويات LAP3 أو تُمنع فعاليته، تُعلّق أنظمة الوسم PD-L1 بشكل أكبر، ويتكسّر أسرع، وتنخفض مستوياته السطحية—مما يسمح لخلايا T بالاقتراب والهجوم.
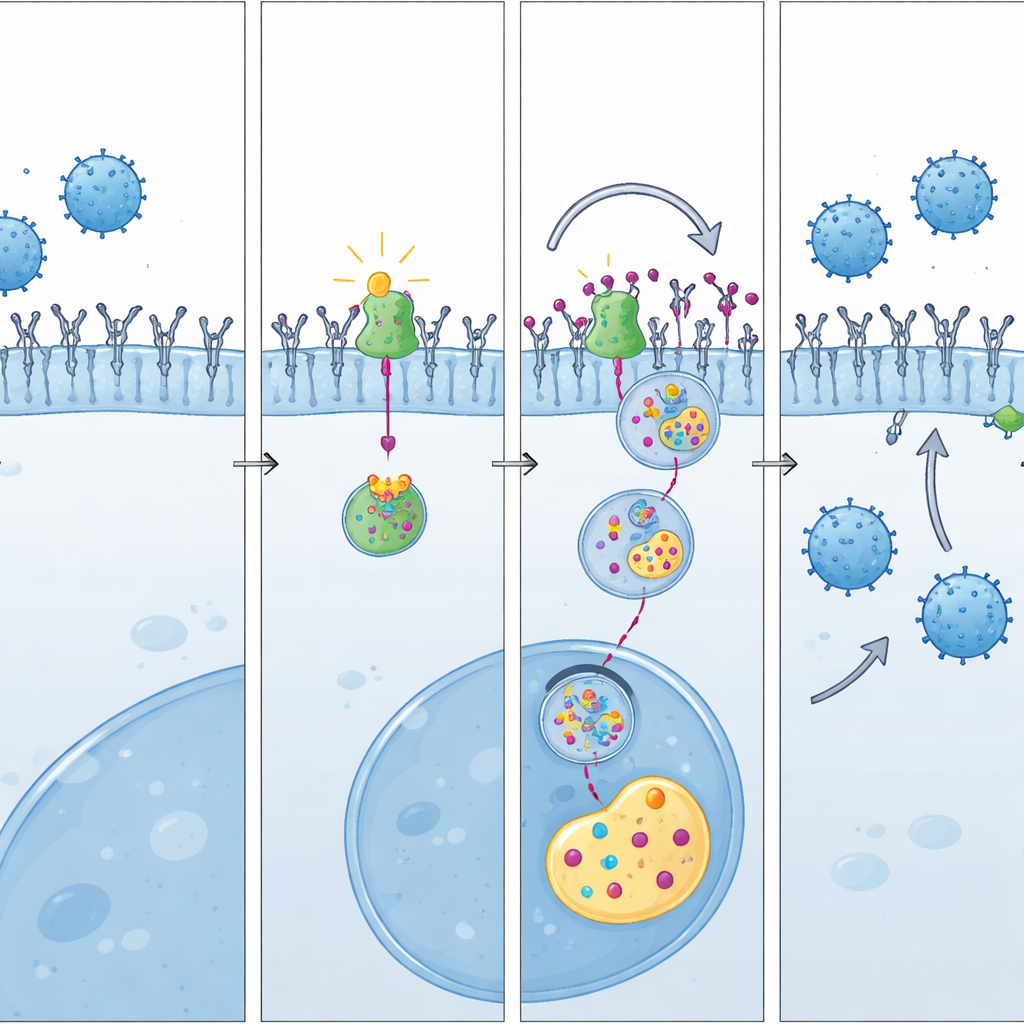
كيف يعبّر يبنيمكس الميزان
ثم يظهر البحث أن يبنيمكس يعمل عن طريق التدخل في شراكة LAP3–UBE3A. تشير نمذجة الحاسوب والتجارب الكيميائية الحيوية إلى أن يبنيمكس يحجز في LAP3 في نفس المنطقة التي يتفاعل فيها LAP3 عادةً مع UBE3A. هذا الارتباط التنافسي يفصل UBE3A عن LAP3، مطلقاً إياه لوضع علامات على PD-L1 لتدميره. في تجارب خلوية، خفض يبنيمكس PD-L1 على سطح الورم، وزاد من وسم PD-L1 للتخلص منه، وعكس تأثيرات رفع LAP3 على زيادة PD-L1. في الفئران الحية، تُرجمت تلك التحولات الجزيئية إلى المزيد من خلايا CD8 النشطة وسيطرة ملحوظة على الأورام عند دمج يبنيمكس مع حجب PD-L1.
ماذا يعني هذا للمرضى
بالمجمل، يرسم البحث صورة واضحة: العديد من أورام المعدة تنتج LAP3 بكميات مفرطة، مما يساعدها على الحفاظ على مستويات عالية من PD-L1 وبالتالي الاختفاء من جهاز المناعة. يكسر يبنيمكس هذا الحماية عن طريق منع قبضة LAP3 على UBE3A، مما يسمح بإزالة PD-L1. مع قلة الكوابح على سطح خلايا السرطان، يمكن لأدوية حجب PD-L1 وخلايا T القاتلة أن تعمل معاً بفاعلية أكبر بكثير. وبما أن يبنيمكس موجود بالفعل في الاستخدام السريري ويمكن قياس LAP3 في عينات الأورام، يوفر هذا البحث استراتيجية ملموسة وقابلة للاختبار لتحسين العلاج المناعي في سرطان المعدة وربما في سرطانات أخرى ذات مستويات مرتفعة من LAP3.
الاستشهاد: Zhao, C., Li, J., Zheng, J. et al. Ubenimex synergizes with the PD-L1 blockade in gastric cancer by competitively binding LAP3 with UBE3A. Cell Death Dis 17, 241 (2026). https://doi.org/10.1038/s41419-026-08509-3
الكلمات المفتاحية: سرطان المعدة, العلاج المناعي, PD-L1, يبنيمكس, LAP3