Clear Sky Science · ar
يساهم CCL11 في عودة سرطان الكبد بعد الجراحة عن طريق تعزيز خلايا بلعميّة شبيهة بالطور M2 حاملة CCR5 وCD206 المثبطة للمناعة وتعزيز عدوانية الورم
لماذا يمكن أن يعود سرطان الكبد بعد الجراحة
تعد جراحة الكبد غالبًا أفضل أمل لمرضى السرطان في مراحله المبكرة، ومع ذلك يعود السرطان لدى كثير من المرضى خلال سنوات قليلة. تطرح هذه الدراسة سؤالاً بسيطًا لكنه حاسم: هل يستفيد الجسم عن غير قصد من استجابة الالتهاب للجراحة بحيث يساعد خلايا السرطان المتبقية على النمو والانتشار؟ ركز الباحثون على جزيء إشارة يُدعى CCL11 وأظهروا كيف أن ارتفاعًا مفاجئًا لهذا الجزيء بعد الجراحة يمكن أن يضعف المناعة المضادة للسرطان ويجعل الخلايا الورمية الناجية أكثر عدوانية.
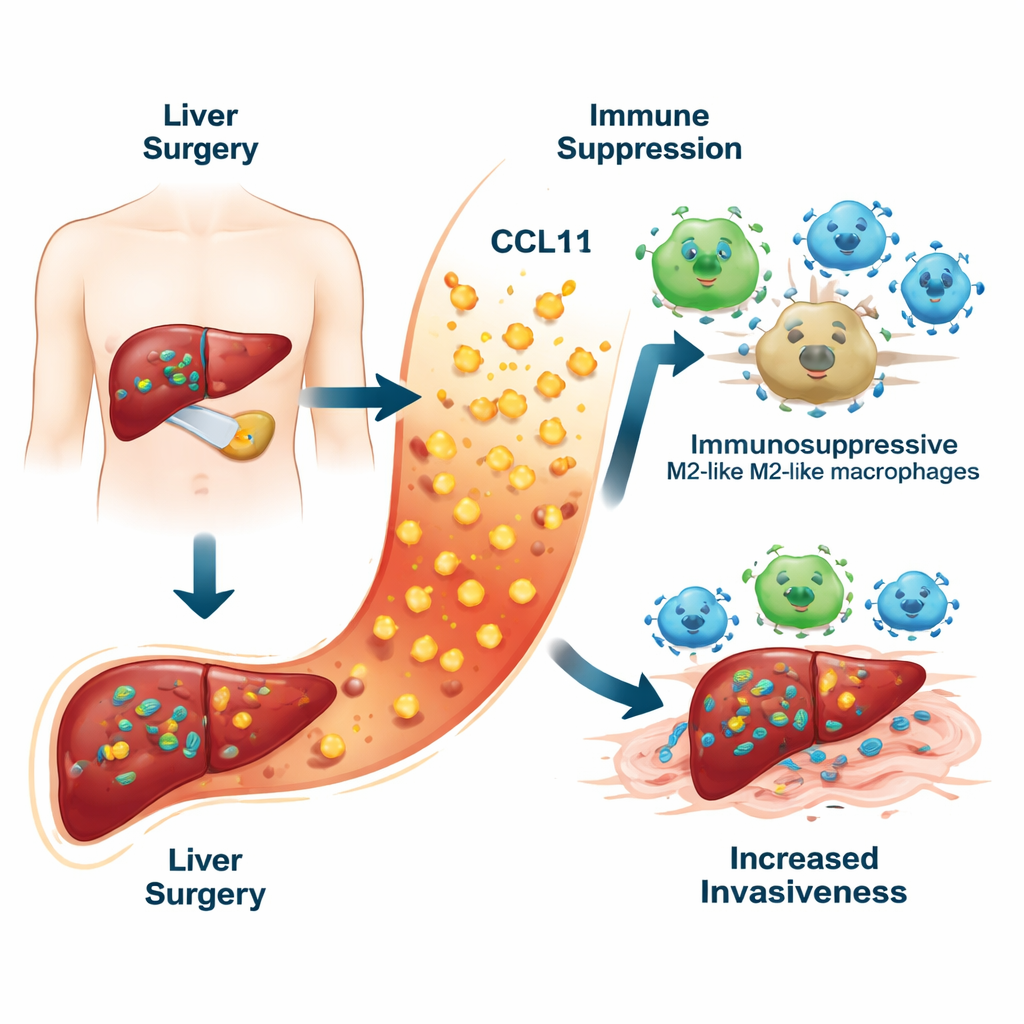
خطر خفي في استجابة الشفاء
عندما يستأصل الجراحون ورمًا كبديًا، يضطرون إلى ربط الأوعية الدموية وإلحاق ضرر بالأنسجة المحيطة. يطلق هذا الضرر موجة من الالتهاب التي تُساعد الكبد على الشفاء. عبر قياس عشرة جزيئات التهابية مختلفة في دم المرضى بعد أسبوع من الجراحة، وجد الفريق أن كيموكينًا واحدًا، CCL11، كان بارزًا. المرضى الذين عاد إليهم سرطان الكبد لاحقًا كانت لديهم مستويات أعلى بكثير من CCL11 مقارنة بمن بقوا خالين من السرطان. كما ارتبطت مستويات CCL11 العالية ببقاء أسوأ. عندما جمع الباحثون CCL11 مع بيانات سريرية روتينية مثل اختبارات الدم وميزات الورم، بنوا «بطاقة مخاطر» توقعت عودة المرض خلال خمس سنوات بدقة أكبر من النماذج التقليدية.
حتى نسيج الكبد الذي يبدو طبيعيًا مهم
تركز معظم الأبحاث على الورم نفسه، لكن هذه الدراسة تُظهر أن نسيج الكبد «الطبيعي» المحيط قد يكون مهمًا بنفس القدر. في عينات من أكثر من 100 مريض، كان CCL11 في الواقع أعلى في الكبد غير الورمي منه في عقيدات السرطان أو في كُبُد المتبرعين الأصحاء. المرضى الذين أنتج نسيج كبدهم القريب المزيد من CCL11 كانوا أكثر عرضة لمرض متقدم، وانتشار بعيد، وانتكاس بعد الجراحة. في نماذج فأرية تحاكي فقدانًا مؤقتًا للدم ثم عودته أثناء العملية، ارتفعت مستويات CCL11 بسرعة نتيجة إصابة الكبد. وتحت ظروف نقص الأكسجة في المختبر، أنتجت خلايا داعمة للكبد مثل الميوفايبروبلاست وخلايا بطانة الأوعية الدموية المزيد من CCL11 أيضًا، ممّا يشير إلى أن ضغط الجراحة يجعل بقايا الكبد بيئة مؤيدة للسرطان.
كيف يحول CCL11 المدافعين المناعيين إلى مشاهير جانبيين
لرصد تأثير CCL11 على المناعة، ركز المؤلفون على البلعمات الكبيرة (الماكروفاجات)، وهي خلايا بيضاء متعددة المهام يمكن أن تهاجم الأورام أو تحميها. وجدوا أن في نسيج الكبد غير الورمي، ارتبط ارتفاع CCL11 بوجود نمط فرعي من البلعمات يحمل العلامة CCR5 ويعرض ملفًا شبيهًا بالطور M2 الصديق للورم. في المرضى، ارتبطت الكبدات الغنية بهذه البلعمات CCR5+ الشبيهة بـM2 ببقاء أسوأ. في مزراع الخلايا، دفع إضافة CCL11 الوحيدات (المونوسايت) لتتحول إلى هذا النوع المثبط للمناعة من البلعمات، مرفقة بزيادة في جزيئات مثل PD‑L1 وIL‑10 وإطلاق إشارات أخرى تجذب وتحوّر المزيد من الخلايا المناعية. هذه البلعمات الممتحنة بـCCL11 شجعت بعد ذلك الخلايا التائية المساعدة البدائية على التحول إلى خلايا تائية تنظيمية، وهي فئة معروفة بتقليل الاستجابات المضادة للورم. أظهرت تجارب آلية أن CCL11 يُفعّل سلسلة إشارات داخل البلعمات تنتهي بمسار NF‑κB وإنتاج PD‑L1، ما يساعد على حماية الخلايا السرطانية من الهجوم المناعي.
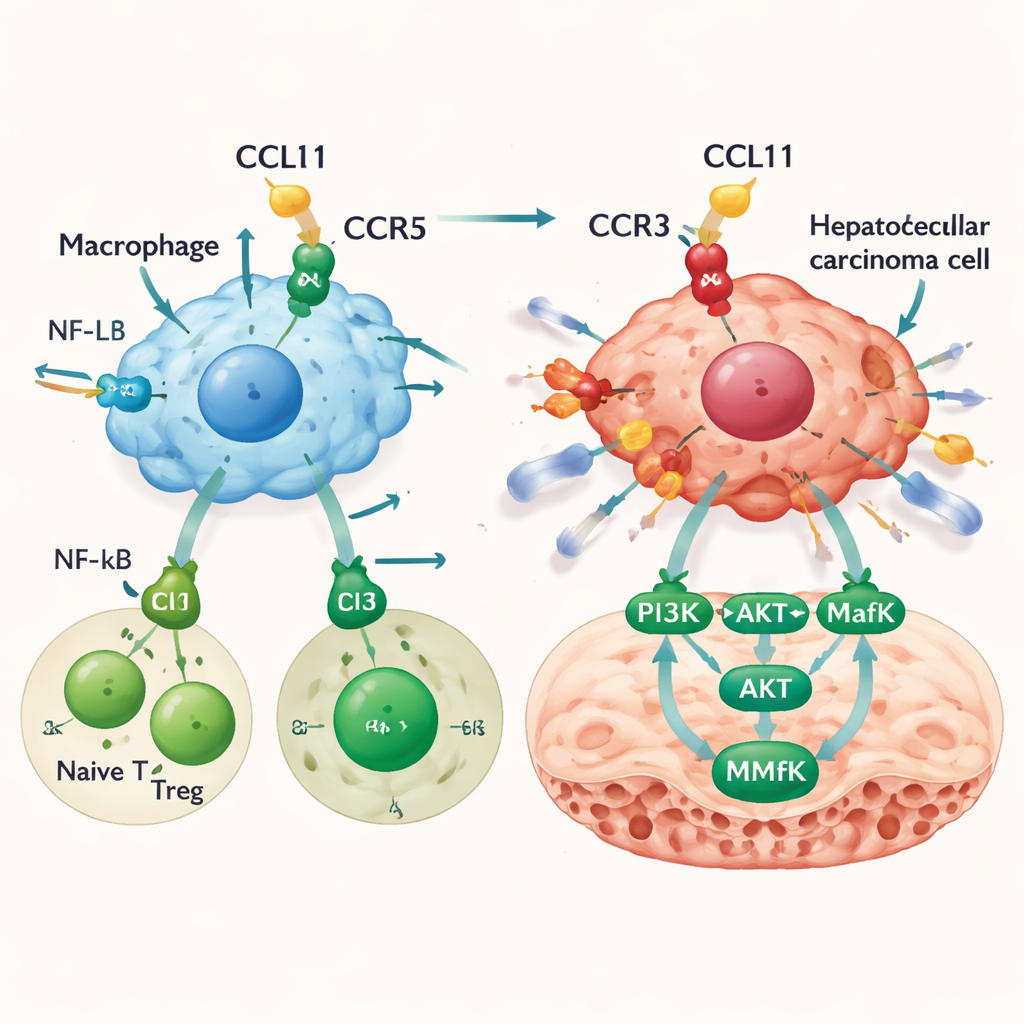
كيف يجعل CCL11 خلايا السرطان المتبقية أكثر غزوًا
لا يعيد CCL11 تشكيل المشهد المناعي فحسب؛ بل يؤثر مباشرة على خلايا سرطان الكبد. رغم أن الخلايا السرطانية نفسها تنتج القليل من CCL11، إلا أنها تحمل أحد مستقبلاته، CCR3. في تجارب معملية، لم يسرّع CCL11 نمو خلايا سرطان الكبد لكنه زاد من هجرتها وغزوها عبر الحواجز، وهي سمة تميّز القدرة على الانتقال النقائل. أدى حجب مستقبل CCR3 إلى محو هذا التأثير إلى حد كبير. أشارت تحليلات الجينات إلى مسار حيث يشغّل إشارة CCL11–CCR3 إنزلات PI3K وAKT، التي تفعل بدورها عامل نسخ يُدعى MafK. يقوم MafK بعد ذلك برفع إنتاج MMP13، إنزيم يكسر النسيج المحيط ويفتح مسارات لانتشار السرطان. في نماذج فأرية، أدت حقن CCL11 في الكبد إلى زيادة عبء الورم ومزيد من النقائل، إلى جانب مستويات أعلى من مسار PI3K–AKT–MafK–MMP13 داخل الأورام.
تحويل إشارة محفوفة بالمخاطر إلى فرصة علاجية
لأن CCL11 يبدو أنه يسكّت الدفاعات المناعية ويقوي الخلايا الورمية المتبقية في آن واحد، اختبر الباحثون ما إذا كان حظره بعد الجراحة قد يغيّر النتائج. في فئران تحمل أورامًا كبدية أُزيِلت جراحيًا، أدى العلاج بأجسام مضادة محايدة لـCCL11 إلى تقليل كبير في معدل عودة السرطان في الكبد وتحسّن البقاء، من دون آثار جانبية واضحة مثل فقدان الوزن. تجتمع النتائج لتبرز CCL11 كمفتاح رئيسي يربط إصابة الجراحة ببيئة كبدية مثبطة للمناعة ومهيّئة للغزو. ولأجل المرضى، تشير هذه الدراسة إلى أن قياس CCL11 بعد الجراحة قد يساعد على تحديد من هم أكثر عرضة للانتكاس، وأن العقاقير التي تستهدف محور CCL11–CCR5/CCR3 قد تصبح يومًا جزءًا من استراتيجيات منع عودة سرطان الكبد.
الاستشهاد: Wang, J., Yeung, O.WH., Qiu, W. et al. CCL11 promotes hepatocellular carcinoma recurrence after surgery by potentiating immunosuppressive CCR5 + CD206 + M2-like macrophages and promoting tumor invasiveness. Cell Death Dis 17, 236 (2026). https://doi.org/10.1038/s41419-026-08508-4
الكلمات المفتاحية: عودة سرطان الكبد, كيموكين CCL11, البيئة الدقيقة للورم, قمع المناعة, انتشار السرطان