Clear Sky Science · ar
الخلايا الليفية المرتبطة بالسرطان تعزز مقاومة الأوزيمرتينيب في خلايا سرطان الرئة غير صغيرة الخلايا عبر تعديل NET1 m7G بوساطة METTL1
لماذا تتوقف بعض سرطانات الرئة عن الاستجابة لعقار «ذكي»
لقد غيرت الأدوية المستهدفة مثل الأوزيمرتينيب ملامح علاج كثير من المرضى المصابين بنوع شائع من سرطان الرئة، فوفرت حياة أطول مع آثار جانبية أقل مقارنة بالعلاج الكيماوي التقليدي. ومع ذلك، فإن هذه الفوائد مؤقتة لمعظم المرضى: فالأورام في نهاية المطاف تجد طرقًا للتغلب على الدواء. تطرح هذه الدراسة سؤالًا بسيطًا في ظاهره ولكن له تبعات كبيرة: هل النسيج الداعم للورم — وتحديدًا خلايا تُسمى الخلايا الليفية المرتبطة بالسرطان — يساعد بصمت خلايا السرطان على الهروب من تأثير الأوزيمرتينيب؟
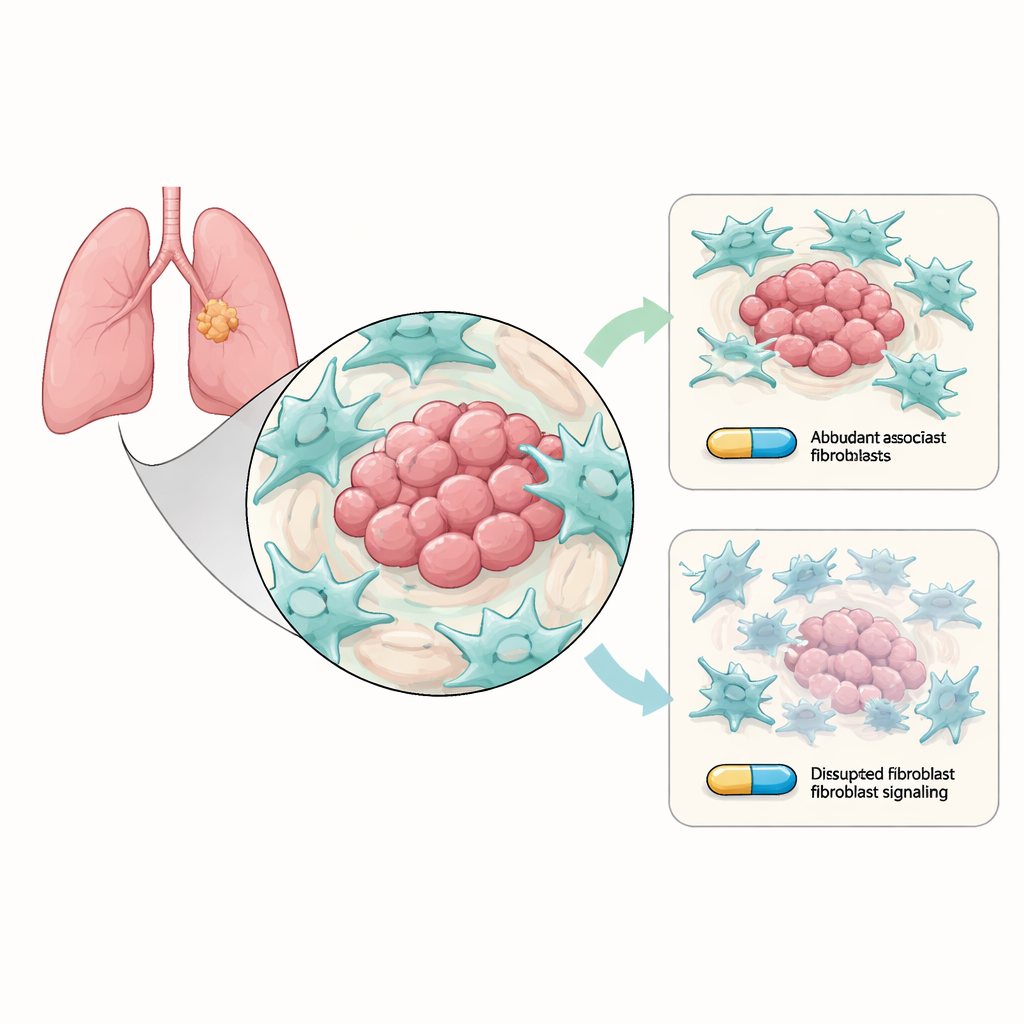
خلايا مساعدة تحمي الورم بصمت
ينمو سرطان الرئة غير صغير الخلايا داخل مجتمع مزدحم من الخلايا غير السرطانية يُعرف ببيئة الورم الدقيقة. ومن بين أكثر الساكنين وفرةً هناك الخلايا الليفية المرتبطة بالسرطان (CAFs)، وهي خلايا نسيج ضام تعيد تشكيل المنطقة المحيطة بالورم. زرع الباحثون خلايا سرطان الرئة الحاملة لطفرات EGFR الحساسة عادةً للأوزيمرتينيب مع خلايا CAFs في المختبر. ووجدوا أنه بوجود CAFs تصبح خلايا السرطان أصعب قتلًا بواسطة الأوزيمرتينيب: شكلت مستعمرات أكثر، قلَّت معدلات الموت الذاتي، وأظهرت سمات أقوى «شبيهة بالجذع» مرتبطة بالبقاء طويل الأمد والانتكاس. بمعنى آخر، رغم أن الدواء ظل يستهدف خلايا السرطان، فإن الخلايا الليفية المحيطة ساعدت بصمت هذه الخلايا على التحمل.
علامة كيميائية على الرنا تغير القواعد
نظرت المجموعة بعد ذلك إلى ما هو أبعد من الجينات نفسها إلى العلامات الكيميائية التي تزيّن الرنا — نسخ العمل من المعلومات الوراثية داخل الخلايا. إحدى هذه العلامات، المسماة m7G، يمكن أن تؤثر على ثبات جزيء الرنا وكفاءته في الترجمة إلى بروتين. باستخدام اختبارات بيوكيميائية ورسم خرائط على مستوى الجينوم، أظهر الباحثون أن CAFs تزيد وسم m7G العام على الرنا داخل خلايا سرطان الرئة. وكان هذا الارتفاع مدفوعًا أساسًا بواسطة إنزيم ناقل ميثيل يُدعى METTL1، الذي يضع علامات m7G على الرنا الرسول. كانت مستويات METTL1 أعلى في أورام الرئة مقارنة بالأنسجة الطبيعية المجاورة وارتبطت بمراضٍ أكثر تقدّمًا وببقاء أسوأ للمرضى، مما يوحي بأن هذا الإنزيم يفعل أكثر من مجرد ضبط الوظائف الخلوية الروتينية.
إشارة مفرزة وسلسلة جزيئية قابلة للاختراق
كيف ترفع CAFs من مستويات METTL1 في خلايا السرطان؟ تشير الدراسة إلى بروتين يُدعى HMGB1 تفرزه CAFs في محيطها. بالمقارنة مع خلايا السرطان، أفرزت CAFs كميات أكبر بكثير من HMGB1. عندما أضاف الباحثون HMGB1 إلى خلايا سرطان الرئة ارتفعت مستويات METTL1 وعلامات m7G؛ وعندما قاموا بحجب HMGB1 في الوسط المهيأ بواسطة CAFs تلاشى هذا التأثير. وبالتفصيل أكثر، حددوا مستهدف رناوي رئيسيًا لـ METTL1: هو NET1، جين يعزز نمو الخلايا وحركتها. زادت CAFs كلًا من وسم m7G ووفرة رنا NET1 والبروتين، وربط METTL1 رنا NET1 ماديًا ليُثبّته. انخفاض METTL1 أدى إلى انخفاض NET1 المعدّل، وإضعاف إشارات بقاء خلايا السرطان، وزيادة الحساسية تجاه الأوزيمرتينيب.
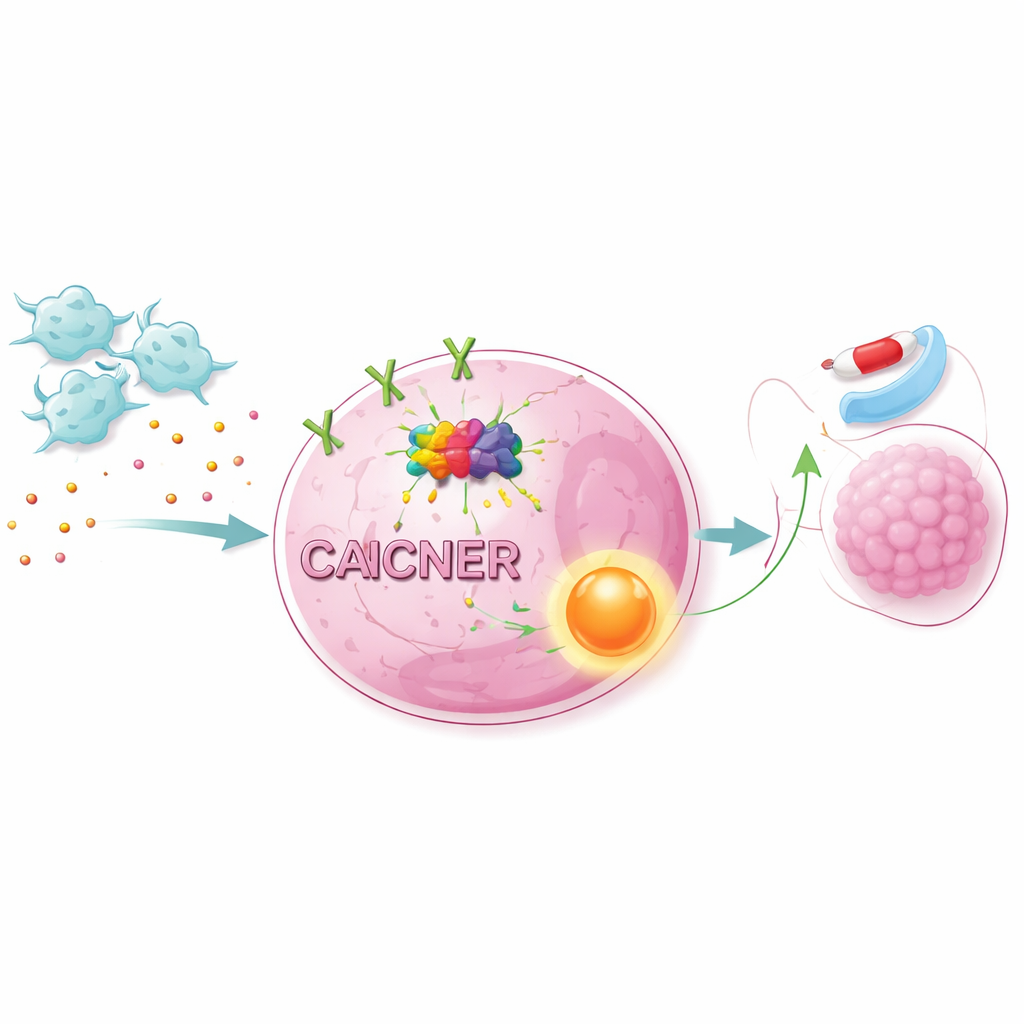
تشغيل مسارات البقاء داخل خلايا السرطان
لم يعمل إشارة NET1 المعززة بمفردها. عبر دمج بيانات رنا واسعة النطاق مع تحليل المسارات، أظهر العلماء أن CAFs تنشط مسارًا رئيسيًا للنمو والبقاء داخل الخلايا يُعرف بمسار AKT/NF-κB. حجب AKT أو NF-κB بمثبطات محددة جعل خلايا سرطان الرئة أكثر عرضة للأوزيمرتينيب، حتى بوجود CAFs. وكان لتغيير مستويات NET1 آثار مماثلة: تقليل NET1 أضعف حماية CAFs، بينما زيادة NET1 عززت المقاومة. في فئران زُرعت فيها خلايا سرطان رئة بشرية، أدى إضافة CAFs إلى نمو أسرع للأورام وقلة استجابة للأوزيمرتينيب. وأدى إسكات METTL1 في خلايا السرطان إلى تقليل علامات m7G وخفض NET1 وتنشيط المسار، ومن ثم خفض حدة نمو الورم المدفوع بواسطة CAFs.
ما معنى هذا لعلاج سرطان الرئة مستقبلاً
بالنسبة للأشخاص المصابين بسرطان الرئة الحامل لطفرات EGFR، يقدم هذا العمل إطارًا جديدًا لفهم سبب فشل أدوية قوية مثل الأوزيمرتينيب في نهاية المطاف. فبدلًا من إلقاء اللوم فقط على الطفرات الجديدة في خلايا السرطان، يبرز السلسلة الجزيئية التي تبدأ خارج خلية الورم — بإفراز CAFs لـ HMGB1 — وتمتد عبر METTL1، وعلامات m7G على NET1، وتنشيط مسارات البقاء التي تُضعف تأثير الدواء. إن مقاطعة هذه السلسلة عند أي نقطة منها قد يعيد، من حيث المبدأ، حساسية العلاج أو يطيلها. وعلى الرغم من أن الأدوية التي تستهدف METTL1 أو HMGB1 أو الرناوات الموسومة بـ m7G مباشرةً لا تزال في مراحل مبكرة، تشير الدراسة إلى أن الجمع بين الأوزيمرتينيب وعلاجات تستهدف الخلايا الداعمة للورم أو إشارات تعديل الرنا قد يساعد في إبقاء هذا الشكل من سرطان الرئة تحت السيطرة لفترة أطول.
الاستشهاد: Qian, Y., Gong, Z., Jia, Y. et al. Cancer-associated fibroblasts promote osimertinib resistance in non-small cell lung cancer cells via METTL1-mediated NET1 m7G modification. Cell Death Dis 17, 248 (2026). https://doi.org/10.1038/s41419-026-08505-7
الكلمات المفتاحية: مقاومة الأوزيمرتينيب, سرطان الرئة غير صغير الخلايا, الخلايا الليفية المرتبطة بالسرطان, مثيلة الرنا, مسار METTL1 NET1