Clear Sky Science · ar
إشارة ROR1-PI3K/AKT تدفع نحو مقاومة تكيُّفية لحصار دورة الخلية في سرطان المبيض المتحور TP53
لماذا يهم هذا البحث لصحة النساء
يُعد سرطان المبيض من أكثر السرطانات فتكًا لدى النساء إلى حد كبير لأن الأورام غالبًا ما تطوّر مقاومة للعلاج الكيميائي. يطرح هذا البحث سؤالًا محوريًا: عندما تُصمم أدوية قوية لدفع الخلايا السرطانية نحو خطأ انقسامي قاتل، كيف تَجد تلك الخلايا طرقًا للبقاء على قيد الحياة، وهل يمكن تحويل ممر الهروب هذا إلى نقطة ضعف؟ من خلال تتبّع خلايا سرطان المبيض لأسابيع أو أشهر أثناء العلاج، يكشف الباحثون عن نظام تحكم مركزي داخل الخلايا يقرر ما إذا كانت ستستمر في الانقسام أو تتوقف لإصلاح الضرر — ويعرضون نهجًا جديدًا لمهاجمة الأورام التي تعلّمت مقاومة الأدوية القياسية. 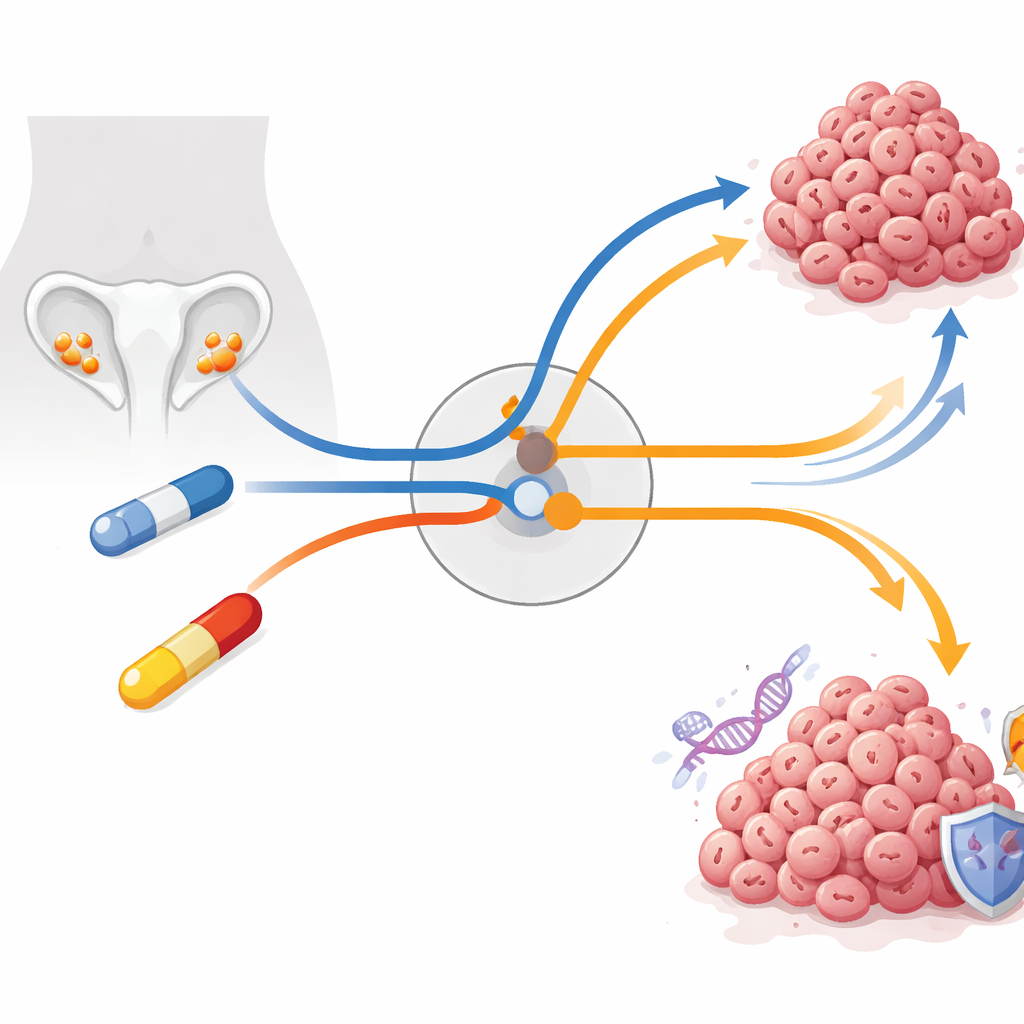
دواءان شائعا الاستخدام، وممر هروب واحد مشترك
ركّز الفريق على سرطان المبيض المصلي عالي الدرجة، وهو الشكل الأكثر عدوانية وانتشارًا من المرض، الذي يحمل تقريبًا دائمًا طفرات في جين TP53 المعروف بـ«حارس الجينوم». وبما أن TP53 معطّل، تعتمد هذه الأورام بشكل غير عادي على نقاط تحقق لاحقة في دورة انقسام الخلية. يستغل دواءان مستخدمان أو قيد الاختبار هذه الضعف: أدافوزرتيب، وهو مثبط WEE1 تجريبي يدفع الخلايا المتضررة إلى الانقسام مبكرًا، وباكليتاكسيل، عقار كيميائي أساسي يعطل الهيكل الداخلي اللازم لانفصال الكروموسومات. من الناحية النظرية، ينبغي أن يدفع كلاهما الخلايا السرطانية إلى «كارثة انقسامية» — فشل انقسامي قاتل. ومع ذلك، في العيادة والمختبر، تتكيف الأورام في كثير من الأحيان. أنشأ الباحثون نماذج خلايا مقاومة طويلة الأمد بزيادة جرعات الدواء تدريجيًا على مدى شهور، بما يحاكي ما يحدث للمرضى بشكل أفضل من تجارب الجرعات القصيرة والعالية.
كيف تعيد الخلايا السرطانية تشكيل نفسها للبقاء
باستخدام تصوير متقدم وتقنية «دهان الخلية» (Cell Painting) التي تصبغ هياكل خلوية متعددة في آن واحد، لاحظ العلماء أن الخلايا المقاومة لم تَعد تشبه سابقاتها ببساطة. كثير منها كان متعدد النوى، ومعاد تنظيم الهياكل الداخلية، وشكل تجمعات أكثر إحكامًا وكُريات ثلاثية الأبعاد أصغر وأكثر تشتتًا — وهي علامات على تحول جزئي في الشكل يعرف بالانتقال الظهاري-اللحمي. أشارت هذه التغيرات الفيزيائية إلى أن الخلايا أعادت توصيل طرق حركتها وانقسامها وتفاعلها. في الوقت نفسه، أظهر تسلسل الرنا المفرد تفصيليًا أن كل دواء وخط خلوي طوّرا نمطًا خاصًا من الجينات والكروموسومات المتغيرة. رغم هذا التنوع الجيني، برز موضوع ثابت: نشاط مسار النمو والبقاء المتمركز حول PI3K وAKT ارتفع عبر النماذج المقاومة، غالبًا بمرافقة مسارات إشارية ذات صلة مثل MAPK وNF-κB.
مفتاح خلوي بين «التجاوز السريع» و«الإصلاح البطيء»
بالتعمق أكثر، وجد الباحثون أن نظام PI3K/AKT يعمل كمفتاح يقلب الخلايا السرطانية بين استراتيجيتين للبقاء. في وضع «التجاوز السريع»، يؤدي ارتفاع نشاط PI3K/AKT إلى تعطيل بروتين الكبح FOXO3 وإضعاف نقاط التحقق في دورة الخلية، مما يسمح للخلايا بالاستمرار في الانقسام وتجنّب التأثيرات المميتة لأدافوزرتيب أو باكليتاكسيل. في وضع معاكس «الإصلاح البطيء»، يكون نشاط PI3K/AKT أقل، يبقى FOXO3 نشطًا في النواة، وتبطئ الخلايا نسخها، وتشغّل برامج إصلاح الحمض النووي، وتطرد الأدوية بكفاءة أكبر. من اللافت أن التعرض القصير الأجل للأدوية حفّز اندفاعًا حادًا لنشاط PI3K/AKT في جميع النماذج؛ ثم استقرت المقاومة الطويلة الأمد في إما حالة التجاوز السريع أو الإصلاح البطيء اعتمادًا على الخلفية الجينية والإشارات السابقة للسرطان. هذا يبيّن أن نفس المحور المركزي يمكن أن يدعم مسارات هروب مختلفة تمامًا. 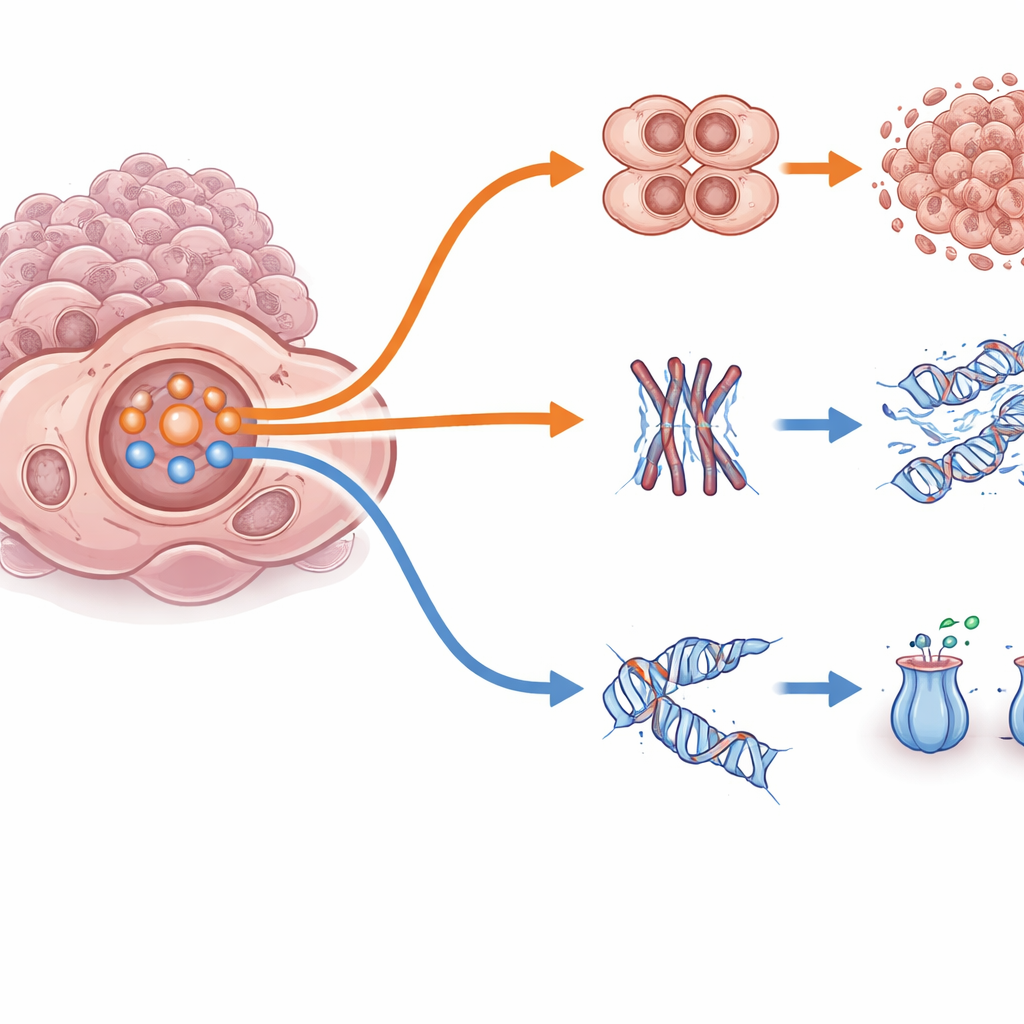
تحويل إشارة المقاومة إلى هدف علاجي
أحد العناصر العليا في هذا المحور هو ROR1، مستقبل بروتيني نادرًا ما يوجد في الأنسجة البالغة الطبيعية لكنه مرتفع في عدة أنواع من السرطان. في العديد من نماذج سرطان المبيض المقاومة، ارتفعت مستويات ROR1 جنبًا إلى جنب مع نشاط PI3K/AKT. أظهر الفريق أن زيادة أو خفض ROR1 يمكن أن يغيّر سهولة اكتساب الخلايا للمقاومة تجاه أدافوزرتيب أو باكليتاكسيل، وبشكل معتمد على السياق. والأهم من ذلك، اختبروا زيليفرتاماب-فيدوتين، رابط عقار-مضاد للأجسام المضادة يستهدف ROR1 ويوصل حمولة سامة. في خطوط الخلايا ونماذج العضيات الثلاثية الأبعاد المأخوذة من المرضى، كانت الأورام المقاومة لأدافوزرتيب والمرتفعة ROR1 عرضة بشكل خاص لهذا العامل، وغالبًا ما عزّز الجمع بينه وبين أدافوزرتيب قتل الخلايا. كانت بعض نماذج المقاومة ضد باكليتاكسيل أقل استجابة، على الأرجح لأنها طوّرت أيضًا قدرة أكبر على طرد الأدوية.
ماذا يعني هذا لعلاج سرطان المبيض في المستقبل
يعيد هذا العمل تأطير مقاومة الأدوية في سرطان المبيض المتحور TP53 ليس كحدث عشوائي بل كرد منسق تحكمه مفاتيح إشارية مركزية. من خلال تحديد محور PI3K/AKT–FOXO3 وROR1 كنقاط رئيسية، يشير البحث إلى استراتيجيات عملية: إقران الأدوية المستهدفة للانقسام مثل أدافوزرتيب وباكليتاكسيل بعلاجات تمنع محور المقاومة أو تستغل وجود ROR1 على الخلايا المقاومة. وبما أن ROR1 يكاد يكون غائبًا عن الأنسجة السليمة، قد تتيح مثل هذه التركيبات مهاجمة الأورام المتكررة والمصقولة بالأدوية بشكل انتقائي مع حفاظ نسبي على الخلايا الطبيعية. ورغم أن هذه النتائج جاءت من نماذج مخبرية وزُرعات مأخوذة من المرضى وليس من تجارب سريرية مكتملة، فإنها تقدم خارطة طريق واضحة لتصميم علاجات أكثر ذكاءً وديمومة للنساء المصابات بسرطان المبيض المصلي عالي الدرجة.
الاستشهاد: Raivola, J., Rantanen, F., Dini, A. et al. ROR1-PI3K/AKT signaling drives adaptive resistance to cell cycle blockade in TP53 mutated ovarian cancer. Cell Death Dis 17, 276 (2026). https://doi.org/10.1038/s41419-026-08501-x
الكلمات المفتاحية: سرطان المبيض, مقاومة الأدوية, مسار PI3K AKT, علاج بالأجسام المضادة ضد ROR1, مثبطات دورة الخلية