Clear Sky Science · ar
ΔNp63α يحفّز تخليق السيرين لتعزيز مقاومة الكاربوبلاتين في سرطان الرئة غير صغير الخلايا
لماذا يهم تجويع الخلايا السرطانية من مغذٍّ «غير أساسي»
معظمنا يفكر في علاج السرطان على أنه أدوية قوية تقتل الخلايا الورمية مباشرة. تُظهر هذه الدراسة أن ما تتغذى عليه الخلايا السرطانية قد يكون بنفس الأهمية. اكتشف الباحثون أن أنواعاً معينة من سرطانات الرئة تعيد توصيل طرق تصنيعها واستخدامها لحمض الأمين السيرين، مما يساعدها على البقاء أمام الدواء الكيميائي الشائع الكاربوبلاتين. بفهم هذه الحيلة الأيضية الكامنة واستهدافها، قد يتمكّن الأطباء مستقبلاً من زيادة فاعلية العلاجات القياسية—ببساطة عبر الجمع بين الأدوية وتعديلات في وصول الأورام إلى مغذيات محددة.
خط إمداد يغذي أورام الرئة العنيدة
سرطان الرئة هو السبب الرئيسي للوفيات الناجمة عن السرطان عالمياً، ويشكّل سرطان الرئة غير صغير الخلايا (NSCLC) نحو 85% من الحالات. ضمن NSCLC، يمتلك نوع يُسمى سرطان الخلايا الحرشفية للرئة (LUSC) خيارات علاجية موجهة أقل بكثير من الأشكال الأخرى ولا يزال يعتمد بشكل كبير على العلاج الكيميائي القائم على الكاربوبلاتين. ركّز المؤلفون على السيرين، حمض أميني تستخدمه الخلايا السرطانية كقِطع لبناء الحمض النووي والبروتينات والدهون، وكجزء أساسي من دفاعاتها المضادة للأكسدة. رغم أن أجسامنا قادرة على صنع السيرين، يبدو أن الأورام العدوانية تعزز كلّاً من إنتاجه وامتصاصه، ما يشير إلى أنها قد تكون معتمدة بشكل غير عادي على هذا المغذّي للنمو والبقاء.
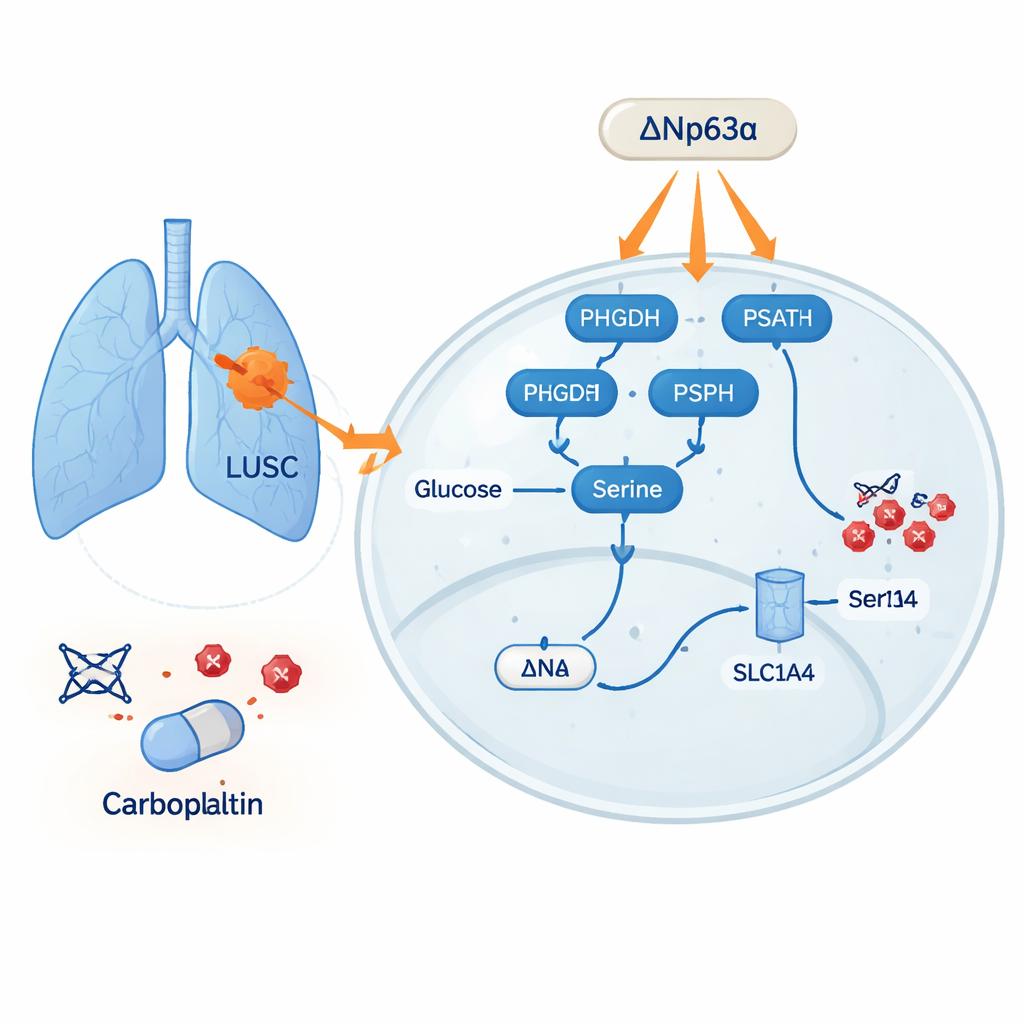
المسار الأيضي الكامن وراء المقاومة
باستخدام مجموعات بيانات وسجلات مرضى عريضة وعينات ورمية، أظهر الفريق أن عدة بروتينات مشاركة في تصنيع واستيراد السيرين—PHGDH وPSAT1 وPSPH والناقلة SLC1A4—مرتفعة باستمرار في سرطانات الرئة مقارنةً بالنسيج الرئوي الطبيعي. ارتبطت مستويات هذه الجينات المرتبطة بالسيرين ببقاء أسوأ. كان التأثير أقوى في سرطان الخلايا الحرشفية، الذي أظهر مزيداً من هذه الإنزيمات ومحتوى أعلى من السيرين مقارنةً بسرطان غُدّة الرئة. في مزروعات الخلايا، كانت الخلايا السرطانية ذات محتوى السيرين الأعلى أقل حساسية للكاربوبلاتين، وإضافة سيرين إضافي ساعدها على تحمل أثر الدواء. في الفئران، قاومت الأورام عند الحيوانات التي غذيت بنظام عالي السيرين الكاربوبلاتين، بينما تقلصت الأورام في الفئران ذات الحميات الفقيرة بالسيرين أكثر تحت نفس العلاج.
جين نسبي يرفع إنتاج السيرين إلى الحد الأقصى
تساءل الباحثون بعد ذلك لماذا خلايا LUSC جيدة جداً في صناعة السيرين. ركّزوا على ΔNp63α، بروتين يعمل كمُنظّم «نسبي» في السرطانات الحرشفية وغالباً ما يُستخدم لتشخيص LUSC. من خلال تحليل بيانات التعبير الجيني العامة وإجراء تجارب جزيئية، وجدوا أن الأورام ذات مستويات عالية من ΔNp63α أظهرت أيضاً تعبيراً مرتفعاً للرباعي الأساسي من جينات مسار السيرين. في خطوط الخلايا، رفع ΔNp63α زاد كمية السيرين داخل الخلايا، بينما خفضه نقلها إلى مستوى أقل. أظهرت اختبارات أخرى أن ΔNp63α يرتبط مباشرة بمناطق التحكم في جينات مسار السيرين ويشغّلها، عاملٌ رئيسي يرفع إنتاج واستيراد السيرين في خلايا سرطان الرئة الحرشفية.
كيف يحمي السيرين الإضافي الخلايا من العلاج الكيميائي
يقتل الكاربوبلاتين الخلايا السرطانية أساساً بإتلاف حمضها النووي وزيادة جزيئات أكسجين ضارة تُسمى أنواع الأكسجين التفاعلية (ROS). يساعد السيرين الخلايا بطريقتين حاسمتين: فهو يزوّد المواد الخام لصنع اللبنات الأساسية للحمض النووي ويغذي إنتاج الغلوتاثيون، مضاد أكسدة رئيسي يلتقط ROS. عندما أزال العلماء السيرين وحمض الغليسين القريب منه من وسط مزروعات الخلايا، تسبّب الكاربوبلاتين في مزيد من انكسارات الحمض النووي ومستويات أعلى بكثير من ROS. إعادة إضافة الفورمات (ناتج من السيرين يُستخدم لتخليق الحمض النووي) أو مضاد أكسدة أنقذت الخلايا جزئياً، واستخدام الاثنين معاً أعاد بقاءها تقريباً. في خلايا سرطان الرئة الحرشفية التي تصنّع الكثير من السيرين بالفعل، جعل حجب إنزيم PHGDH بدواء (NCT‑503) الكاربوبلاتين أكثر فعالية بكثير، في المختبر وفي أورام الفئران على حد سواء.
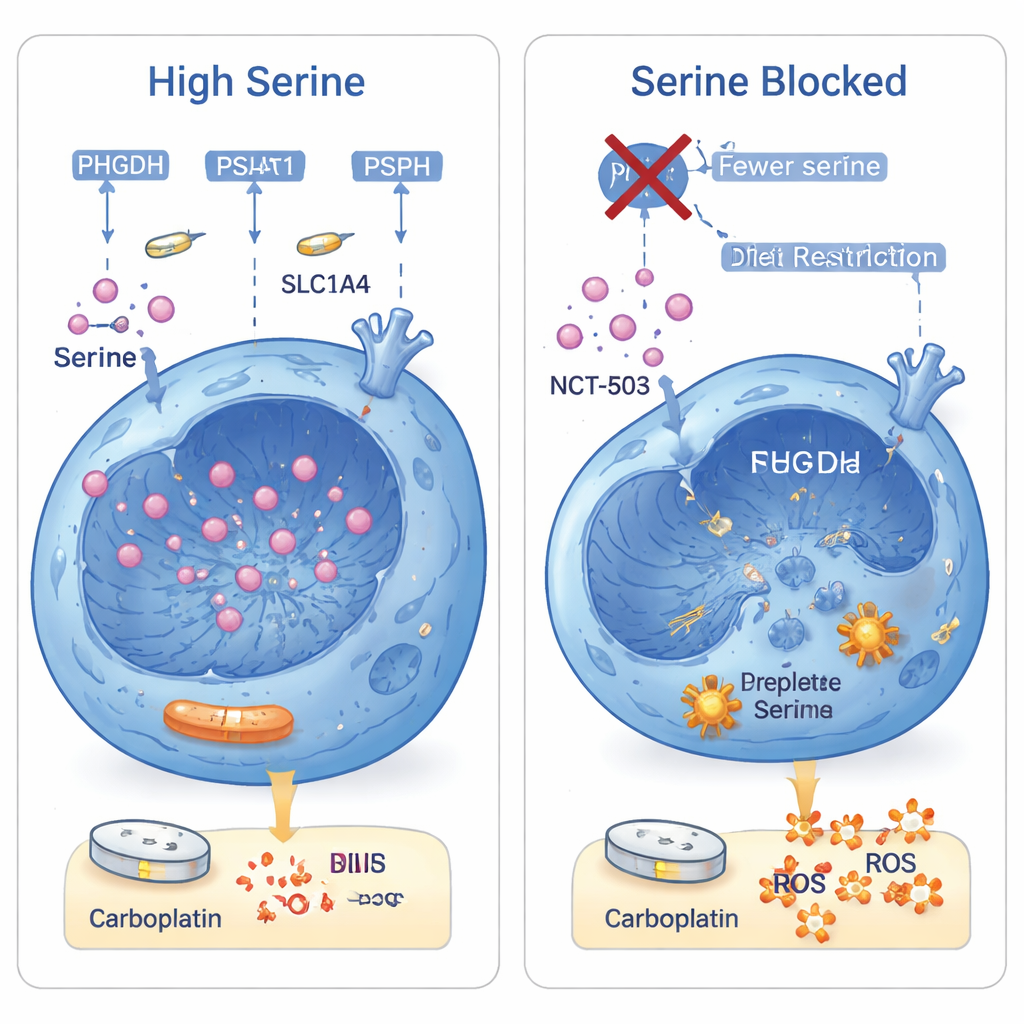
تحويل ضعف إلى فرصة علاجية
الرسالة الأساسية للقارئ العادي هي أن بعض سرطانات الخلايا الحرشفية للرئة تنجو من العلاج الكيميائي عبر الإفراط في إنتاج حمض أميني واحد، السيرين، تحت سيطرة جين ΔNp63α. يسمح هذا السيرين الإضافي للخلايا الورمية بإصلاح أضرار الحمض النووي التي يحدثها الكاربوبلاتين وتحييد الجزيئات السامة التي كانت ستقتلها. تُظهر الدراسة أنه إذا قُطعت كِلتا «المصنع» الداخلي لإنتاج السيرين وخط الإمداد الخارجي من النظام الغذائي، يعمل الكاربوبلاتين بشكل أفضل بكثير. بعبارة أخرى، عن طريق الجمع بين العلاج الكيميائي القياسي وأدوية تُعيق إنتاج السيرين ومعالجات غذائية مُدارة بعناية، قد يتمكن الأطباء مستقبلاً من التفوق على آلية مقاومة رئيسية في شكل من أشكال سرطان الرئة يصعب علاجه.
الاستشهاد: Deng, L., Yang, X., Zhang, J. et al. ΔNp63α drives serine synthesis to promote carboplatin resistance in NSCLC. Cell Death Dis 17, 227 (2026). https://doi.org/10.1038/s41419-026-08497-4
الكلمات المفتاحية: تمثّل السيرين, سرطان الخلايا الحرشفية للرئة, مقاومة الكاربوبلاتين, ΔNp63α, علاج أيض السرطان