Clear Sky Science · ar
NSD2 يثبط التعبير عن PD-L1 عبر الفسفرة التأكسدية للتحكم في المراقبة المناعية في سرطان الكبد الخلوي
لماذا تهم هذه القصة عن سرطان الكبد
سرطان الكبد الخلوي، الشكل الأكثر شيوعًا لسرطان الكبد، يُشخّص غالبًا في مراحل متأخرة ومقاوم للعديد من العلاجات. تساعد أدوية العلاج المناعي التي تحجب "عباءة التخفي" PD-L1 على الخلايا الورمية بعض المرضى، لكنها لا تفيد الأغلبية. يكشف هذا البحث عن لاعب غير متوقع، بروتين يدعى NSD2، يربط بين كيفية حصول خلايا سرطان الكبد على الطاقة ومدى ظهورها أمام الجهاز المناعي. قد يشير فهم هذا الارتباط إلى طرق جديدة لتعزيز العلاجات الحالية وتحديد المرضى المرجح أن يستفيدوا منها.
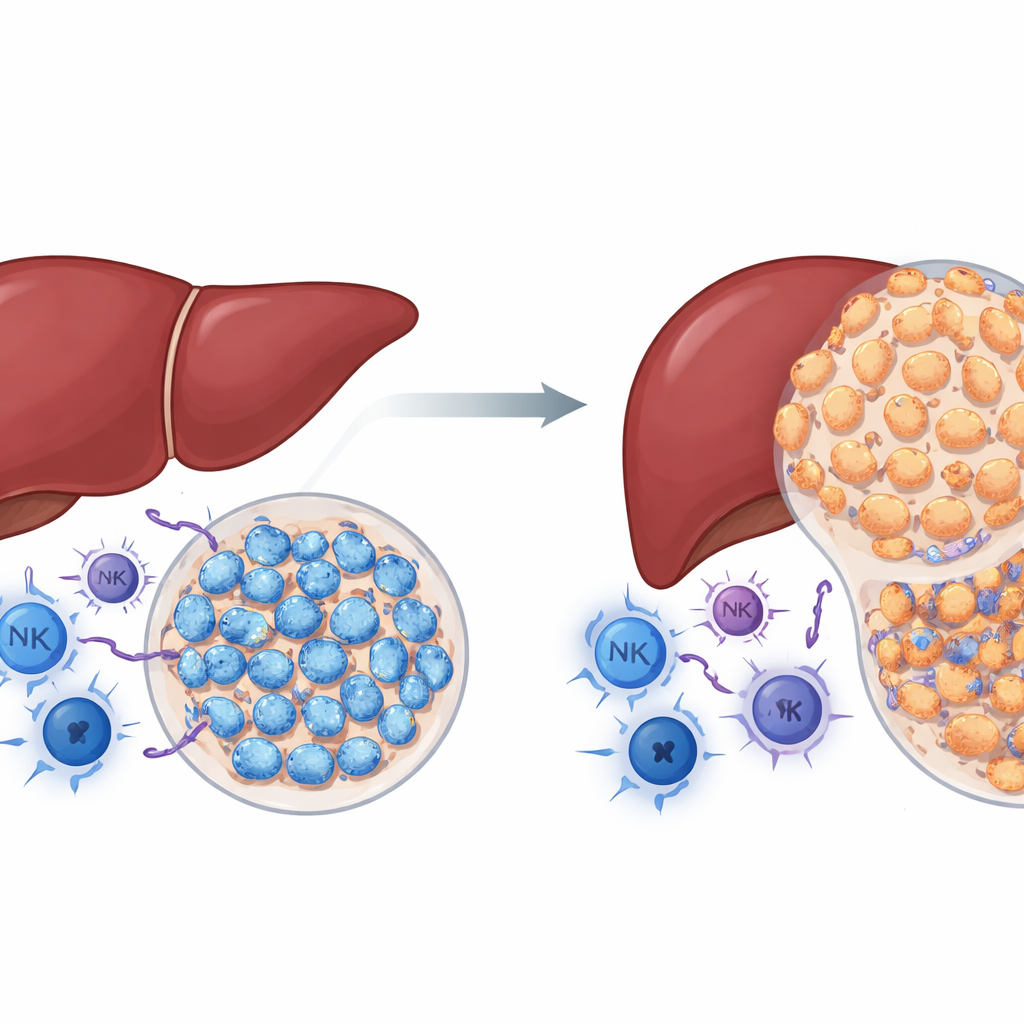
دور مفاجئ لبروتين سرطاني معروف
NSD2 هو إنزيم يعدل الهستونات، البروتينات التي تلتف حولها الحمض النووي. في العديد من السرطانات، اعتُبر NSD2 دافعًا لنمو الورم. تساءل المؤلفون عما إذا كان الحال نفسه في سرطان الكبد. باستخدام فئران معدلة وراثيًا تُفعَّل فيها NSD2 خصيصًا في خلايا الكبد، عالجوا الحيوانات بمادة كيميائية تحفز تكوّن أورام الكبد بشكل موثوق. وعلى خلاف التوقعات، طورت الفئران ذات التعبير الزائد عن NSD2 عددًا أقل بكثير من الأورام وأحجامًا أصغر مقارنة بالفئران العادية، وأظهرت أكبادها أضرارًا وتندبًا وتكاثرًا خلويًا أقل. في الوقت نفسه، احتوت الأورام في أكباد فائض NSD2 على خلايا مناعية مضادة للسرطان أكثر، بما في ذلك خلايا T المساعدة والقاتلة والخلايا القاتلة الطبيعية. تشير هذه النتائج إلى أن NSD2، في وجود جهاز مناعي سليم، يتصرف أقل كمسارع وأكثر ككابح لسرطان الكبد.
مصانع الطاقة واستخدام الوقود في خلايا الورم
لفهم كيف يقيّد NSD2 الأورام، قام الفريق بتحليل نشاط الجينات في نسيج الكبد. وجدوا أن التعبير الزائد عن NSD2 يخفض بقوة جينات المشاركة في الفسفرة التأكسدية، العملية التي تولّد بها المتقدرات — "محطات الطاقة" الخلوية — الطاقة باستخدام الأكسجين. أظهرت تجارب لاحقة في خطوط خلايا سرطان كبد من الفئران والبشر أن تعزيز NSD2 خفض تعبير العديد من جينات الفسفرة التأكسدية، وقلل استهلاك الأكسجين وإنتاج ATP، وخفض الجهد الغشائي للمتقدرة، وهو علامة على نشاط متقدري أضعف. وفي الوقت نفسه، استهلكت هذه الخلايا كمية أقل من الجلوكوز لكنها لم تحول اعتمادها نحو التحلل السكري، مما يشير إلى انخفاض صاف في إنتاج الطاقة. أما فقدان NSD2 فكان له تأثيرات معاكسة، حيث عزز قدرة المتقدرات واستخدام الوقود.
كيف يعيد NSD2 توصيل الطاقة والوضوح المناعي
بتعمق أكبر، جمع الباحثون رسم خرائط الكروماتين على مستوى الجينوم مع بيانات التعبير الجيني وحددوا مجموعة من الجينات المنشطة مباشرة بوجود NSD2. اثنان من هذه الجينات، Camk2d وPrkce، معروفان بأنه يقيّدان نشاط المتقدرات. زاد NSD2 علامة هستونية معينة (H3K36me2) عند محرضاتهما، معززًا تعبيرهما. إعادة إدخال هذه الجينات في خلايا سرطان الكبد الناقصة لـ NSD2 خفضت استهلاك الأكسجين المتقدري وإنتاج ATP، مما يؤكد أنهما يعملان كفرامل ناتجة عن NSD2 على الفسفرة التأكسدية. والأهم أن أعمالًا سابقة أشارت إلى أن المتقدرات النشطة بقوة تفضّل ارتفاع مستويات PD-L1 على الخلايا الورمية. متسقًا مع ذلك، وجد المؤلفون أن التعبير الزائد عن NSD2 خفض مستويات PD-L1، بينما رفع فقدان NSD2 PD-L1 على خلايا سرطان الكبد وفي نسيج الورم.
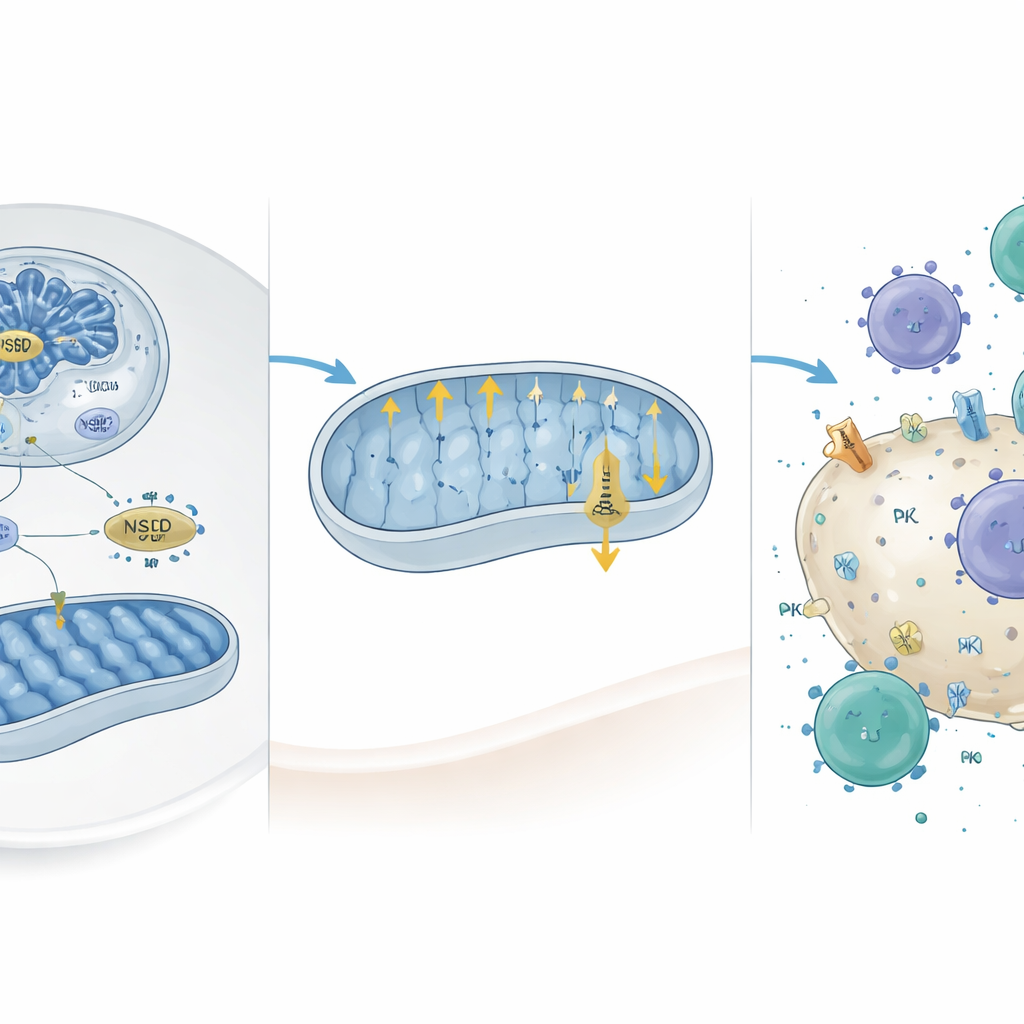
خفض الدرع وإيقاظ الهجوم المناعي
اختُبرت الأهمية الوظيفية لهذه التحولات الجزيئية في فئران تلقت حقنًا كبدية بخلايا سرطانية مُهندَسة لكسب أو فقدان NSD2. شكلت الخلايا الناقصة لـ NSD2 أورامًا أكبر بسرعة، عبرت عن PD-L1 بمستويات أعلى واحتوت على خلايا T وخلايا قاتلة طبيعية أقل، خصوصًا خلايا T القاتلة النشطة. عندما حجب الباحثون كيميائيًا المركب V المتقدري، وهو مكون رئيس في الفسفرة التأكسدية، انخفضت مستويات PD-L1 في الخلايا الناقصة لـ NSD2 عائدةً نحو الطبيعي وتمكنت الخلايا المناعية من تحفيز موت الخلايا الورمية بشكل أفضل. بالمثل، أدى التعبير الزائد عن Camk2d أو Prkce في الخلايا الناقصة لـ NSD2، أو علاج الأورام بأضداد تحجب PD-L1، إلى تقليص حجم الورم واستعادة تسلل الخلايا المناعية. في مجموعات بيانات المرضى، ارتبط انخفاض تعبير NSD2 ببقاء أسوأ ولكن، وبشكل لافت، باستجابة أفضل لعلاج يستهدف PD-L1، مما يوحي أن حالة NSD2 قد تساعد في توقع من سيستفيد من مثل هذه الأدوية.
ما معنى هذا لعلاج سرطان الكبد في المستقبل
للقارئ العام، الرسالة الرئيسية أن هذه الدراسة تعيد تعريف NSD2 كعامل مكبح للورم في سرطان الكبد، على الأقل بوجود جهاز مناعي عامل. عن طريق خفض إنتاج الخلية للطاقة المعتمد على الأكسجين، يخفض NSD2 بشكل غير مباشر PD-L1 على الخلايا الورمية، ماسحًا جزءًا من "عباءة التخفي" ويسمح للخلايا المناعية بالتعرف عليها ومهاجمتها. تشير سلسلة NSD2–الطاقة–PD-L1 الموصوفة حديثًا إلى فكرتين عمليتين: أولًا، قد يكون المرضى الذين تفتقر أورامهم إلى NSD2 مرشحين جيدين بشكل خاص لأدوية تحجب PD-L1؛ وثانيًا، قد يوفر الجمع بين أدوية تثبط إنتاج الطاقة المتقدري والعلاج المناعي ضربة مزدوجة قوية ضد سرطان الكبد.
الاستشهاد: Zhang, W., Feng, W., Ma, C. et al. NSD2 inhibits the expression of PD-L1 via oxidative phosphorylation to control immune surveillance in hepatocellular carcinoma. Cell Death Dis 17, 284 (2026). https://doi.org/10.1038/s41419-026-08490-x
الكلمات المفتاحية: سرطان الكبد الخلوي, NSD2, الفسفرة التأكسدية, PD-L1, العلاج المناعي للأورام