Clear Sky Science · ar
DNMT2 يعيق تقدم سرطان الغدة الدرقية غير المتمايز عن طريق خفض إنتاج 5’tiRNAGly-GCC
لماذا تهم هذه الكيمياء الخفية للحمض النووي الريبوزي
سرطان الغدة الدرقية غير المتمايز هو من أخطر أنواع السرطان لدى البشر، وغالبًا ما يقتل المرضى خلال أشهر رغم الجراحة والإشعاع والعلاج الكيميائي. تكشف هذه الدراسة عن متسبب مفاجئ داخل خلايا السرطان: علامات كيميائية صغيرة على الحمض النووي الريبوزي الناقل (tRNA)، الجزيئات التي تساعد على بناء البروتينات. يُظهر المؤلفون أنه عند فقدان أو انخفاض إنزيم معين، DNMT2، تنمو الأورام الدرقية أسرع، وتنتشر بسهولة أكبر، وتقاوم الدواء العلاجي الشائع دوكسوروبيسين. والأكثر إثارة للاهتمام أنهم يحددون قطعة صغيرة من الحمض النووي الريبوزي تظهر عندما يكون DNMT2 منخفضًا ويبرهنون أن حجب هذه القطعة قد يصبح استراتيجية علاجية جديدة.
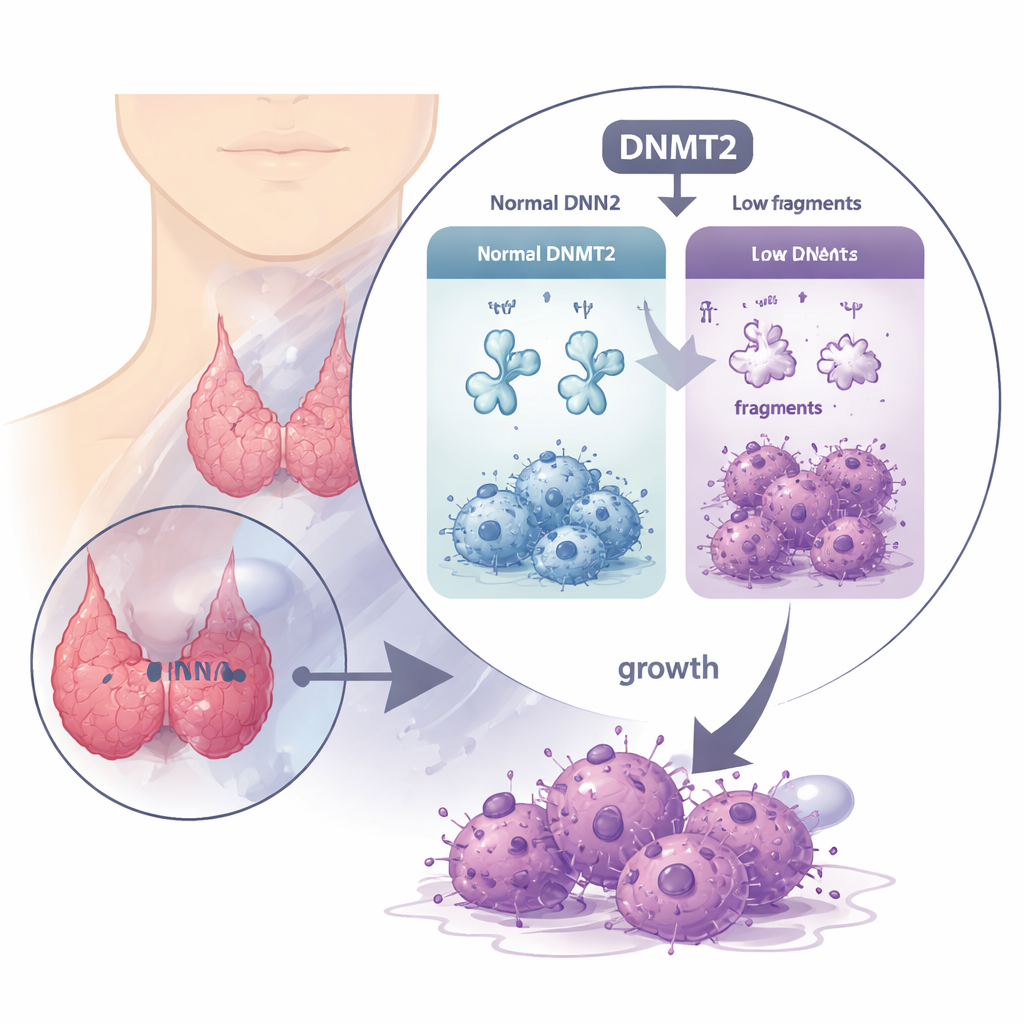
إنزيم وقائي يختفي
عادةً ما تحمل الحَمْضَاتُ النّاقِلَة للأحماض الأمينية إلى آلة تصنيع البروتين في الخلية، وثباتها يعتمد على زخارف كيميائية دقيقة. DNMT2 هو إنزيم يضيف إحدى هذه العلامات، مجموعة ميثيل، إلى مواقع محددة على الـ tRNA. في العديد من السرطانات يكون DNMT2 مرتفعًا ويُعتقد أنه يساعد الأورام، لكن هنا القصة معكوسة. من خلال تحليل قواعد بيانات كبيرة للمرضى وعينات أورام، وجد الباحثون أن مستويات DNMT2 أقل بكثير في نسيج سرطان الغدة الدرقية غير المتمايز مقارنة بالغدة الدرقية الطبيعية. ويميل المرضى الذين تحتوي أورامهم على DNMT2 أعلى إلى العيش لفترة أطول دون تدهور السرطان، ما يشير إلى أن DNMT2 يعمل كفرامل أكثر منه كمسرِّع في هذا المرض.
كيف يغذي انخفاض DNMT2 السلوك العدواني
لمعرفة ما يفعله DNMT2 فعليًا في خلايا السرطان، عبَّرت الفريق عن تعديل مستوياته في خطوط خلايا سرطان الغدة الدرقية غير المتمايز المزروعة في أطباق ونماذج الفئران. عندما انخفض DNMT2، تكاثرت الخلايا أسرع، وغزت الأغشية بسهولة أكبر، وشكلت مستعمرات أكثر، وهي جميعها علامات على ورم عدواني. كما أصبحت هذه الخلايا أقل حساسية للدواء دوكسوروبيسين، الدواء القياسي لهذا السرطان. في الفئران، نمت الأورام المهندسة لتحتوي على DNMT2 أقل بشكل أكبر وانتشرت إلى الرئتين بسهولة أكبر، بينما أدى تعزيز تعبير DNMT2 إلى التأثير المعاكس. وتتبع الباحثون هذه التغيرات جزئيًا إلى تنشيط برنامج خلوي معروف باسم انتقال الظهارة إلى اللحمة (epithelial–mesenchymal transition)، الذي يجعل خلايا السرطان أكثر قابلية للحركة والغزو.
من tRNA المتضرر إلى شظايا صغيرة ضارة
بالغوص أعمق، تُظهر الدراسة أن DNMT2 يضع علامة ميثيل في موضع محدد (يسمى C38) على ثلاثة أنواع فقط من tRNA. دون هذا الحماية، تصبح هذه الـ tRNA أكثر عرضة للقطع بواسطة إنزيم آخر، الأنجيوجينين. ذلك القطع يولد قطعة قصيرة من الحمض النووي الريبوزي مشتقة من tRNA-Gly-GCC، وتسمى 5’tiRNAGly-GCC. باستخدام التسلسل والاختبارات البيوكيميائية، وجد المؤلفون أنه عندما يكون DNMT2 منخفضًا، يتراكم هذا النسيج، خصوصًا من tRNA الحاملة للجلايسين. في تجارب أنبوبية، إضافة علامة الميثيل حمت الـ tRNA بقوة من أن تُقطع، مؤكدة أن DNMT2 عادةً ما يحمي هذه الجزيئات من التقطيع إلى قطع أصغر قد تكون ضارة.
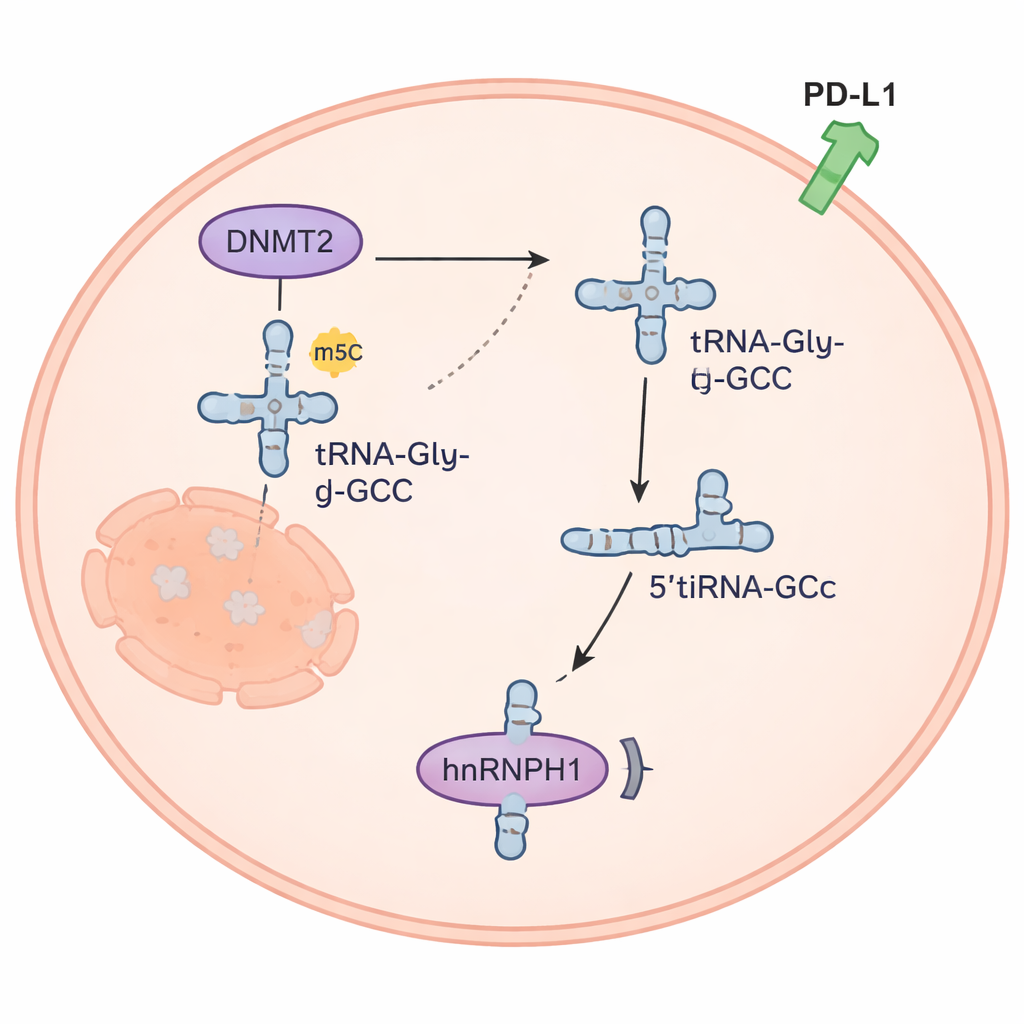
قطعة RNA صغيرة تعيد توصيل إشارات السرطان
تبين أن قطعة 5’tiRNAGly-GCC أكثر من مجرد حطام جزيئي. كانت وفيرة في خلايا سرطان الغدة الدرقية غير المتمايز ونادرة في الخلايا الدرقية الطبيعية. عندما رفع الباحثون مستوياتها تصنعيًا، تكاثرت الخلايا السرطانية أسرع، وغزت أكثر، وأصبحت أكثر مقاومة للدوكسوروبيسين؛ كما أن خفض هذه القطعة أعطى التأثير المعاكس. في الفئران، أبطأ مثبط مصمم كيميائيًا لـ5’tiRNAGly-GCC نمو الورم، والجمع بين هذا المثبط والدوكسوروبيسين كان أكثر فعالية من أي علاج بمفرده. اكتشف الفريق أن 5’tiRNAGly-GCC ترتبط ببروتين يُدعى hnRNPH1، مما يقلل من كميته داخل الخلايا. ولأن hnRNPH1 عادةً ما يساعد في ضبط مستويات البروتين المرتبط بالمناعة PD-L1، فإن فقدان hnRNPH1 يسمح بارتفاع PD-L1، وهو تغيير يمكن أن يساعد الأورام على الهروب من الهجوم المناعي ويرتبط بتراكم الخلايا التائية المنظمة حول الأورام.
ماذا يعني هذا للعلاجات المستقبلية
بعبارة بسيطة، تكشف الدراسة عن تفاعل سلسلة: عندما يكون DNMT2 منخفضًا، تفقد بعض الـ tRNA علامة حمائية، وتُقَطع إلى شظايا صغيرة، وتُعطل إحدى هذه الشظايا (5’tiRNAGly-GCC) بروتينًا يكبح PD-L1. النتيجة هي سرطان أكثر عدوانية ومقاومة للأدوية وقادر على التملص من الجهاز المناعي. بدلًا من محاولة رفع DNMT2 مباشرة — وهو ما قد يكون محفوفًا بالمخاطر في أنسجة أخرى — يقترح المؤلفون استهداف قطعة الحمض النووي الريبوزي الضارة نفسها. تجاربهم على الفئران باستخدام مثبط 5’tiRNAGly-GCC، لا سيما عند الجمع مع الدوكسوروبيسين، تقدم دليلًا مبكرًا أن تعطيل هذه الدائرة الدقيقة من الحمض النووي الريبوزي قد يساعد في ترويض أحد أخطر أشكال سرطان الغدة الدرقية.
الاستشهاد: Zhou, R., Li, B., Cao, M. et al. DNMT2 inhibits anaplastic thyroid cancer progression by downregulating 5’tiRNAGly-GCC production. Cell Death Dis 17, 240 (2026). https://doi.org/10.1038/s41419-026-08488-5
الكلمات المفتاحية: سرطان الغدة الدرقية غير المتمايز, DNMT2, شظايا الحمض النووي الريبوزي الناقلة (tRNA), مقاومة الكيمياء الدوائية, PD-L1