Clear Sky Science · ar
استهداف فوسفوتياز الميتوكوندريا PGAM5 يخفف من الفيروسبتوز والتهاب البنكرياس الحاد عبر زيادة تعبير FSP1 بوساطة NRF2
لماذا تهم الخلايا المتعبة والبنكرياسات المؤلمة
عندما تُدفع الخلايا إلى حدٍّ مفرط، يمكن أن تموت بطرق تضر بالجسم كله. أحد أشكال موت الخلايا هذا، المسمى الفيروسبتوز، يقوده الحديد وتفاعلات كيميائية خارجة عن السيطرة تؤدي إلى تزنخ الدهون في أغشية الخلايا. ارتبط هذا المسار بإصابات أعضاء مختلفة، بما في ذلك حالة مؤلمة وأحيانًا مميتة تعرف بالتهاب البنكرياس الحاد. تكشف الدراسة التي يستعرضها هذا المقال عن مفتاح تحكم داخل الميتوكوندريا — مصانع طاقة الخلية — يمكنه تعديل الفيروسبتوز صعودًا أو هبوطًا، وتُظهر كيف أن حجب هذا المفتاح يمكن أن يحمي البنكرياس في نموذج فأري.
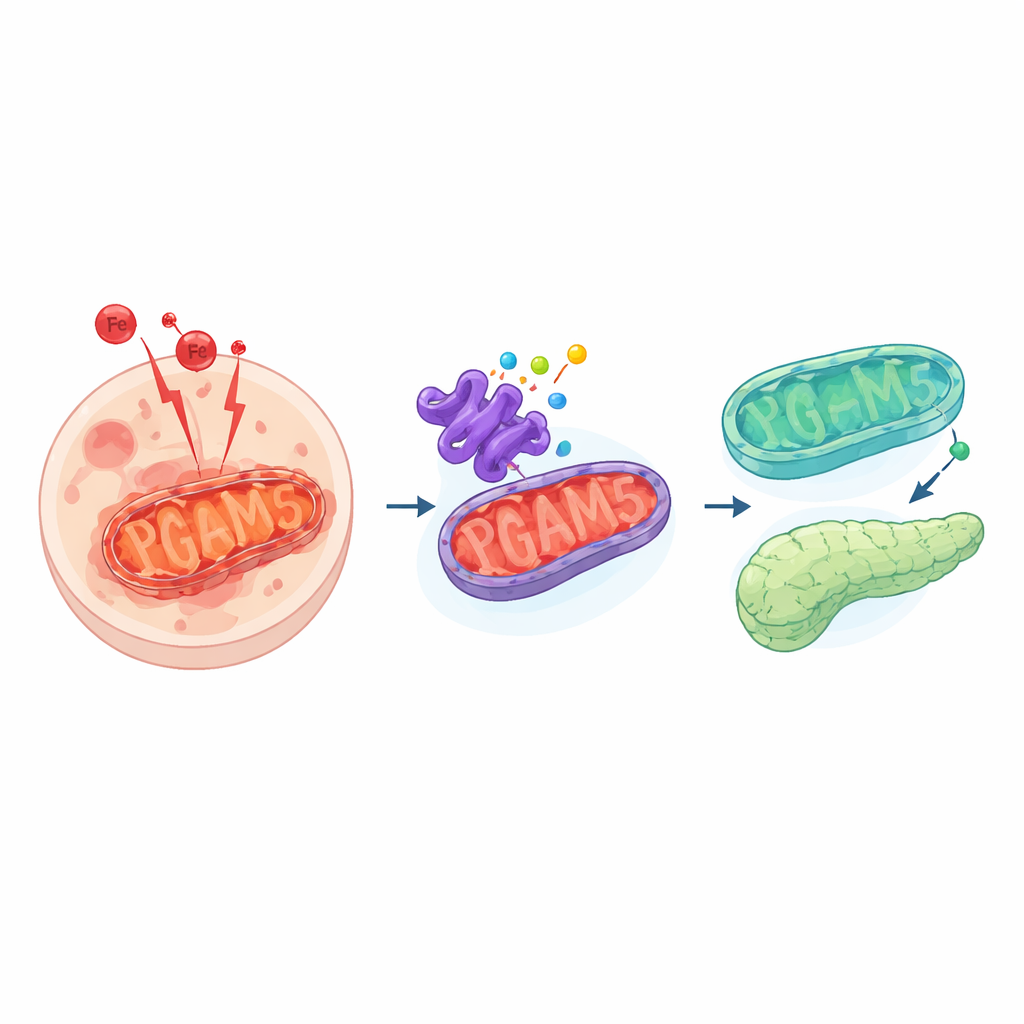
شكل خطير من موت الخلايا
الفسروبتوز يختلف عن أشكال موت الخلايا الأكثر شيوعًا مثل الاستماتة. بدلًا من الدمار المنظم، تمر الخلايا المصابة بالفسروبتوز بعاصفة من التفاعلات المدفوعة بالحديد التي تفسد الدهون الحساسة في أغشيتها. ينتج عن ذلك نواتج سامة وثقوب في الأغشية تؤدي في النهاية إلى موت الخلية. عادةً ما تحافظ الخلايا على هذا تحت السيطرة بأنظمة واقية تزيل هذه الجزيئات التفاعلية. عندما تفشل تلك الأنظمة أو تُغلب، يمكن للفسروبتوز أن ينشر الضرر في الأنسجة، مساهمًا بأمراض تتراوح من السرطان إلى فشل الأعضاء.
مفتاح ميتوكوندري في مرمى البحث
ركز الباحثون على بروتين يسمى PGAM5، الموجود على الوجه الداخلي للميتوكوندريا ويعمل كمحور إشاري. يساعد PGAM5 في التحكم بشكل الميتوكوندريا، والاستجابة للإجهاد، ويؤثر على كيفية تعامل الخلايا مع الأكسدة. وبشكل مفاجئ، عندما قلل الفريق من PGAM5 أو أجبر الخلايا على إنتاج المزيد منه، أصبحت الخلايا أصعب على القتل بالفسروبتوز. قلل كل من التثبيط الكيميائي لـPGAM5 والنقصان الجيني والإفراط في التعبير من تراكم نواتج الدهون الضارة وخفّضوا موت الخلايا الناتج عن دواء محرض للفسروبتوز. كشف هذا أن النظام مضبوط بدقة: كل من القليل جدًا والكثير جدًا من PGAM5 يدفعان الخلايا نحو حالة أكثر حماية.
تشغيل درع داخلي
بالغوص أعمق، اكتشف المؤلفون أن تأثير PGAM5 يسري عبر محور وقائي يشمل لاعبين آخرين: NRF2 وFSP1. NRF2 هو منظم رئيسي عندما يكون نشطًا في النواة يشغل مجموعة واسعة من الدفاعات المضادة للأكسدة. FSP1 هو أحد مدافعيه النصفيّين الذي يساعد على تجدد مضاد أكسدة قابل للذوبان في الدهون، مانعًا تلف الدهون عند غشاء الخلية. عندما تغيّرت مستويات PGAM5، زادت الخلايا كلًّا من رسائل وبروتينات NRF2، وانتقل NRF2 بسهولة أكبر من السيتوبلازم إلى النواة. هناك، زيّد إنتاج FSP1. إسكات FSP1 أو NRF2 أزال الحماية وأعاد الحساسية للفسروبتوز، مما يظهر أن سلسلة PGAM5–NRF2–FSP1 أساسية للمناعة المرصودة.
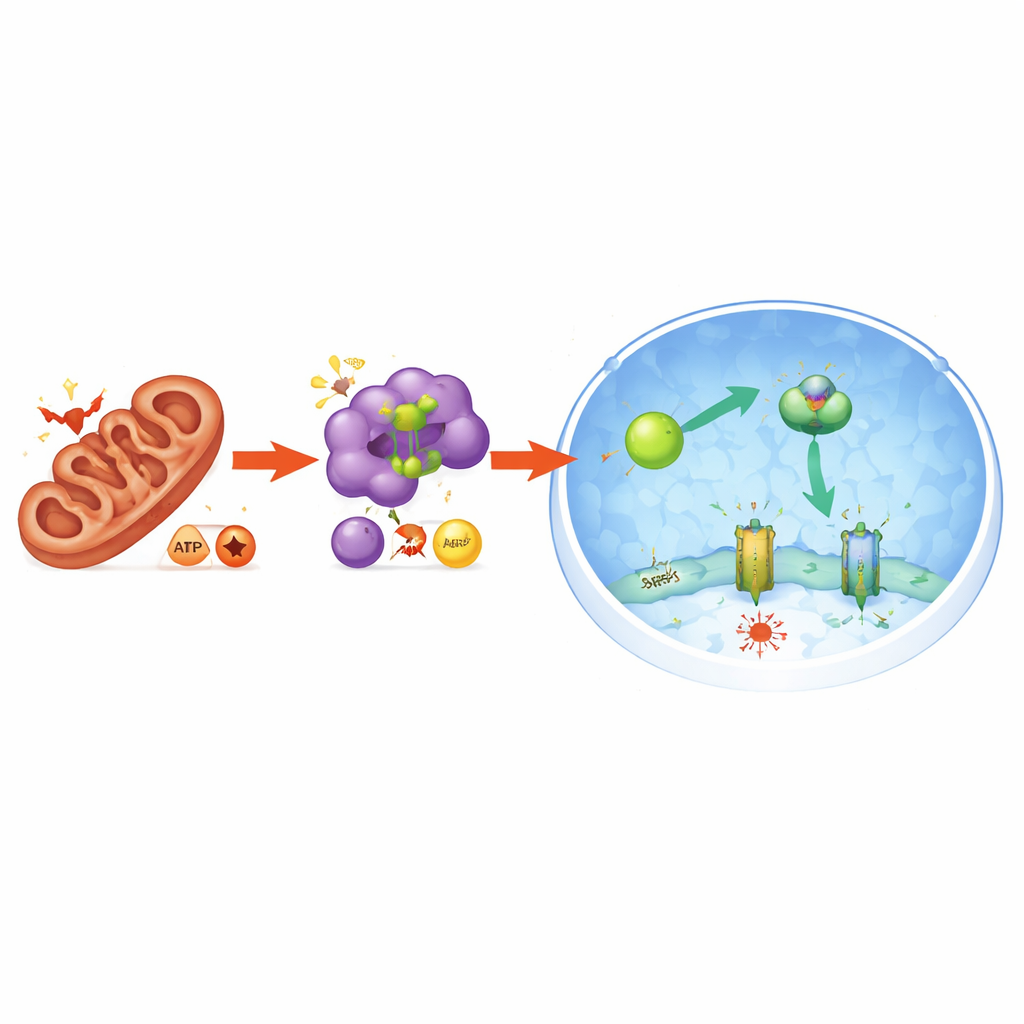
إجهاد الطاقة كمرسال مخفي
كشفت الدراسة أيضًا كيف تُترجم ضغوط الميتوكوندريا إلى هذا الاستجابة الوقائية. تعطيل PGAM5 أخل بتوازن الميتوكوندريا وحوّل عملة الطاقة في الخلية: ارتفعت نسبة الجزيئات منخفضة الطاقة (AMP وADP) إلى ATP عالي الطاقة، مما أشار إلى إجهاد طاقي. هذا بدوره فعّل إنزيم حساس للطاقة وهو AMPK. عدّل AMPK المنشط NRF2 بشكل مباشر بطريقة شجعت دخوله إلى النواة، مما زاد إنتاج FSP1. عندما أزيل AMPK من النظام، لم يعد NRF2 يتراكم في النواة، وانخفضت مستويات FSP1، وعادت الخلايا لتنهار بالفسروبتوز. هكذا يربط PGAM5 حالة الميتوكوندريا برد فعل أوسع للطاقة والمضادات الأكسدة الذي يقي الخلايا من الموت المدفوع بالحديد.
حماية البنكرياس في حيوانات حية
لاختبار ما إذا كانت هذه الآلية مهمة على مستوى عضو كامل، لجأ العلماء إلى نموذج فأري لالتهاب البنكرياس الحاد يُحفَز بجرعات عالية من الحمض الأميني أرجينين. في هذا النموذج، يظهر البنكرياس أضرارًا واسعة، وتعلو مستويات إنزيمات دموية تشير إلى إصابة الأنسجة، ويطرأ ارتفاع مؤشرات الجزيئات الالتهابية. كما ارتفعت علامات بيروكسدة الدهون — وهي بصمة للفسروبتوز — بشكل حاد في البنكرياس. علاج الفئران بمركب يثبط PGAM5 خفف هذه الأعراض: هبطت مؤشرات الضرر في الدم، وبدت أنسجة البنكرياس أكثر صحة تحت المجهر، وتراجعت الإشارات الالتهابية. في الوقت نفسه، انخفضت علامات الفسروبتوز بينما ازدادت نشاط AMPK ومستويات NRF2 وFSP1 في البنكرياس، موافقةً المسار الوقائي المرصود في زراعة الخلايا.
ما الذي يعنيه هذا للعلاجات المستقبلية
مجملاً، تحدد هذه الدراسة PGAM5 كنقطة تحكم مركزية تربط إجهاد الميتوكوندريا، وحالة طاقة الخلية، وبرنامجًا مضادًا قويًا للأكسدة يوقف الفسروبتوز. عبر تقليل نشاط PGAM5، تنشط الخلايا AMPK وNRF2، وتزيد FSP1، وتصبح أكثر مقاومة لتلف الدهون المدفوع بالحديد. في الفئران، تُخفف هذه الاستراتيجية إصابة البنكرياس في التهاب البنكرياس الحاد. للقراء غير المتخصصين، الرسالة هي أن الباحثين وجدوا "قاطع دائرة" داخلي جديد يمكنه منع شكل مدمر من موت الخلايا. ومع بقاء الكثير ليُنجز قبل الاستخدام السريري، قد يفتح استهداف PGAM5 أو شركائه السفليين طرقًا جديدة لعلاج حالات يُشكل فيها الفسروبتوز وفشل الميتوكوندريا دورًا ضارًا.
الاستشهاد: Ma, S., Qin, J., Luan, J. et al. Targeting mitochondrial phosphatase PGAM5 alleviates ferroptosis and acute pancreatitis by upregulating NRF2-mediated FSP1 expression. Cell Death Dis 17, 252 (2026). https://doi.org/10.1038/s41419-026-08484-9
الكلمات المفتاحية: الفسروبتوز, الميتوكوندريا, التهاب البنكرياس الحاد, الإجهاد التأكسدي, موت الخلايا