Clear Sky Science · ar
استهداف مُركّب تخليق الأحماض الدهنية يكبح تطور الأورام في الورم الغشائي الجنبي الناجم عن نقص NF2/CDKN2A
لماذا يهم هذا الأشخاص المعرضين للأسبستوس
الورم الغشائي الجنبي هو سرطان نادر لكنه في الغالب قاتل ينمو على الغشاء المحيط بالرئتين، وغالبًا بعد تعرض للأسبستوس قبل عقود. عند تشخيصه، يكون من الصعب علاجه وعادة ما يقاوم العلاج الكيميائي التقليدي. تستكشف هذه الدراسة زاوية مختلفة: بدلاً من مهاجمة الورم بأدوية تقليدية، حاول الباحثون تجويع خلايا السرطان عن طريق قطع مصدر أساسي لمكونات البناء والطاقة لديها، مما يشير إلى علاج أكثر تخصيصًا لشريحة جينية كبيرة من حالات الميسوثيليوما.
كيف تستغل خلايا الورم آلية إنتاج الدهون
تزيد العديد من الأورام نشاط إنزيم يُسمى مُركّب تخليق الأحماض الدهنية، الذي يركب الأحماض الدهنية طويلة السلسلة التي تستخدمها الخلايا لبناء الأغشية وتخزين الطاقة والتحكم في الإشارات. ركز الفريق على خلايا الميسوثيليوما التي تفتقر إلى جينين وقائيين من الورم، NF2 وCDKN2A (المعروف أيضًا باسم p16)، وهي تغيّرات شائعة في هذا المرض. من خلال فحص 364 مركبًا مضادًا للسرطان، وجدوا أن جزيئًا واحدًا، سيرولينين، الذي يثبط مُركّب تخليق الأحماض الدهنية، كان فعالًا بشكل خاص في إبطاء نمو خلايا الميسوثيليوما الناقصة NF2/p16. بالمقابل، كانت أدوية أخرى، بما في ذلك مُثبط آخر للمركب يُدعى C75 والعوامل القياسية سيزبلاتين وبيمتركسيد، أقل فعالية بكثير عند جرعات مماثلة.
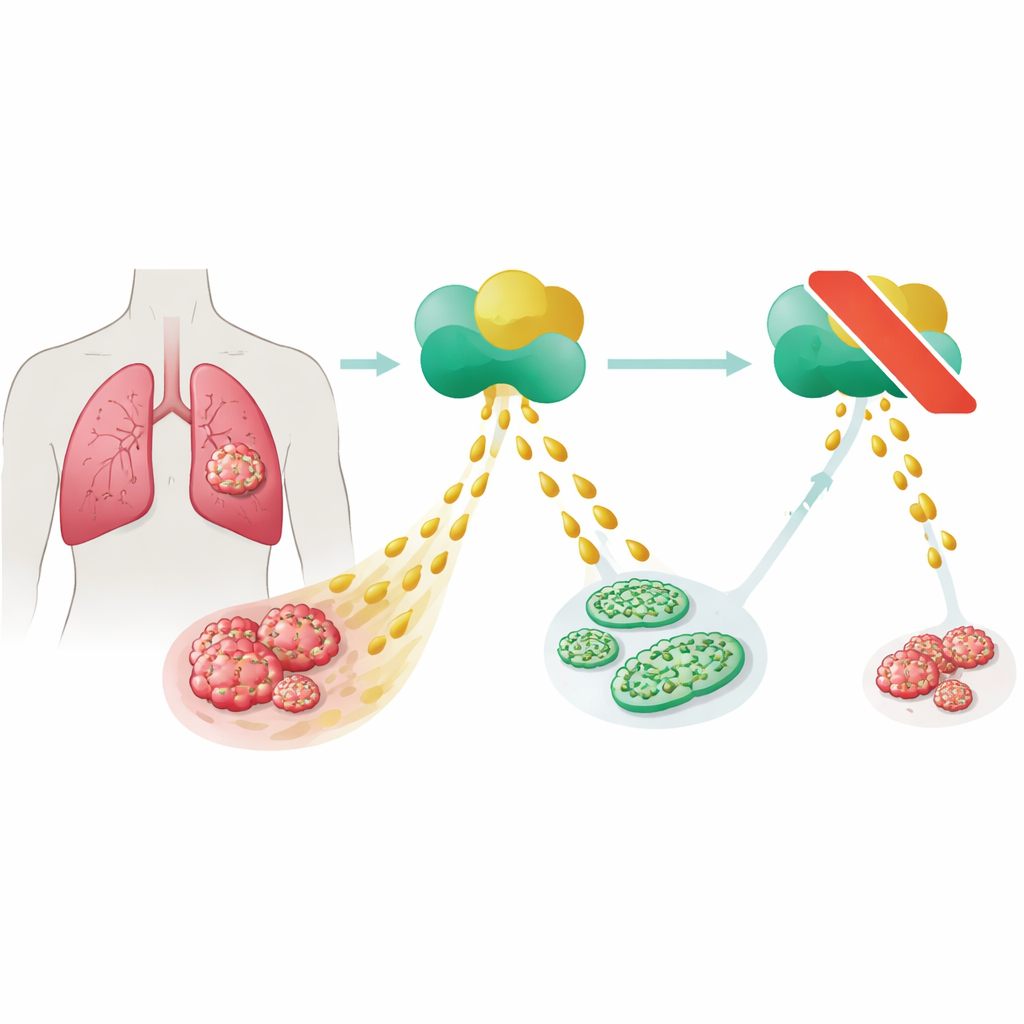
ربط إنزيم تصنيع الدهون بأورام المرضى
لمعرفة ما إذا كان هذا الإنزيم مهمًا بالفعل في المرض البشري، فحص الباحثون عينات نسيجية من 45 شخصًا مصابًا بالورم الغشائي الجنبي وقارنوها بالغشاء الجنبي الطبيعي. وجدوا بروتين مُركّب تخليق الأحماض الدهنية في كل ورم فقد كلا من NF2 وp16، لكن في نحو ثلث الأورام فقط عندما كانت تلك الجينات سليمة، ولا يوجد إطلاقًا في النسيج الطبيعي. وعند الرجوع إلى قاعدة بيانات عامة كبيرة للسرطان، كان المرضى الذين أظهرت أورامهم مستويات أعلى من جين مُركّب تخليق الأحماض الدهنية لديهم بقاء إجمالي أقصر من أولئك ذوي المستويات المنخفضة. تشير هذه النتائج مجتمعة إلى أن الإنزيم ليس مجرد عنصر ثانوي بل مرتبط بقوة بسلوك ورمي عدواني في هذا النوع من السرطان.
اختبار دواء موجه في الحيوانات
كانت الخطوة التالية معرفة ما إذا كان حظر مُركّب تخليق الأحماض الدهنية يمكن أن يقيِّد الأورام في كائن حي. زرع الفريق خلايا ميسوثيليوما بشرية ناقصة NF2/p16 تحت جلد فئران ذات مناعة منخفضة وعالجوها إما بسيرولينين أو بمحلول ملحي غير ضار. أبطأ سيرولينين نمو الأورام بشكل ملحوظ دون إحداث فقدان في الوزن أو أضرار مرئية في القلب أو الكبد أو الكليتين. كما ظلت اختبارات الدم لوظائف الكبد والكلى والكهارل والدهون والسكر ضمن النطاقات الطبيعية. تشير هذه النتائج إلى أن سيرولينين، على الأقل في هذا الإعداد التجريبي، يمكن أن يحد من نمو الورم مع مظهر أمان معقول على المدى القصير.
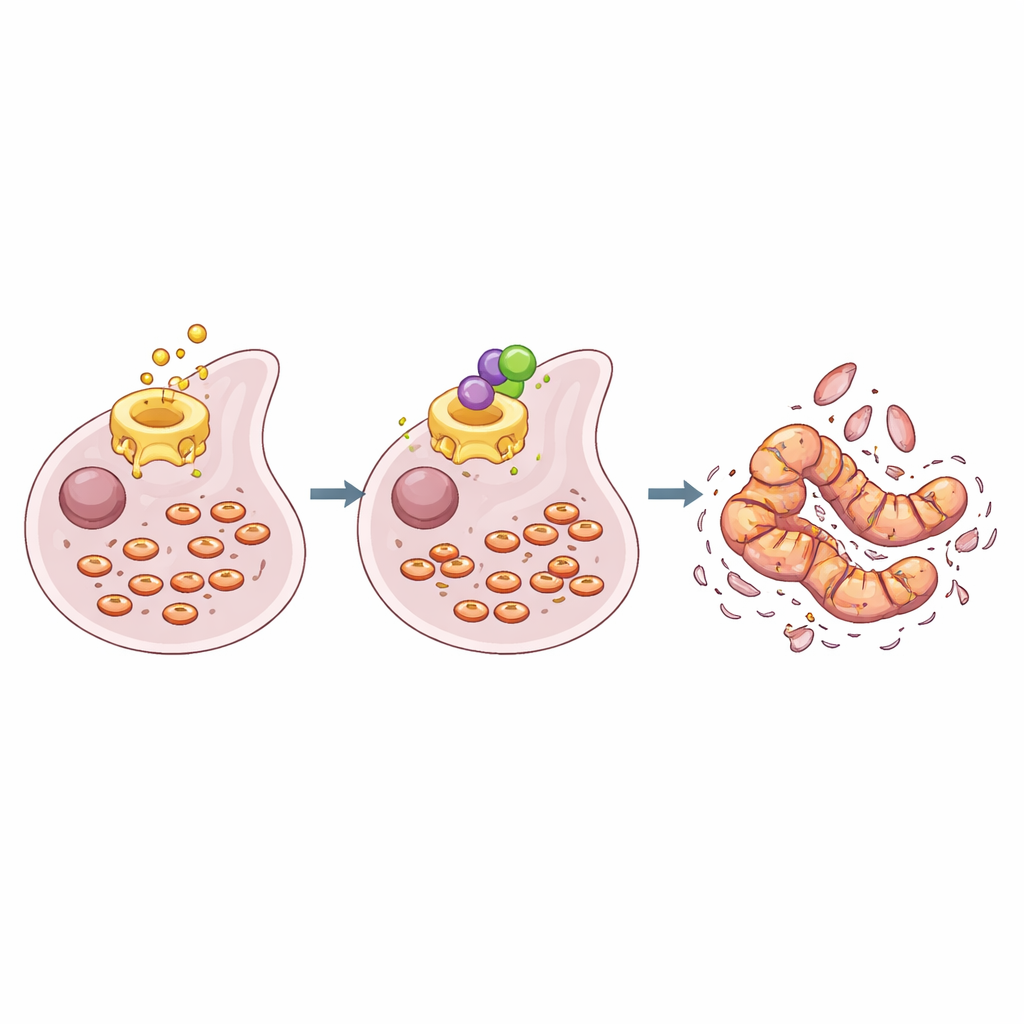
كيف يوجه إعادة توصيل "المصانع الصغيرة" الخلوية خلايا السرطان نحو الموت
تعتمد خلايا السرطان اعتمادًا كبيرًا على الميتوكوندريا، البُنى الصغيرة التي تولد معظم طاقة الخلية. تنقسم هذه الميتوكوندريا وتندمج باستمرار، ويتغير هذا التوازن في المرض. في خلايا الميسوثيليوما الناقصة NF2/p16، دعم نشاط مُركّب تخليق الأحماض الدهنية نمطًا من الميتوكوندريا الصغيرة والمجزأة والإشارات النشطة التي تعزز بقاء الخلية. عندما أضاف الباحثون سيرولينين، اندمجت الميتوكوندريا في هذه الخلايا لتشكل شبكات طويلة وأسطوانية وانخفض نشاط DRP1، البروتين الذي يقود تشظي الميتوكوندريا. كما كبلت الإشارات عبر مسار نمو رئيسي (PI3K–AKT–mTOR) ونظام تحكم بالنمو معروف باسم Hippo–YAP. أظهرت التحليلات الخلوية وبروتينية أن المزيد من الخلايا المعالجة دخلت في الموت المبرمج، مع مستويات متزايدة من PARP المقسّم والكاسبيز-3.
دليل وراثي على أن مُركّب تخليق الأحماض الدهنية موضع ضعف
لتأكيد أن هذه التأثيرات ناتجة بالفعل عن حظر مُركّب تخليق الأحماض الدهنية وليس عن فعل ثانوي لسيرولينين، استخدم الفريق تحرير الجينات CRISPR لإزالة جين مُركّب تخليق الأحماض الدهنية نفسه في خلايا صِفْحِية ناقصة NF2/p16، خلفين "خلايا محذوفة ثلاثية". نمت هذه الخلايا المعدّلة بشكل أبطأ، وكانت لديها ميتوكوندريا أكثر اندماجًا واستطالة، وأظهرت انخفاضًا في مستويات DRP1 ولكن زيادة في بروتينات تعزز اندماج الميتوكوندريا. كما أنتجت المزيد من أنواع الأكسجين التفاعلية، علامة على إجهاد الميتوكوندريا، وظهرت عليها المزيد من مؤشرات الاستماتة. اقترحت تجارب إضافية أنه بدون مُركّب تخليق الأحماض الدهنية، يصبح DRP1 أكثر وسمًا باليبوبتين ويتم تحلّله، مما يميل بالتالي التوازن نحو اندماج الميتوكوندريا وموت الخلية.
ماذا قد يعني هذا للعلاج المستقبلي
بشكل إجمالي، تُظهر الدراسة أن خلايا الميسوثيليوما المفقودة NF2 وp16 تعتمد على مُركّب تخليق الأحماض الدهنية للحفاظ على مصانع الطاقة في حالة تدعم النمو ولإدامة إشارات بقاء قوية. حظر هذا الإنزيم بسيرولينين يضعف هذه الأورام انتقائيًا في الخلايا وفي عينات الأنسجة البشرية وفي الفئران، مع حفاظ ظاهر على الأنسجة الطبيعية على المدى القصير. بالنسبة للمرضى، تشير هذه النتائج إلى أن الأدوية المستهدفة لمُركّب تخليق الأحماض الدهنية، لا سيما في الأورام التي يُختبر فيها فقدان NF2 وCDKN2A، قد تصبح جزءًا من استراتيجية طبية دقيقة تستفيد من اعتماد استقلابي محدد لسرطانهم.
الاستشهاد: Karnan, S., Ota, A., Hasan, M.N. et al. Targeting fatty acid synthase suppresses tumor development in NF2/CDKN2A-deficient pleural mesothelioma. Cell Death Dis 17, 287 (2026). https://doi.org/10.1038/s41419-026-08481-y
الكلمات المفتاحية: الورم الغشائي الجنبي, مُركّب تخليق الأحماض الدهنية, سيرولينين, ديناميكا الميتوكوندريا, طب دقيق/أورام موجهة