Clear Sky Science · ar
يوربي3A يُحفّز يوبيكويتنة mH2A1 وينشّط نسخ TERT لتعزيز مقاومة الشيخوخة في سرطان البنكرياس
لماذا تهم هذه الدراسة المرضى
يُعد سرطان البنكرياس من أكثر الأورام فتكا، جزئياً لأن خلايا الورم بارعة بشكل غير عادي في التحايل على مكابح الشيخوخة الطبيعية للجسم. تكشف هذه الدراسة عن «دائرة تخريب» جزيئية مخفية تساعد خلايا سرطان البنكرياس على البقاء شابة، ومواصلة الانقسام، والمقاومة للعلاج. ومن خلال فهم هذه الدائرة، يشير الباحثون إلى طريقة جديدة لدفع هذه الخلايا نحو الشيخوخة ثم إزالتها انتقائياً، ما يفتح الباب لعلاجات مركبة وأكثر ذكاءً.
الشيخوخة كمكبح طبيعي للأورام
تحمل كل الخلايا ساعة داخلية تجعلها في نهاية المطاف تتوقف عن الانقسام، وهي عملية تُعرف بالشيخوخة الخلوية. في الآفات الباكرة في البنكرياس، يمكن أن تبطئ هذه الساعة تطور الورم بوضع الخلايا ما قبل السرطانية في حالة تقاعد دائم. العديد من علاجات السرطان تعمل جزئياً عن طريق إجبار الخلايا الورمية على الدخول في هذه الحالة المشابهة للشيخوخة. ومع ذلك، إذا لم تُزل هذه الخلايا المسنة، فيمكن أن تغذي الالتهاب وتساعد الورم على العودة. أدى ذلك إلى فكرة علاجية جديدة: أولاً دفع الخلايا السرطانية إلى الشيخوخة، ثم القضاء على تلك الخلايا المسنة بواسطة أدوية "سنوليتك" سامة لها بشكل خاص.
إنزيم مروّج للسرطان تحت الأضواء
للعثور على الجينات التي تساعد خلايا سرطان البنكرياس على تحدي الشيخوخة، استخرج الفريق بيانات كبيرة للمرضى ثم حقق في نتائجهم في عينات ورمية وسلاسل خلوية. ركزوا على بروتين يُدعى UBE3A، وهو إنزيم يعلّم البروتينات الأخرى علامة التدمير. كانت مستويات UBE3A أعلى بكثير في أورام البنكرياس مقارنة بنسيج مجاور سليم، ويميل المرضى ذوو المستويات الأعلى من UBE3A إلى امتلاك أورام أكبر وأكثر تقدماً وبقاء أسوأ. في خلايا مزروعة مخبرياً، تسريع UBE3A عزز النمو، وخفّض مؤشرات الشيخوخة الخلوية الكلاسيكية، وقلّل الإفرازات الالتهابية النموذجية للخلايا المسنة. أما إسكات UBE3A فكان له تأثير معاكس وفي نماذج الفئران خفّض بشكل حاد نمو الورم وانتقاله إلى الكبد. 
كيف تمحو الخلايا السرطانية مكبح الكروماتين
بالغوص أعمق، سأل الباحثون عن الجزيئات التي يؤثر عليها UBE3A. باستخدام فحوصات مطياف الكتلة المتقدمة، وجدوا أن UBE3A يرتبط بنوع خاص من الهستون يُدعى macroH2A1 (mH2A1) ويعلّمه كيميائياً؛ هذا المتغير يساعد على تكثيف الحمض النووي وعادة ما يعمل كمكبح على نشاط الجينات. يربط UBE3A سلسلة من علامات «اهدموني» بـ mH2A1 في موضع محدد، ما يؤدي إلى تكسيره بواسطة آلية التخلص من البروتين في الخلية. في أورام البنكرياس كانت مستويات mH2A1 أقل حيثما كان UBE3A عالياً، واستعادة mH2A1 عكست قدرة UBE3A على منع الشيخوخة ودفع نمو الورم. يكشف هذا عن خطوة رئيسية: تزيح خلايا سرطان البنكرياس علامة كروماتينية واقية عبر استخدام UBE3A للقضاء على mH2A1.
فتح تيلوميراز للحفاظ على الشباب الخلوي
السؤال التالي كان أي الجينات تتحرر عند إزالة mH2A1. بدمج تسلسل RNA وخرائط ربط الحمض النووي، حدّد الفريق جين التيلوميراز TERT كهدف مركزي. يحافظ التيلوميراز على الأغطية الواقية على نهايات الكروموسومات، مما يسمح للخلايا بالاستمرار في الانقسام بدلاً من الدخول في الشيخوخة. تُظهر الدراسة أن mH2A1 عادةً ما يجلس عند منطقة معزِّز داخل جين TERT، حيث يجذب إنزيمًا آخر، EZH2، لوضع علامة كيميائية قمعية على هستونات قريبة. يحافظ هذا المزيج على إخماد TERT ويسمح للتيلوميرات بالانكماش. عندما يدمر UBE3A mH2A1، ينهار المجمع القمعي، وينشط المعزز، ويُشغّل TERT، وتحافظ التيلوميرات، وتكتسب خلايا سرطان البنكرياس مقاومة للشيخوخة. الأشكال الطافرة من UBE3A التي لا تستطيع تعليم البروتينات، أو أشكال طافرة من mH2A1 التي لا يمكن تعليمها، تكسر هذه الدائرة وتستعيد مكبح الشيخوخة.
مزاوجة تحفيز الشيخوخة مع تنظيف سنوليتك
أخيراً، اختبر الباحثون ما إذا كان يمكن استغلال هذا المسار علاجياً. أدى تعطيل UBE3A إلى دفع خلايا سرطان البنكرياس نحو الشيخوخة وزيادة اعتمادها على بروتينات مضادة للموت من عائلة BCL‑2—وهي نقطة ضعف معروفة للخلايا المسنة. ثم جمع الفريق بين تثبيط UBE3A وABT‑263، دواء سنوليتك يستهدف هذه بروتينات البقاء. في الخلايا المزروعة، تسبب المزيج في وفاة مبرمجة لعدد أكبر بكثير من خلايا السرطان مقارنة بأي من العلاجين وحدهما. في نماذج الفئران، تقلصت الأورام ذات UBE3A المنخفض حتى أكثر عندما أُعطي الحيوانات ABT‑263، وانخفضت علامات تكاثر الخلايا داخل الأورام بشكل حاد. 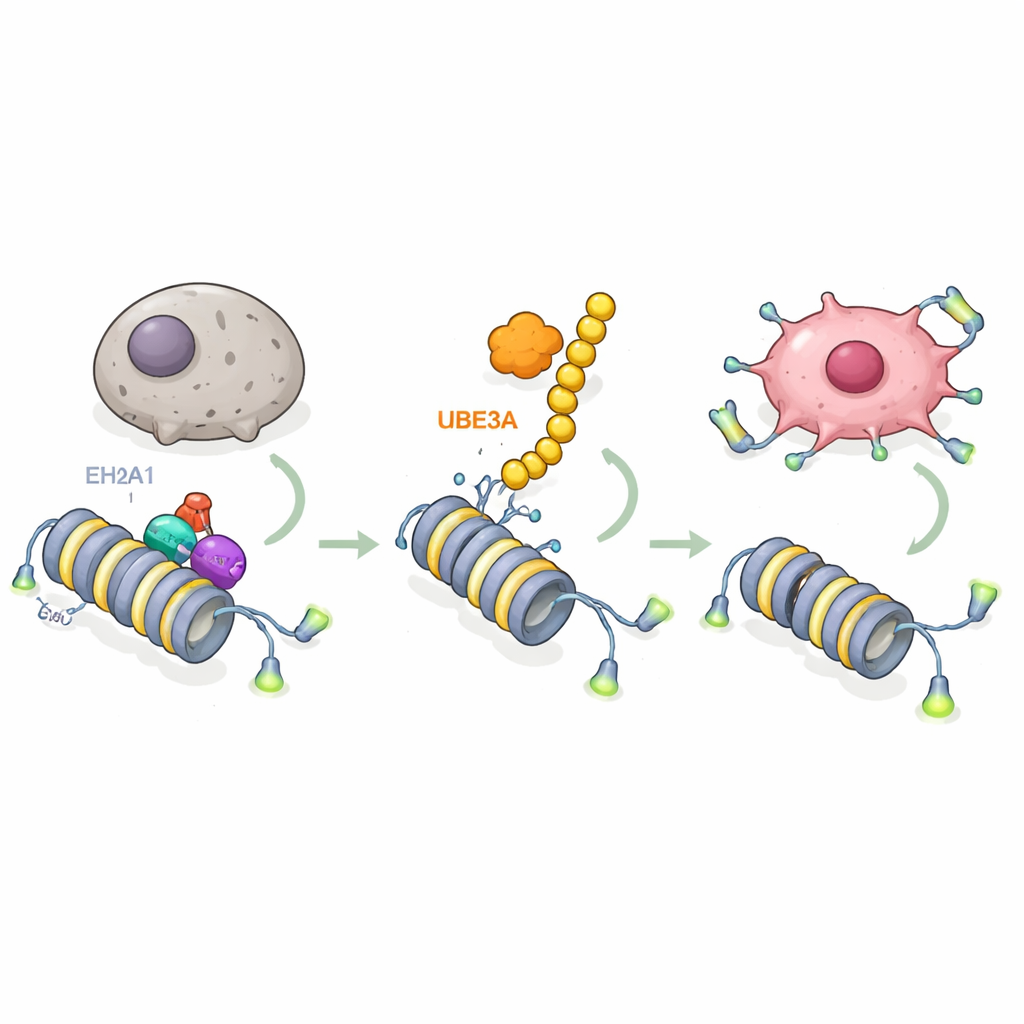
ماذا يعني ذلك للعلاج المستقبلي
تكشف هذه الدراسة سلسلة مفصلة من الأحداث التي تسمح لخلايا سرطان البنكرياس بتجنب الشيخوخة: يدمر UBE3A مكبح الكروماتين mH2A1، مما يرفع القمع عن جين التيلوميراز TERT ويساعد على الحفاظ على التيلوميرات، مُمكناً الخلايا من الاستمرار في الانقسام. باستهداف UBE3A، قد يتمكن الأطباء من إعادة تفعيل برنامج الشيخوخة الطبيعي للخلايا ثم استخدام أدوية سنوليتك مثل ABT‑263 لإزالة هذه الخلايا السرطانية المسنة والموضعَة على نحو انتقائي. وبينما هناك حاجة لمزيد من الدراسات لترجمة هذا الميكانيزم إلى علاجات للمرضى، يقدم محور UBE3A–mH2A1–TERT مقبضاً واعداً لمهاجمة أحد أكثر السرطانات مقاومة للعلاج.
الاستشهاد: Ren, L., Lu, R., Fei, X. et al. UBE3A-mediated mH2A1 Ubiquitination activates TERT transcription to promote senescence resistance in pancreatic cancer. Cell Death Dis 17, 274 (2026). https://doi.org/10.1038/s41419-026-08480-z
الكلمات المفتاحية: سرطان البنكرياس, الشيخوخة الخلوية, تيلوميراز, ليغاز يوبيكويتين, علاج سنوليتك