Clear Sky Science · ar
مثبط صغير لجزيء بروتين GTPase ARF1 يحدّ من نمو وانتشار خلايا سرطان الكبد والقولون
لماذا تهمّ هذه الدراسة
يُعد غُرَيانُ الكبد والقولون من بين الأورام الأكثر فتكاً، والعلاجات الحالية غالباً ما تقلّص الأورام مقابل آثار جانبية قاسية. تستكشف هذه الدراسة نوعاً جديداً من الأدوية لا يقتصر على تسميم الخلايا سريعة الانقسام، بل يدخل إلى داخل الخلايا السرطانية ويفصل «مركز تحكم» بروتيني تعتمد عليه للنمو والانتشار. من خلال استهداف هذا المركز، يسعى المركب التجريبي إلى إبطاء نمو الورم مع الحفاظ على الأنسجة السليمة.
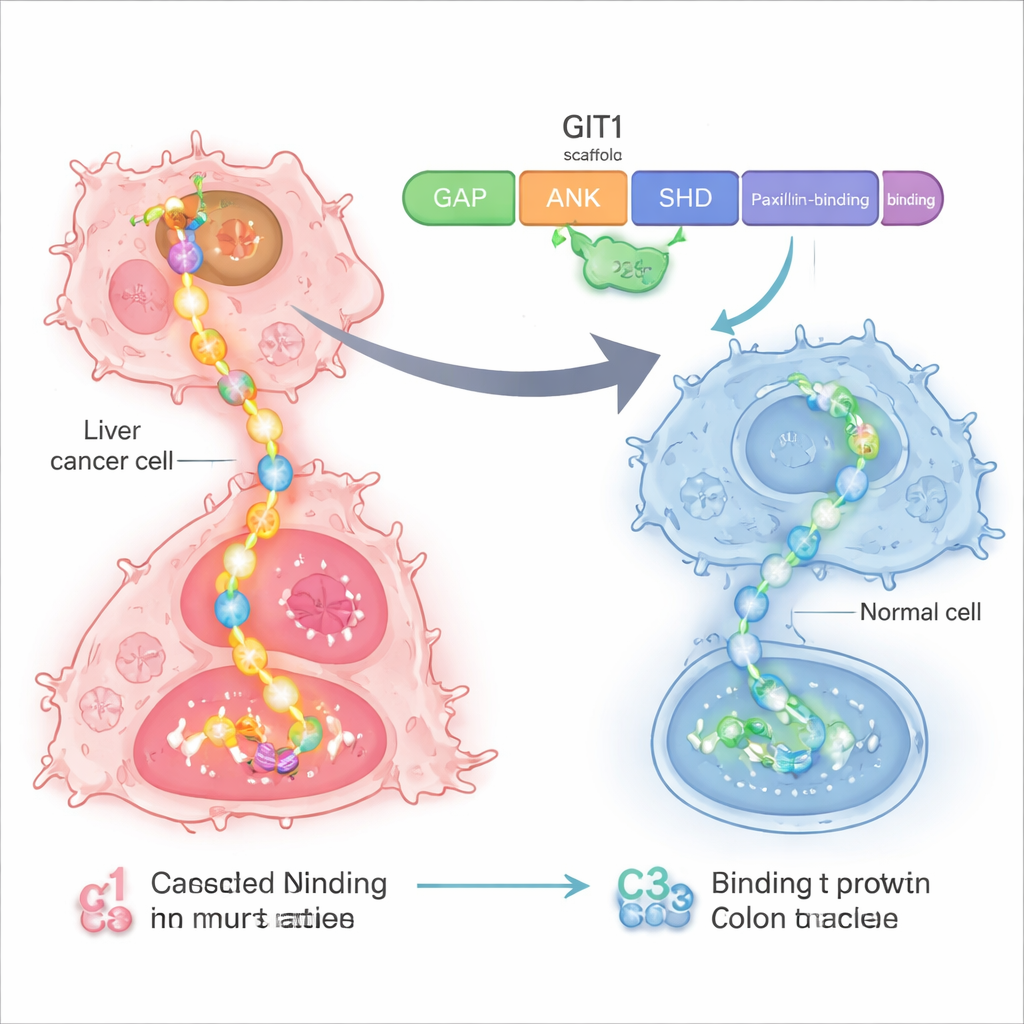
مركز تحكم ضعيف داخل الخلايا السرطانية
ركز الباحثون على بروتين يسمى GIT1، الذي يعمل كهيكل داعم أو وصلة توزيع للطاقة داخل الخلايا. في سرطانات الكبد والقولون، يتم إنتاج GIT1 وشريكه البروتيني MAT2B بكميات زائدة. معاً، يجمعان عدة مكوّنات من مسار نمو رئيسي معروف باسم RAS–RAF–MEK–ERK، وهو سلسلة إشارات تخبر الخلايا بالانقسام والهجرة. أظهرت أعمال سابقة أنه عندما تكون مستويات GIT1 وMAT2B مرتفعة، تنمو أورام الكبد والقولون بشكل أسرع وتنتشر بسهولة أكبر، وعندما تُقلل هذه البروتينات يتباطأ نمو السرطان. هذا جعل من سقالة GIT1–MAT2B هدفاً جذاباً لعلاج أكثر دقة.
تصميم جزيء صغير بلا مخطط ثلاثي الأبعاد
أحدى التحديات الرئيسية كانت عدم توفر البنية البلورية ثلاثية الأبعاد لـGIT1، لذلك لم يتمكن الفريق من «عرض» شكل البروتين بسهولة. بدلاً من ذلك، استخدموا نمذجة حاسوبية للتنبؤ ببنية منطقة من GIT1 مكوّنة من تكرارات الأنكيرين، تقع بالقرب من مواقع ارتباط MAT2B وبروتينات الإشارة الأخرى. ثم أجروا فحصاً افتراضياً لمكتبة كبيرة من الجزيئات الصغيرة مقابل هذا النموذج لرؤية أيّها قد يلتصق بتلك المنطقة. من بين تسعة مرشحين اختُبروا في خلايا، برز جزيء واحد — سُمّي المركب 3 (C3). ارتبط C3 بشكل محدد بـGIT1، لكنه لم يرتبط بأقاربه القريب GIT2، وقلّل نشاط إشارة النمو ERK في خطوط خلايا سرطانية متعددة.
إيقاف انقسام الخلايا السرطانية وانتشارها
عند معالجة خلايا سرطان الكبد والقولون بـC3، تباطأ نموها، وعند جرعات أعلى ماتت خلايا كثيرة، بينما بقيت خلايا الكبد والكلى غير السرطانية متأثرة إلى حد ضئيل. أدى C3 إلى توقّف الخلايا السرطانية عند الحدّ الفاصل بين الطور G2 وطور M من دورة الخلية، وهي نقطة تفتيش تسبق وأثناء الانقسام الخلوي. كما قلّل المركب بشدة من قدرة الخلايا السرطانية على تشكيل مستعمرات والتحرك عبر الصحن — مقياسان مخبريان مرتبطان بإعادة نمو الورم والانتشار. على المستوى الجزيئي، أضعف C3 التفاعلات بين GIT1 وMAT2B وبروتينات الإشارة RAF–MEK–ERK، مما أدّى إلى انخفاض نشاط MEK وERK وانخفاض مستوى دافع دورة الخلية السيكلين D1.
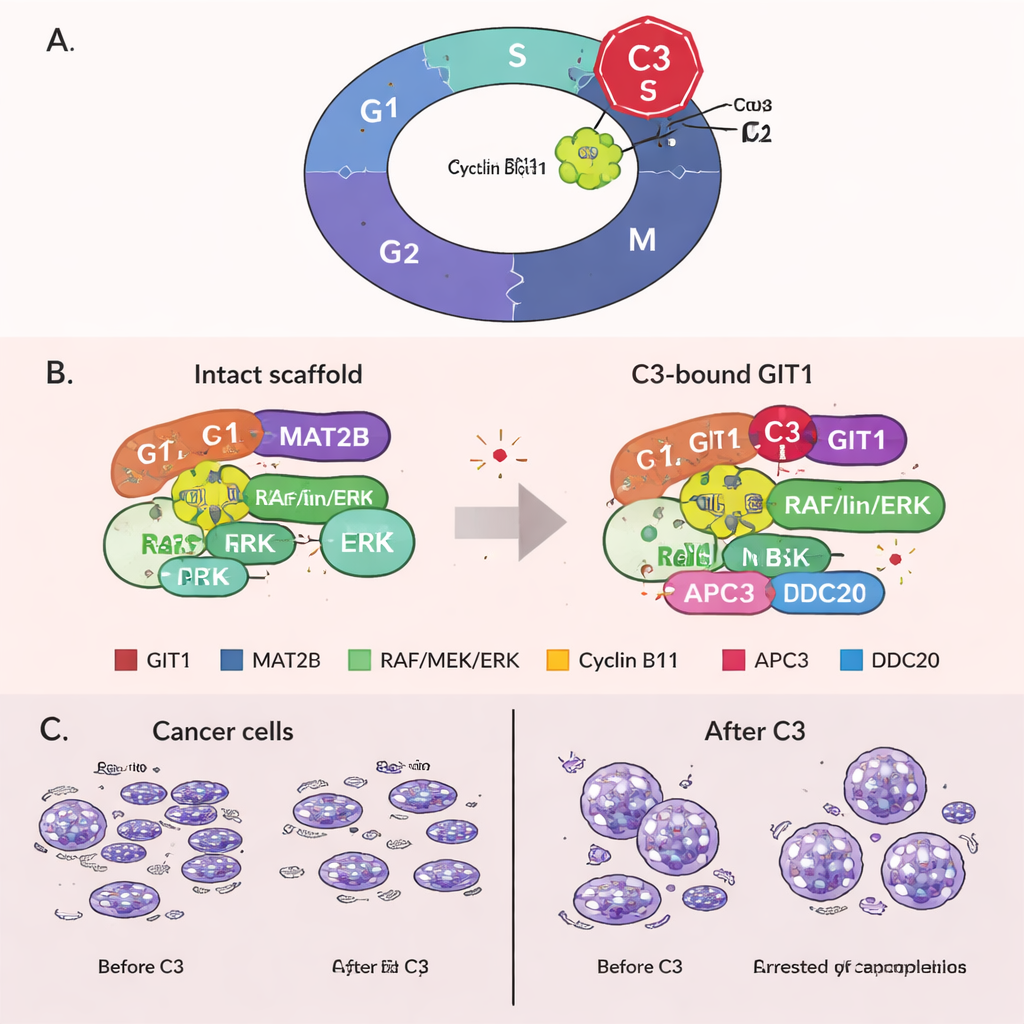
حبس الخلايا في الطور الانقسامي عبر دور جديد مكتشف لـGIT1
بشكل غير متوقع، كشف الفريق عن دور جديد لـGIT1 في المراحل النهائية للانقسام الخلوي. وجدوا أن GIT1 يرتبط بالسيكلين B1، وهو بروتين يساعد على دفع الخلايا إلى الطور الانقسامي، وكذلك بأجزاء من جهاز بروتيني يُدعى مركب تحفيز الطور الانفصالي (APC/C)، الذي عادةً ما يؤشر السيكلين B1 للتدمير لتسهيل خروج الخلية من الطور الانقسامي. عزز علاج C3 الرابط بين GIT1 والسيكلين B1 لكنه أضعف الروابط بين GIT1 والسيكلين B1 ومكونات APC/C. نتيجة لذلك، لم يعد السيكلين B1 يتحلل بكفاءة، وظلت مستوياته مرتفعة، وانحصرت الخلايا في الطور الانقسامي. من المعروف أن هذا التوقّف المطوّل يؤدي إلى موت الخلية، ما يوفّر آلية ثانية يمكن عبرها أن يقتل C3 الخلايا السرطانية. من المهم أن تقليل GIT1 تجريبياً أضعف قدرات C3 على رفع السيكلين B1، ووقف دورة الخلية، وكبح النمو، مما يدل على أن تأثيراته تعتمد بالفعل على GIT1.
نتائج واعدة في نماذج حيوانية
انتقل الباحثون بعد ذلك إلى نماذج فأرية لمعرفة ما إذا كان C3 يعمل في كائنات حية. في فئران ذات جهاز مناعي سليم وزُرع فيها أورام القولون والمستقيم، أدت حقن C3 مباشرة في الأورام إلى إبطاء نموها بشكل كبير من دون سمّية واضحة للأعضاء الرئيسية. في نموذجين إضافيين — خلايا سرطان قولون بشرية تنمو في أكباد فئران ذات جهاز مناعي ناقص، وخلايا سرطان قولون فئارية انتشرت إلى الكبد في فئران ذات جهاز مناعي سليم — قلّل C3 المعطى عن طريق الحقن داخل الصفاق من عبء الورم وعلامات الانتشار. أشارت فحوصات الدم وفحوصات الأنسجة إلى تحمل جيد للعلاجات، وأظهرت دراسات الحرائك الدوائية أن مستويات الدواء في الدم ظلت مرتفعة بما يكفي لعدة ساعات بعد الجرعة.
ما الذي قد يعنيه هذا لعلاجات السرطان المستقبلية
لغير المتخصص، الرسالة الأساسية هي أن الباحثين وجدوا طريقة لمهاجمة السرطان ليست عبر استهداف إنزيم واحد مطفّر، بل عبر تعطيل تجمّع متعدد البروتينات تعتمد عليه الخلايا السرطانية لكلٍ من إشارات النمو والانقسام السليم. جزيئهم الصغير C3 يرتبط بشكل محدد بـGIT1، ويعيد تشكيل شبكة شركائه، ويخفض مسار نمو رئيسي، ويحبس الخلايا السرطانية في ازدحام قاتل أثناء الطور الانقسامي. بينما لا يزال C3 أداة تجريبية وليس دواءً جاهزاً للمرضى، تُظهر هذه العملة أن استهداف بروتينات السقالة مثل GIT1 قد يفتح مساراً جديداً لعلاج سرطانات الكبد والقولون بدقة أكبر وربما بآثار جانبية أقل.
الاستشهاد: Peng, H., Chhimwal, J., Fan, W. et al. A small molecule inhibitor of ARF GTPase protein 1 limits liver and colon cancer cell growth and metastasis. Cell Death Dis 17, 238 (2026). https://doi.org/10.1038/s41419-026-08477-8
الكلمات المفتاحية: سرطان الكبد, سرطان القولون, علاج موجه, توقف دورة الخلية, بروتين هيكلي (سقالة)