Clear Sky Science · ar
متغيرات فقدان الوظيفة في HPDL تضر تطور القشرة البشرية عبر تغييرات في وظيفة الميتوكوندريا
لماذا تهم محركات الخلايا الصغيرة أدمغة النمو
يفكر معظم الناس في الجينات والتوصيلات عندما يتصورون كيف يتطور الدماغ. تُظهر هذه الدراسة أن عاملاً آخر، غالبًا ما يُهمل — المحطات الصغيرة للطاقة داخل خلايانا المسماة الميتوكوندريا — يمكن أن يشكل أيضًا كيفية تشكيل أدمغتنا. من خلال دراسة اضطرابات الحركة الطفولية النادرة المرتبطة بجين اسمه HPDL، يكشف المؤلفون كيف أن خلل إنتاج الطاقة يمكن أن يصغر القشرة النامية، وهي منطقة الدماغ الحاسمة للحركة والتفكير والسلوك.
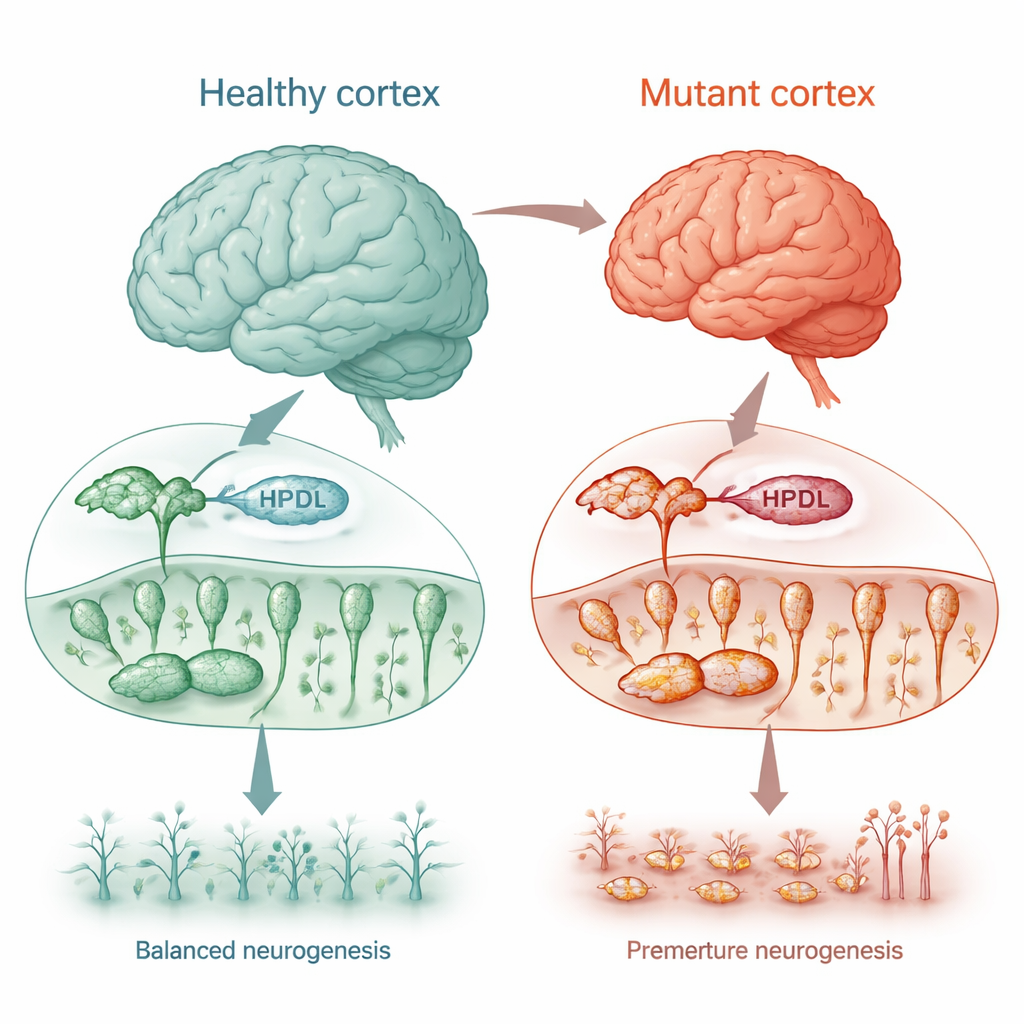
اضطراب حركة نادر نافذة على نمو الدماغ
يعاني بعض الأطفال الذين لديهم تغيرات في جين HPDL من الشلل الرخو الوراثي الباسق، وهو حالة تسبب تيبّسًا وضعفًا في الساقين، إلى جانب نوبات، وتأخرًا في النمو، وفي الحالات الشديدة صغرًا في حجم الدماغ عن المعدل الطبيعي (صغر الرأس). بالرغم من أن بروتين HPDL كان معروفًا بتواجده في الميتوكوندريا، لم تكن مهمته الدقيقة — ولماذا يسبب فقدانه ضررًا للدماغ — واضحة. استخدم الباحثون عدة نماذج خلوية بشرية، بما في ذلك خلايا سرطانية شبيهة بالعصب وخلايا دماغية نمت من عينات جلد مرضى، لاختبار ما إذا كان HPDL ضروريًا للتطور الطبيعي للدماغ وصحة الميتوكوندريا.
ماذا يحدث عندما يُطفأ HPDL
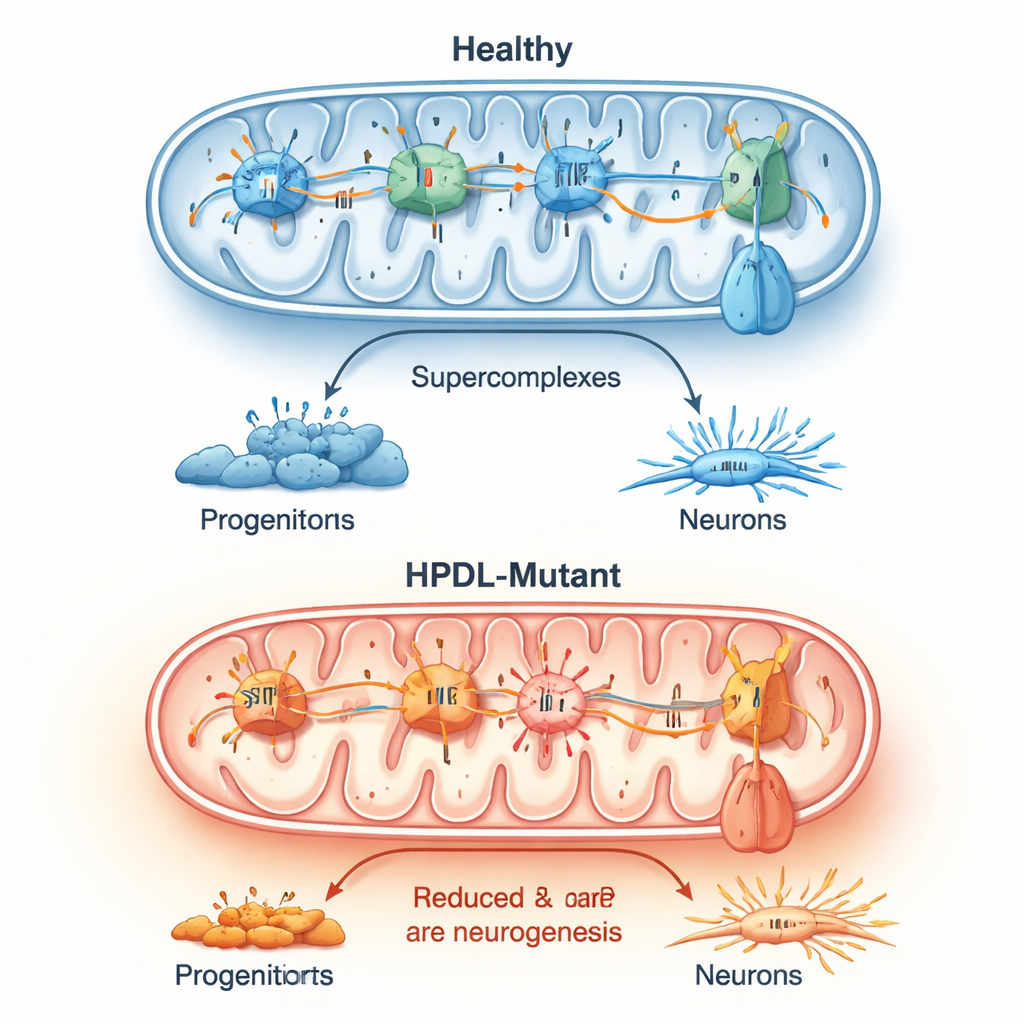
أولاً، أوقف الفريق عمل HPDL في خط خلوي بشري من الورم العصبي باستخدام تعديل الجينات بتقنية CRISPR. من دون HPDL، فقدت هذه الخلايا البروتين بطوله الكامل وأظهرت مشاكل واضحة في الميتوكوندريا. تَفَكَّكت التجمعات الكبيرة لبروتينات سلسلة التنفس التي تعمل عادة معًا لتوليد الطاقة، وتراجعت مكونات أساسية مشاركة في استخدام الأكسجين. حرقَت الخلايا كمية أقل من الأكسجين، وأنتجت تنفّسًا مرتبطًا بالطاقة أقل، وولّدت المزيد من الأنواع التفاعلية للأكسجين — منتجات فرعية ضارة تُسمى غالبًا «الإجهاد التأكسدي». ومع ذلك، لم ينخفض العدد الإجمالي للميتوكوندريا، وكانت مستويات الإنزيم المساعد Q10، الجزيء الحيوي لنقل الطاقة، أعلى في الواقع، ما يشير إلى عيب نوعي — لا مجرد كمي — في وظيفة الميتوكوندريا.
نسيج دماغي في طبق يكشف إفراطًا مبكرًا في إنتاج الخلايا العصبية
لمعرفة كيف يؤثر فقدان HPDL على التطور الدماغي البشري الحقيقي، أعاد الباحثون برمجة خلايا جلد من أربعة أطفال متأثرين إلى خلايا جذعية محرضة متعددة القدرات ثم حثّوها على تكوين خلايا قشرية ثلاثية الأبعاد و"دماغات مصغرة" (أورغانويد). في وقت مبكر من التطور، في مرحلة كان من المفترض أن تظل غالبية الخلايا فيها قابلة للانقسام كخلايا سلف عصبية، احتوت الزرعات المتحورة في HPDL بالفعل على خلايا عصبية أكثر نضجًا وعددًا أقل من الخلايا السلفية. دعمت ملفات نشاط الجينات هذا: تم تشغيل المسارات التي تحفز تشكيل الخلايا العصبية مبكرًا جدًا، بينما خفّضت المسارات التي تحافظ على الخلايا في حالة انقسام. في الأورغانويدات، أدت هذه التحوّل المبكر من اللبنات إلى خلايا عصبية ناضجة إلى هياكل شبيهة بالدماغ أصغر بكثير، مما يعكس صغر الرأس المرصود في أخطر الحالات لدى الأطفال المصابين.
محطات طاقة معطلة وخلايا متوترة
أظهر فحص أدق أن خلايا الدماغ المتحورة في HPDL كان لديها فاعلية ضعيفة في عملية الفسفرة التأكسدية — وهي الطريقة الرئيسية التي تُنتج بها الميتوكوندريا الطاقة. كشفت تلوينات إنزيمية عن نشاط أضعف لمركب ميتوكوندري رئيسي، بينما أظهرت مقاييس أخرى تغيرًا في الشحنة الكهربائية عبر غشاء الميتوكوندريا. في العديد من الخلايا المتحورة، بدا أن إنزيمًا حاسمًا يصنع عادةً ATP يعمل بالعكس لدعم شحنة الغشاء هذه، وهو علامة على ضائقة أيضية عميقة. عبر خطوط مرضى متعددة، كانت الأنواع التفاعلية للأكسجين مرتفعة باستمرار، وكانت التجمعات الكبيرة لعوامل سلسلة التنفس أقل تشكيلًا بشكل سليم. تابعت هذه التغيرات الميتوكوندرية عن كثب توقيت ودرجة الإسراع في إنتاج الخلايا العصبية.
اختبار طرق لتخفيف الإجهاد
بما أن الإجهاد التأكسدي واضطراب كيمياء الإنزيم المساعد Q10 بدا مركزيًا، اختبر الفريق ما إذا كانت علاجات تستهدف هذه المشاكل قد تبطئ التسرع نحو تكوين الخلايا العصبية. عرّضوا الزرعات القشرية المبكرة لمُكَوِّنين مضادين للأكسدة ولـ4-هيدروكسي بنزوات، جزيء صغير مرتبط ببناء الإنزيم المساعد Q10. في عدة خطوط مشتقة من مرضى، خفّضت هذه المركبات جزئيًا التكوّن العصبي المبكر، لكن الاستجابة اعتمدت على طفرة HPDL الدقيقة. استجابت بعض الخطوط في المقام الأول للمضادات الأكسدة، وأخرى للمقدمة الحيوية لإنزيم المساعد Q10، ولم تستجب إحداها على الإطلاق. هذه النمطية المرتبطة بالطفرات تشير إلى أن استراتيجيات علاج مخصصة قد تكون ضرورية لاضطرابات متعلقة بـHPDL.
ماذا يعني هذا للأطفال والعلاجات المستقبلية
بعبارات بسيطة، تُظهر هذه الدراسة أن HPDL يعمل كحارس لبنات بناء الدماغ خلال التطور المبكر. عندما يفشل HPDL، تصبح الميتوكوندريا غير فعالة ومجهدة بشكل مفرط، مما يدفع الخلايا السلفية لأن تتحول إلى خلايا عصبية مبكرًا جدًا. تُستنزف مجموعة الخلايا القابلة للانقسام، ولا تستطيع القشرة الوصول إلى حجمها الكامل، وتتغير أنماط التوصيل، مساهِمةً في مشاكل الحركة وأعراض أخرى. الانتعاش الجزئي الذي لوحظ بالمضادات الأكسدة ومركبات مرتبطة بالإنزيم المساعد Q10 يلمح إلى أن تعديل توازن الطاقة الخلوية والإجهاد التأكسدي قد يساعد يومًا أطفالًا يعانون طفرات في HPDL، وربما آخرين مصابين بأشكال ميتوكوندرية من أمراض الدماغ.
الاستشهاد: Baggiani, M., Desbats, M.A., Naef, V. et al. Loss of function variants in HPDL impair human cortical development via alterations of mitochondrial function. Cell Death Dis 17, 237 (2026). https://doi.org/10.1038/s41419-026-08476-9
الكلمات المفتاحية: HPDL, الميتوكوندريا, تطور القشرة, صغر الرأس, الإجهاد التأكسدي