Clear Sky Science · ar
إعادة توصيل مصير خلايا الميلانوما: منظمات TRPM8 تحفز الاستماتة وتعزز سمّية خلايا القاتل الطبيعي
لماذا يهم توجيه «مستشعر البرد» ضد سرطان الجلد
الميلانوما شكل خطير من سرطان الجلد وغالبًا ما يتعلم التملص من الأدوية والجهاز المناعي معًا. تستكشف هذه الدراسة نقطة ضعف غير متوقعة في خلايا الميلانوما: بروتين يُدعى TRPM8، معروف بكونه المستشعر الذي يمكّن الخلايا العصبية من الشعور بالبرد أو بالمنثول. يبيّن الباحثون أن عقاقير مصممة بعناية لعرقلة TRPM8 يمكن أن تدفع خلايا الميلانوما إلى الانتحار المبرمج وفي الوقت نفسه تجعلها أكثر عرضة لهجمات خلايا القاتل الطبيعي (NK). هذا التأثير المزدوج يشير إلى نهج جديد لعلاج الميلانوما المتقدمة العنيدة.
مفتاح خفي على خلايا الميلانوما
من خلال تحليل قواعد بيانات سرطانية واسعة وفحص خلايا ميلانوما مشتقة من مرضى في المختبر، وجد الفريق أن TRPM8 أكثر وفرة بكثير في الميلانوما النقيلي مقارنة بالجلد الطبيعي، بما في ذلك الخلايا الميلانينية السليمة والخلايا الليفية الجلدية. أظهر التصوير أن TRPM8 يتواجد على سطح الخلية وعلى الأغشية الداخلية أيضًا، ما يضعه في مواقع استراتيجية للتأثير على سلوك الخلية. عند تطبيق مجموعة من الجزيئات الجديدة المستهدفة لـTRPM8، برز مركبان اثنان (المسمّيان 4 و9) بوضوح: خفّضا بحدة بقاء خلايا الميلانوما مع مرور الوقت بينما تركا خلايا الجلد الطبيعية إلى حد كبير سالمة. أكدت الاختبارات الجينية أن إزالة TRPM8 أبطلت قدرة هذه الأدوية على القتل، وأن زيادة TRPM8 جعلت خلايا الميلانوما أكثر حساسية، مما يثبت أن التأثير يعتمد على هذا القناة المحددة. 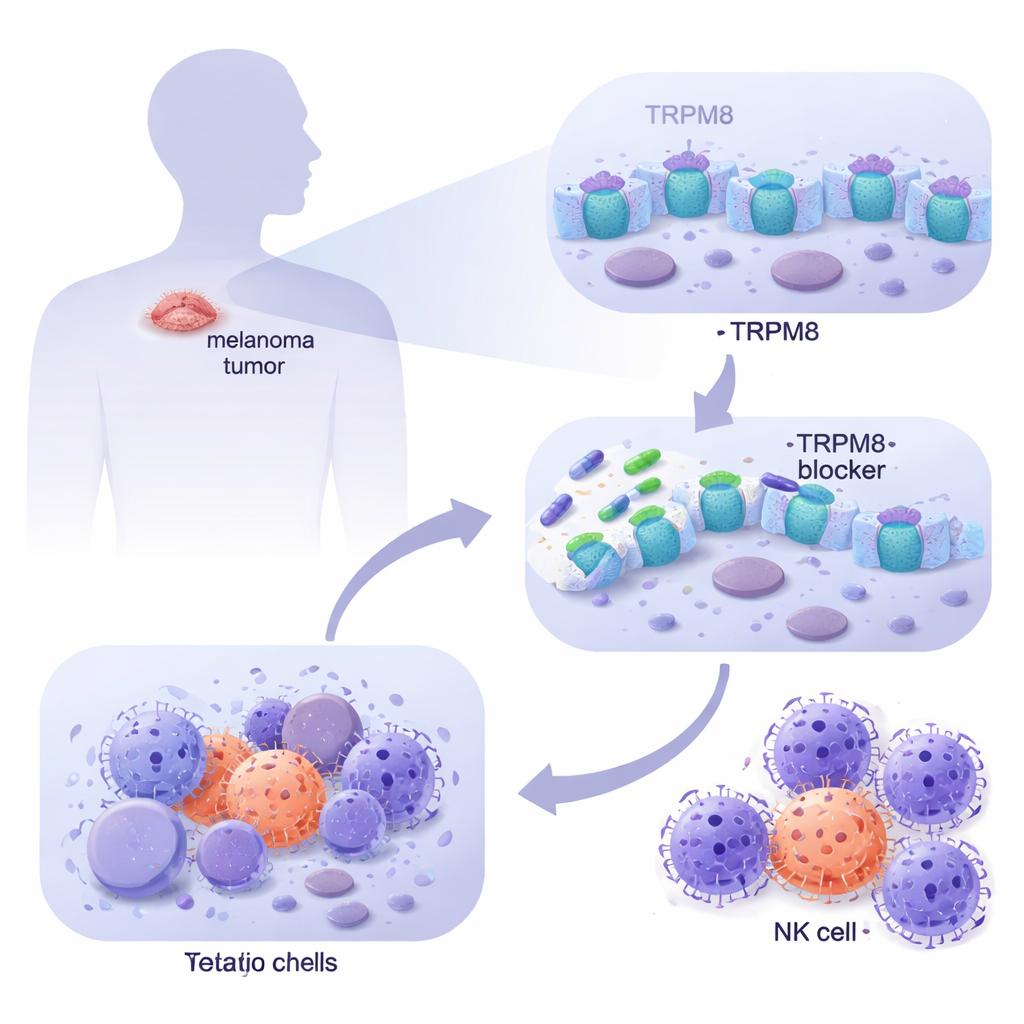
إرغام الخلايا السرطانية على أزمة طاقة
على عكس منشّطات TRPM8 التقليدية مثل المنثول التي تسبب تدفّقًا حادًا من الكالسيوم إلى الخلايا، لم تترجم هذه العوامل الجديدة إلى تغييرات في الكالسيوم. بدلاً من ذلك، أطلقت موجة من الإجهاد التأكسدي داخل خلايا الميلانوما. زادت المركبات بسرعة من الأنواع التفاعلية للأكسجين، خصوصًا داخل الميتوكوندريا، مصانع طاقة الخلية. أدت هذه الانفجار التأكسدي إلى فقدان الميتوكوندريا لشحنتها الكهربائية، وتفتتها، وتسريب السيتوكروم c، وهي خطوة رئيسية في تشغيل برنامج «الانتحار» الداخلي للخلية. الأنزيمات المضادة للأكسدة التي أزالت هذه الجزيئات التفاعلية أنقذت الخلايا إلى حد كبير، مما يدل على أن اختلال توازن الأكسدة والاختزال ليس أثرًا جانبيًا بل هو محرك موت الخلايا. ومؤشرات الموت الكلاسيكية التالية مثل تنشيط الكاسبيز-3 وتقطيع PARP أكدت أن الخلايا تمر بعملية استماتة مبرمجة وليس بضرر عشوائي.
تعطيل إشارات البقاء وإيقاظ الحارس
أدى الضرب التأكسدي إلى إطلاق استجابة إجهاد أوسع. فعّلت الأدوية بروتين ATM، مستقبل تلف الحمض النووي، وأدت إلى تراكم وتنشيط p53، بروتين مكافح للأورام معروف يقرر ما إذا كانت الخلية التالفة ينبغي أن تصلح نفسها أو تموت. في الوقت نفسه، أضعفت المركبات أحد المسارات الرئيسية لبقاء الميلانوما: مسار PI3K–AKT. عادةً ما يتفاعل TRPM8 ماديًا مع مكونات PI3K للمساعدة في إبقاء AKT في صورته النشطة المحفزة للنمو. بعد العلاج، تفككت هذه الشراكة وانخفضت نشاطات AKT، مما زاد الميل نحو موت الخلية. ومن المهم أن هذه التغيرات كانت بارزة في خلايا الميلانوما ولكن ليس في الخلايا غير السرطانية، مما يوحي بوجود نافذة علاجية تضرب الورم بشدة بينما تُبقي الأنسجة السليمة محمية.
جعل الأورام أكثر وضوحًا لفرق الضرب المناعية
تكمن خطورة الميلانوما أيضًا في قدرتها على الهروب من المراقبة المناعية. لذلك تساءل الباحثون عما يحدث للخلايا الورمية التي تنجو من جرعات منخفضة من حاصرات TRPM8 على فترات أطول. اكتشفوا أن هذه الخلايا المتبقية بدأت تعرض مزيدًا من علامة سطحية تُدعى ULBP1، التي تعمل كعلم استغاثة يتعرف عليها مستقبل NKG2D على خلايا NK. لم تتغير العلامات ذات الصلة الأخرى، مما يشير إلى تأثير انتقائي. في الكريات الثلاثية الأبعاد للميلانوما التي تحاكي الأورام الحقيقية بشكل أفضل، أدى المعالجة المسبقة بحاصرات TRPM8 ليس فقط إلى تقليص البنى وزيادة موت الخلايا بل جعلها أكثر عرضة لهجوم خلايا NK بكثير. عندما حُجبت ULBP1 أو NKG2D بأجسام مضادة، اختفى جزء كبير من القتل الإضافي، مما يبيّن أن التحسّن في الإزالة المناعية يمر عبر هذه المصافحة المحددة بين الورم وخلايا NK. 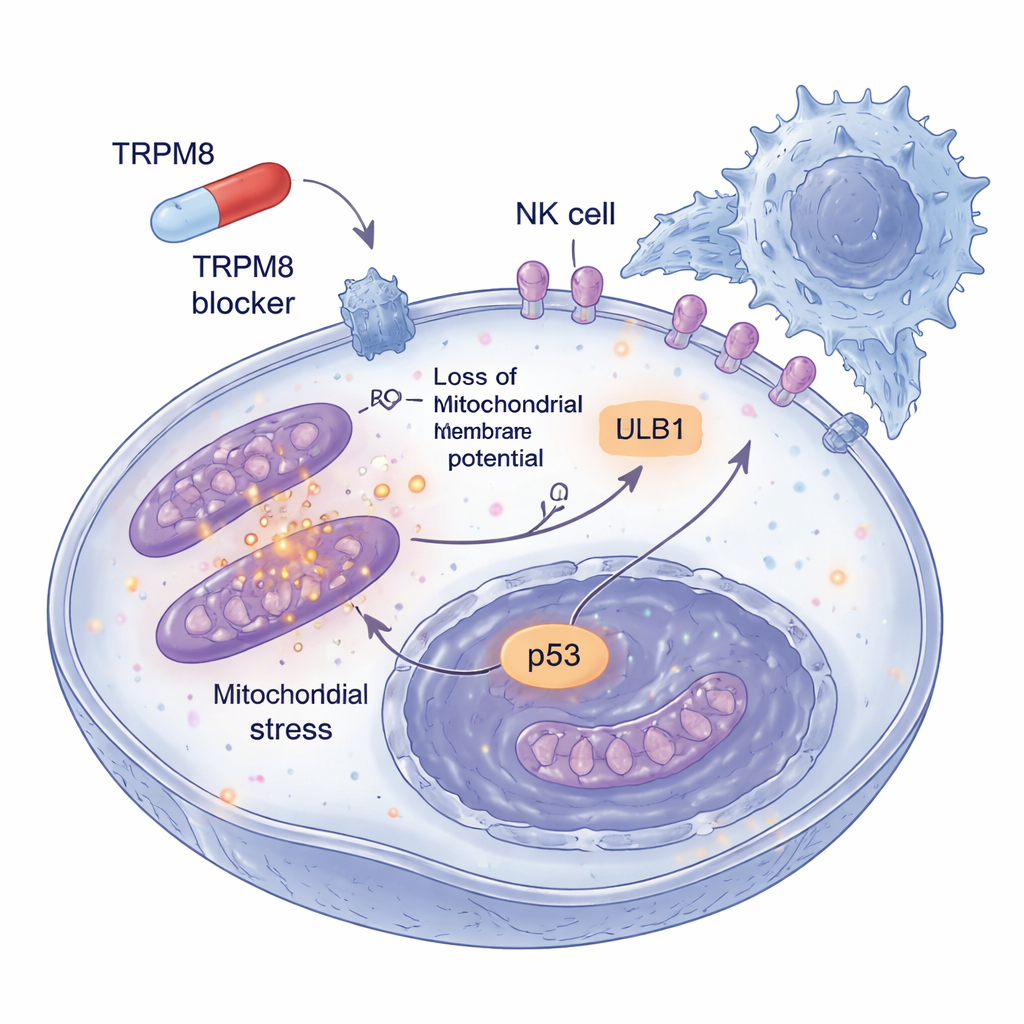
ماذا قد يعني ذلك لرعاية الميلانوما في المستقبل
ببساطة، حجب «مستشعر البرد» TRPM8 يحوله إلى رافعة علاجية: يدفع خلايا الميلانوما إلى أزمة ميتوكوندرية وجينية قاتلة بينما يعلّمها العلم لتدميرها بواسطة خلايا NK. وبما أن الأدوية تحمي خلايا الجلد الطبيعية ولا تضر خلايا NK نفسها، فهي تقدم أساسًا واعدًا لعلاجات جديدة. يقترح المؤلفون أن حاصرات TRPM8 يمكن أن تُدمج مع العلاجات المناعية الحالية لمهاجمة الميلانوما المتقدمة المقاومة للأدوية من اتجاهين: قتل الخلايا الورمية مباشرة وجعل الناجين أسهل على الجهاز المناعي أن يجدهم ويقضي عليهم.
الاستشهاد: Sorrentino, C., Lauretta, C., D’Angiolo, R. et al. Rewiring melanoma cell fate: TRPM8 modulators trigger apoptosis and boost NK cell cytotoxicity. Cell Death Dis 17, 223 (2026). https://doi.org/10.1038/s41419-026-08469-8
الكلمات المفتاحية: الميلانوما, TRPM8, الميتوكوندريا, الإجهاد التأكسدي, خلايا القاتل الطبيعي