Clear Sky Science · ar
تحفيز TRIM29 بواسطة اللاكتيلة يسبب سلوكًا غازيًا وانتشارًا إلى العقد اللمفاوية في سرطان المعدة عبر مسار Wnt/β‑catenin المتوسَّط بـ hnRNPA1
لماذا يهم هذا البحث
سرطان المعدة هو من أكثر السرطانات فتكا عالميًا جزئيًا لأنه ينتشر مبكّرًا إلى العقد اللمفاوية المجاورة، ما يجعل الجراحة وحدها صعبة الشفاء. يكشف هذا البحث كيف يفعّل تعديل كيميائي مرتبط باستقلاب الورم بروتينًا يُدعى TRIM29، مما يساعد خلايا السرطان على اقتحام الأنسجة المحيطة، وتحفيز نمو أوعية لمفاوية جديدة، ومقاومة العلاج الكيميائي. فهم هذه السلسلة من الأحداث يشير إلى سبل جديدة لإبطاء أو حتى منع انتشار سرطان المعدة.
شراكة خطيرة في أورام المعدة
بدأ الباحثون بمقارنة عينات سرطان المعدة بالنسيج السليم المجاور من 100 مريض، بالإضافة إلى قواعد بيانات جينية عامة واسعة. وجدوا أن TRIM29، وهو بروتين ارتبط سابقًا بتنظيم المناعة وسرطانات أخرى، كان أعلى باستمرار في الخلايا الورمية. كان المرضى الذين تحتوي أورامهم على TRIM29 أكثر عرضة لوجود السرطان في العقد اللمفاوية والأوعية الدموية ولهم بقاء إجمالي أسوأ. تشير هذه الأنماط إلى أن TRIM29 ليس مجرد علامة حاضرة، بل يشارك فعليًا في جعل سرطان المعدة أكثر عدوانية.
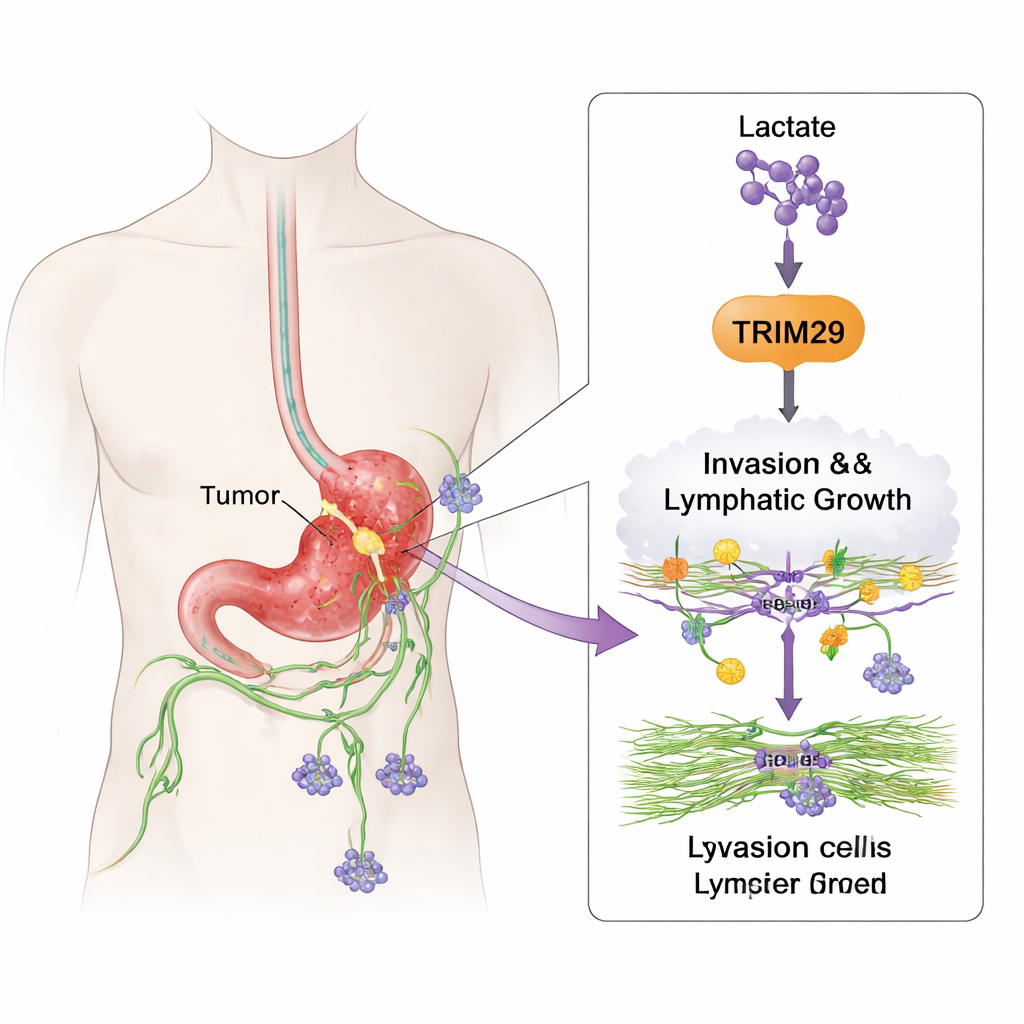
كيف تتعلم خلايا السرطان التنقل
لمعرفة ما يفعله TRIM29 عمليًا، عدّل الفريق مستوياته في خطوط خلايا سرطان المعدة. عندما قللوا TRIM29، أصبحت الخلايا أقل قدرة على الحركة وأقل قدرة على اختراق هلام ثلاثي الأبعاد يحاكي نسيج الجسم. وزيادة TRIM29 أعطت الأثر المعاكس، فزاد غزو الخلايا. كما فحص الباحثون الخلايا البطانية اللمفاوية، وهي الخلايا التي تبطن الأوعية اللمفاوية. شجعت الخلايا السرطانية الغنية بـ TRIM29 هذه الخلايا الوعائية على التفرّع وتشكيل هياكل أنبوبية، علامة على تكوّن أوعية لمفاوية جديدة. في نماذج الفئران، أنتجت الأورام ذات مستويات TRIM29 العالية المزيد من النقائل إلى الكبد والعقد اللمفاوية، بينما انتشرت الأورام مع تثبيط TRIM29 أقل وشكّلت أوعية لمفاوية أقل.
تتابع جزيئي: حماية منظّم رئيسي
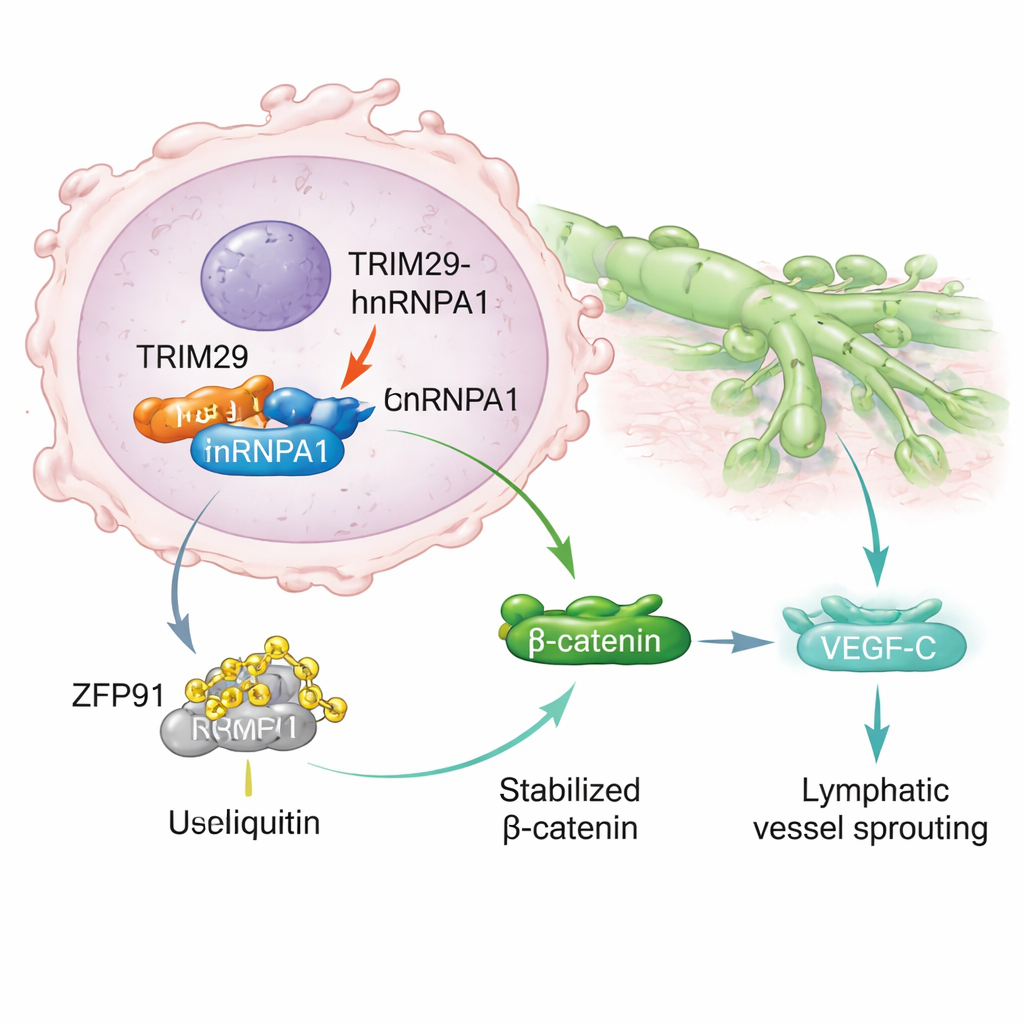
بتعمق أكبر، اكتشف العلماء أن TRIM29 يرتبط فعليًا ببروتين آخر، hnRNPA1، المعروف بتأثيره على معالجة الجينات وارتباطه بانتشار السرطان. عادةً يمكن وسم hnRNPA1 للتدمير بواسطة بروتين آخر، إنزيم يُدعى ZFP91، عبر نظام التخلص داخل الخلية. يتداخل TRIM29 مع هذه العملية عن طريق التنافس مع ZFP91 على الارتباط بـ hnRNPA1. عندما يكون TRIM29 وفيرًا، يحمي hnRNPA1 من الوسم والتحلل. نتيجة لذلك، يصبح hnRNPA1 أكثر استقرارًا ويتراكم في الخلايا السرطانية، مفعّلًا سلسلة إشارات تنتهي بتنشيط مسار Wnt/β‑catenin، وهو محفز معروف لنمو السرطان وحركته. هذا بدوره يزيد إنتاج VEGF‑C، جزيء يحفّز تكوّن أوعية لمفاوية جديدة، مما يمنح الخلايا السرطانية "طرقًا" إضافية للفرار.
تغذية السرطان باللاكتيت
يربط البحث أيضًا هذا السلوك الغازي بكيفية معالجة الأورام للسكر. تعتمد السرطانات سريعة النمو غالبًا على شكل استقلابي ينتج كميات كبيرة من اللاكتيت، وهو ناتج ثانوي كان يُعتبر نفاية في السابق. هنا يبين المؤلفون أن اللاكتيت يمكنه تعديل بروتينات الهيستون التي تُعبأ بها الحمض النووي، وبالتحديد في موضع يُدعى H3K9. تعمل هذه "اللاكتيلة" كمفتاح تشغيل لجين TRIM29، فترفع نشاطه. عندما خفضوا إنتاج اللاكتيت باستخدام أدوية استقلابية، انخفضت مستويات TRIM29؛ وعند رفع اللاكتيت ارتفعت مستويات TRIM29. أظهرت أنسجة سرطان المعدة من المرضى مستويات أعلى من لاكتيلة H3K9، والتي ارتبطت بزيادة TRIM29، ومزيد من انتشار العقد اللمفاوية، وبقاء أسوأ. بجوهرها، يساعد استقلاب الورم المعدل على كتابة برنامج جيني أكثر عدوانية.
طرق جديدة لتعزيز العلاج الكيميائي
لا تنقل الأوعية اللمفاوية الخلايا السرطانية فحسب؛ بل يمكنها أيضًا تصريف أدوية العلاج الكيميائي بعيدًا عن الأورام. باستخدام طعوم ورمية مشتقة من مرضى ونمت في فئران، اختبر الباحثون ما إذا كان حجب TRIM29 ونمو الأوعية اللمفاوية يمكن أن يُحسّن تأثير 5‑فلورويوراسيل (5‑FU)، الدواء القياسي لسرطان المعدة. إنقاص نشاط TRIM29 أو حجب تكوّن الأوعية اللمفاوية جعل كل منهما 5‑FU أكثر فعالية في تقليص الأورام وتقليل انقسام الخلايا. أعطت مزيجة الاستراتيجيتين أقوى استجابة، مما يشير إلى سبيل محتمل لتجاوز بعض أشكال مقاومة الدواء في المرض المتقدم.
ماذا يعني هذا للمرضى
يرسم هذا العمل صورة خطوة بخطوة: تولد أورام المعدة لاكتيت زائدًا، فيشغّل ذلك TRIM29؛ يحمي TRIM29 بدوره hnRNPA1، ويثبت مسارًا نمويًا، ويصعد تكوّن الأوعية اللمفاوية والانتشار إلى العقد اللمفاوية. سريريًا، تحدد مستويات TRIM29 العالية وعلامات اللاكتيلة المرتبطة بها المرضى الذين هم أكثر عرضة لمرض عدواني. في المستقبل، قد تُدمج أدوية تقلل إشارة اللاكتيت، أو تحجب TRIM29، أو تمنع نمو الأوعية اللمفاوية مع العلاجات الكيميائية الحالية لإيقاف انتشار سرطان المعدة وجعل العلاجات أكثر فاعلية.
الاستشهاد: Hua, R., Yu, J., Niu, Y. et al. Lactylation-drived TRIM29 induces invasive behavior and lymph node metastasis in gastric cancer via hnRNPA1-mediated Wnt/β-catenin pathway. Cell Death Dis 17, 222 (2026). https://doi.org/10.1038/s41419-026-08468-9
الكلمات المفتاحية: نقائل سرطان المعدة, TRIM29, اللاكتيت واللاكتيلة, تكوّن الأوعية اللمفاوية, مسار Wnt بيتا‑كاتينين