Clear Sky Science · ar
سيلينوميثيونين كمثبط للفيروبتوزيس بآليتين: تمليك السيلينيوم لتصنيع GPX4 يتجاوز الترانسسلفوريشن وتجميع القدرة الاختزالية على إزالة ROS مستقل عن نشاط GPX4
لماذا حماية خلايانا من «موت يشبه الصدأ» مهمة
يمكن أن تموت خلايا أجسامنا بطرق عديدة، وأحد أحدث وأكثرها إثارة للاهتمام يُسمى الفيروبتوزيس — شكل من أشكال تلف الأغشية الخلوية المدفوع بالحديد والذي يشبه الصدأ. يرتبط هذا المسار الآن بأمراض تمتد من إصابة الكلى إلى التنكس العصبي. يلعب العنصر النزيفي سيلينيوم، المعروف لدى كثيرين من مكملات الحمية، دورًا أساسيًا في إيقاف هذا الشكل الخطير من موت الخلايا. تستكشف هذه الدراسة كيف يمكن لحمض أميني شائع يحتوي على السيلينيوم، السيلينوميثيونين، أن يحمي الخلايا من الفيروبتوزيس عبر استراتيجيتين وقائيتين متميزتين، لا عبر واحدة فقط.
مكتشف جديد من بحث دوائي ضخم
للعثور على جزيئات صغيرة قادرة على منع الفيروبتوزيس، فحص الباحثون آلاف المركبات من أدوية معتمدة من إدارة الغذاء والدواء ومن منتجات طبيعية. استخدموا مادة كيميائية تسمى RSL3 لتحفيز الفيروبتوزيس في خطوط خلايا سرطانية بشرية ثم راقبوا موت الخلايا وتراكم الدهون المؤكسدة المتلفة في أغشية الخلايا. من بين جميع المرشحين، برز السيلينوميثيونين كمادة واقية قوية: خفّض كلًا من تلف الدهون وموت الخلايا عبر أنواع خلوية مختلفة وفي نموذجين رئيسيين للفيروبتوزيس — أحدهما مدفوع بتثبيط GPX4 مباشرة (بواسطة RSL3) والآخر بنقص السيستين، وهو لبنة أساسية لتشكيل مضاد الأكسدة غلوتاثيون. وضعت هذه النتائج السيلينوميثيونين في موقع مثبط واسع ومرن للفيروبتوزيس. 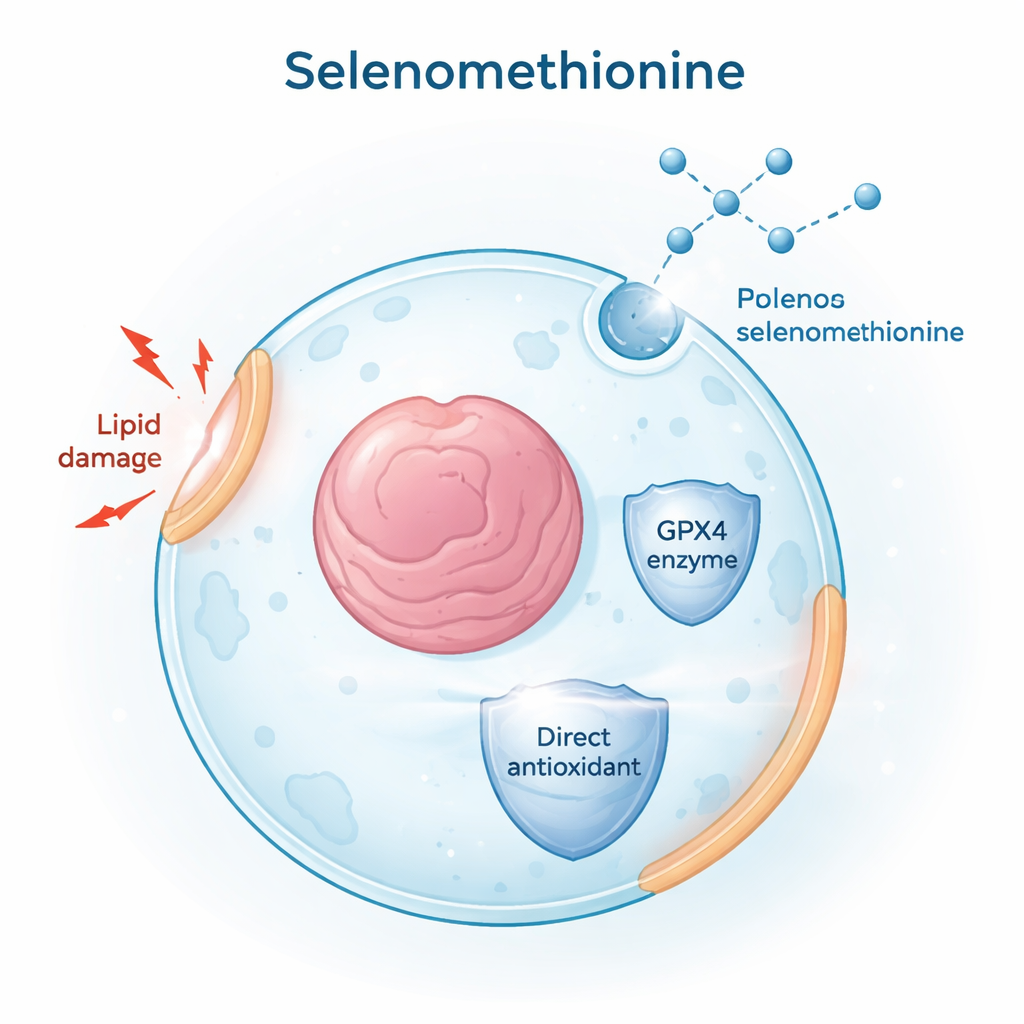
تموين السيلينيوم لإنزيم وقائي رئيسي
درع مضاد الفيروبتوزيس المركزي في الخلايا هو إنزيم يسمى GPX4، الذي يعتمد على السيلينيوم ليعمل. سعى الفريق لمعرفة ما إذا كان السيلينوميثيونين يغذي هذا المسار فحسب أم يفعل أكثر من ذلك. تتبعوا كيف يمكن تحويل السيلينيوم من السيلينوميثيونين إلى أشكال مناسبة لبناء GPX4، حتى عندما يكون الطريق المعتاد المسمى مسار الترانسسلفوريشن مثقلًا أو محجوبًا. باستخدام إخماصات جينية ومثبطات كيميائية لأنزيمات في مسارات الكبريت–السيلينيوم هذه، وجدوا أن السيلينوميثيونين لا يزال يعزز مستويات GPX4 ويحمي الخلايا. أظهر هذا أن الخلايا يمكنها الاستفادة من مسارات أيضية متعددة لاستخلاص السيلينيوم من السيلينوميثيونين والحفاظ على إنتاج GPX4، حتى في الأنسجة التي يكون فيها المسار الكلاسيكي ضعيفًا.
حماية لا تعتمد على الإنزيم المعتاد
إلى دهشة الفريق، عندما أزال الباحثون GPX4 تمامًا من الخلايا باستخدام تعديل جيني بواسطة CRISPR، استمر السيلينوميثيونين في الحماية من الفيروبتوزيس. ظل يقلل من تلف دهون الغشاء وموت الخلايا، مما يشير إلى أن GPX4 ليس القصة بأكملها. أشارت تجارب إضافية إلى أن بعض هذه الحماية تتضمن إدماج السيلينوميثيونين في بروتينات جديدة الصنع، لكن ذلك يمثل جزءًا فقط من التأثير. ركز المؤلفون بعد ذلك على التفاعل الكيميائي للسيلينوميثيونين نفسه. وجدوا أنه قادر مباشرة على تحييد أنواع الأكسجين التفاعلية (ROS)، بما في ذلك بيروكسيد الهيدروجين، ويتحول إلى شكل مؤكسد يسمى «سولفوكسيد». أكدت التحاليل الطيفية للكتلة وجود هذا المنتج، وإعطاء الخلايا لنسخة السولفوكسيد خفّض أيضًا الفيروبتوزيس، ما يوحي بأن الخلايا يمكنها إعادة تدويره إلى السيلينوميثيونين النشط ضمن دورة اختزالية-أكسدة.
من مزروعات الخلايا إلى حماية الكلى في حيوانات حية
لاختبار ما إذا كانت هذه الآليات مهمة على مستوى الكائن الحي، توجه الفريق إلى نموذج فأري لإصابة الكلية الحادة الناجمة عن دواء السرطان سيسبلاتين، وهي حالة معروفة بأنها تنطوي على الفيروبتوزيس. أبدت الفئران المعالجة بالسيسبلاتين فقدانًا في الوزن، وانتفاخًا في الكلى، وضعفًا في وظيفة الكلى، ومستويات مرتفعة من علامات الفيروبتوزيس. عندما تلقت الحيوانات السيلينوميثيونين، تحسنت العديد من هذه المشكلات: تعافى وزن الجسم، انخفض انتفاخ الكلى، عادت مؤشرات وظائف الكلى في الدم إلى وضعها الطبيعي، تراجعت الإشارات الالتهابية، وانخفضت مؤشرات تلف الدهون الكيميائية. كما أظهرت أنسجة الكلى مستويات أعلى من GPX4 وأضرارًا تركيبية أقل. كانت هذه الفوائد قابلة للمقارنة مع تلك المرصودة باستخدام فيروستاتين-1، مثبط تجريبي معروف للفيروبتوزيس. 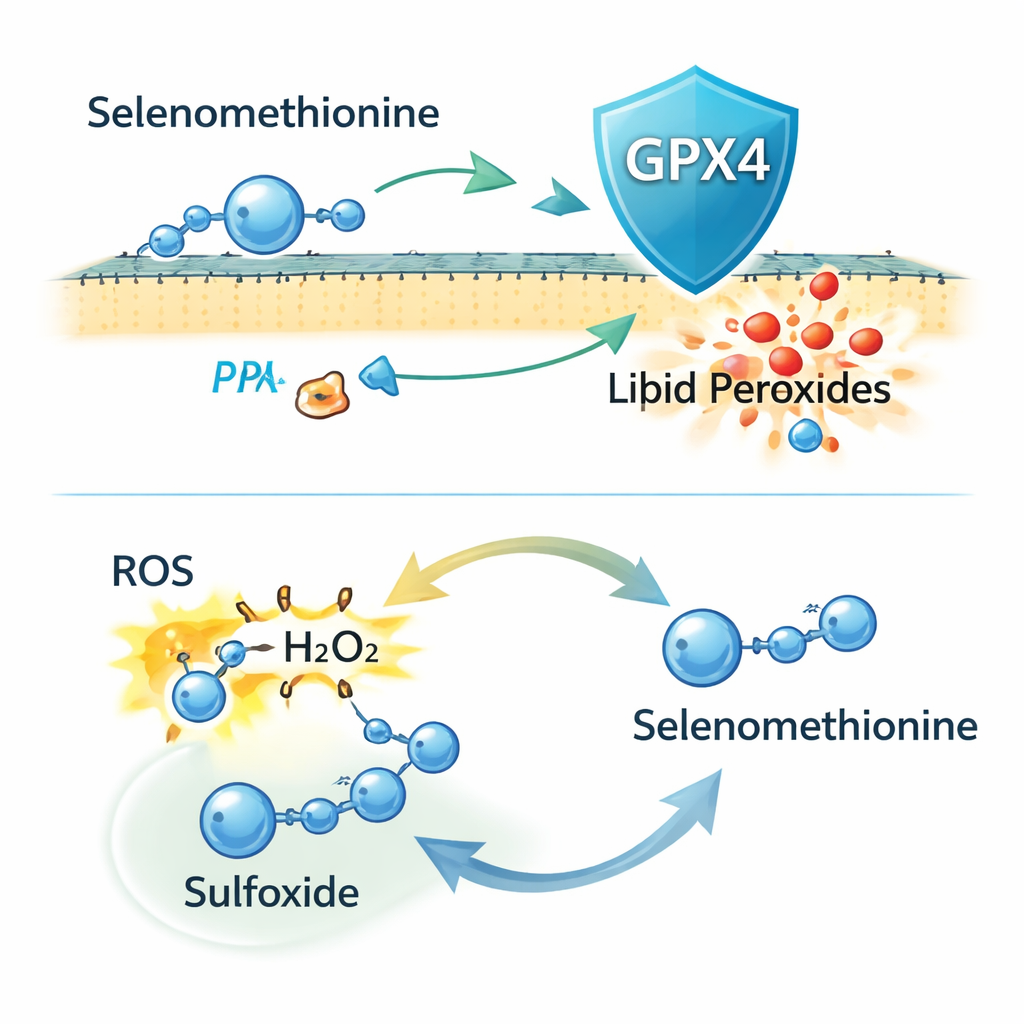
ما يعنيه ذلك للعلاجات المستقبلية
بمصطلحات بسيطة، تقترح هذه الدراسة أن السيلينوميثيونين يعمل مثل مطفأة حريق ذات غرضين ضد «صدأ» أغشية الخلايا المدفوع بالحديد. من جهة، يزود السيلينيوم لتمكين الخلايا من تصنيع المزيد من إنزيم GPX4، الذي يعمل كفرقة تنظيف داخلية للدهون المتلفة. ومن جهة أخرى، يمكن للسيلينوميثيونين نفسه امتصاص المؤكسدات الضارة وإعادة تدويره، مقدّمًا حماية احتياطية مستقلة عن GPX4. معًا، تجعل هذه الخصائص من السيلينوميثيونين مرشحًا واعدًا للوقاية أو علاج الأمراض التي يلعب فيها الفيروبتوزيس دورًا محوريًا، مثل تلف الكلى الناجم عن الأدوية وربما حالات أخرى ناجمة عن فرط الإجهاد التأكسدي.
الاستشهاد: Xia, C., Sun, X., Shao, J. et al. Selenomethionine as a dual-mechanism ferroptosis inhibitor: selenium-supply-driven GPX4 biosynthesis beyond transsulfuration and reductive-capacity-mediated ROS scavenging independent of GPX4 activity. Cell Death Dis 17, 224 (2026). https://doi.org/10.1038/s41419-026-08466-x
الكلمات المفتاحية: الفيروبتوزيس, السيلينيوم, سيلينوميثيونين, الإجهاد التأكسدي, الفشل الكلوي الحاد