Clear Sky Science · ar
إشارة أسيتلة PDHA1 تكبح الموت بالنحاس لتخفيف تأثير مضادات الأندروجين في سرطان البروستاتا
لماذا تهم هذه الدراسة
يعد سرطان البروستاتا من أكثر السرطانات شيوعًا بين الرجال، وكثير من الحالات المتقدمة تُعالج بأدوية تُعطل إشارات الهرمونات الذكرية. دواء أساسي هو إنزالوتاميد، الذي ينجح في البداية غالبًا لكنه يتوقف عن الفاعلية عندما تكتسب الأورام مقاومة. تكشف هذه الدراسة عن سبب غير متوقع لهروب بعض سرطانات البروستاتا من تأثير إنزالوتاميد وتوضح كيف أن حجب مسار استقلابي واحد قد يعيد حساسية الأورام، ما يفتح الباب لعلاجات أكثر ديمومة.
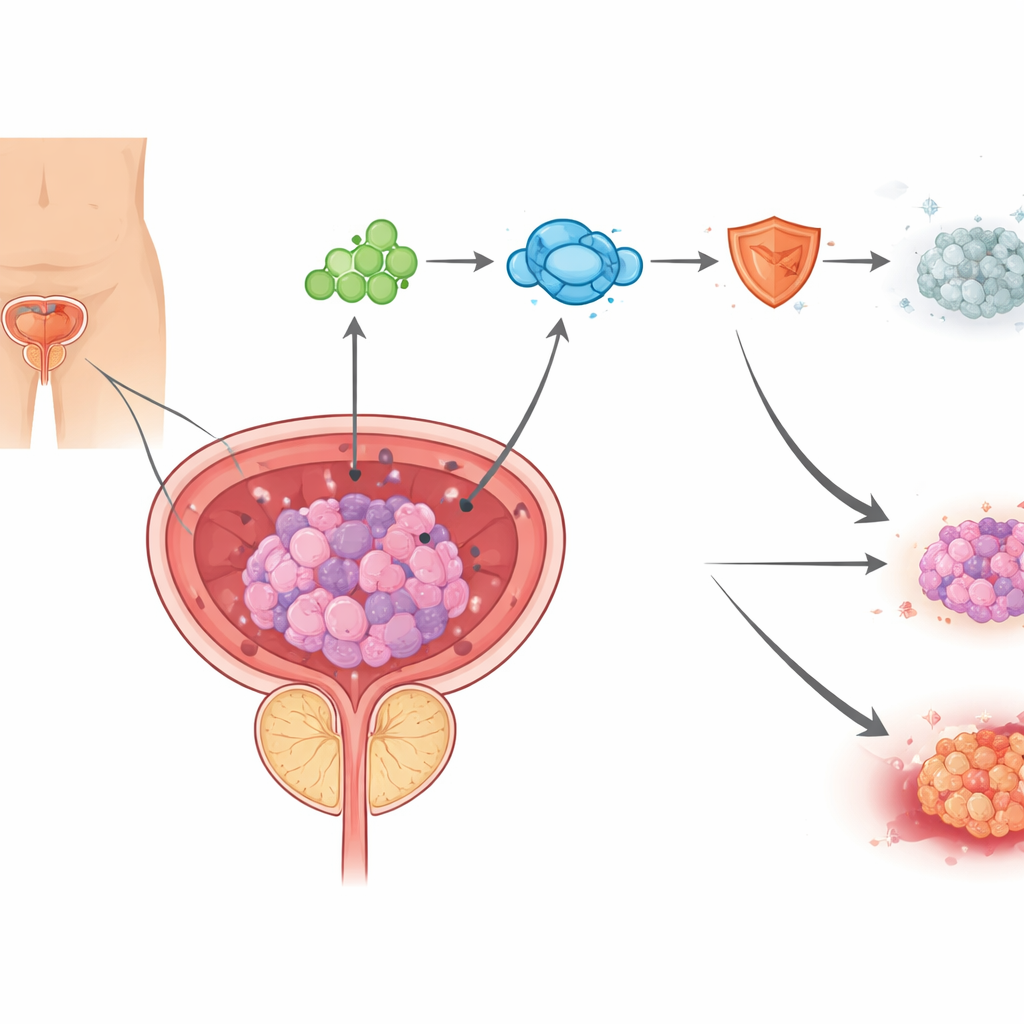
نوع جديد من موت الخلايا يقوده النحاس
تموت الخلايا بطرق متعددة، وتسعى أبحاث السرطان الحديثة بشكل متزايد إلى إعادة تفعيل هذه البرامج الطبيعية للموت داخل خلايا الورم. يركز الباحثون هنا على شكل جديد موصوف مؤخرًا من موت الخلايا يسمى الموت بالنحاس (cuproptosis)، الذي يُحدث عندما يتراكم النحاس داخل الميتوكوندريا، مصانع طاقة الخلية. في عينات سرطان البروستاتا من مرضى عولجوا بأدوية حاصرة للأندروجين، وجد الفريق علامات لتراكم النحاس وتلف الميتوكوندريا، إلى جانب تغييرات بروتينية تُعد سمات للموت بالنحاس. في زِرعات خلوية، زاد إنزالوتاميد من مستويات النحاس وأحدث تلفًا في الميتوكوندريا، ومركب يربط النحاس قد أنقذ الخلايا إلى حد كبير، ما يبين أن إنزالوتاميد يمكن أن يقتل خلايا سرطان البروستاتا جزئيًا بدفعها نحو الموت المحفز بالنحاس.
كيف تخفف الأورام سمية النحاس
إلا أن ليست كل الخلايا السرطانية تنهار. من خلال تحليل مجموعات بيانات متعددة لأورام البروستاتا المقاومة لإنزالوتاميد وتركيزهم على الجينات المرتبطة بالموت بالنحاس، حدَّد الباحثون بروتينًا بارزًا: PDHA1، وهو جزء مركزي من الآلية التي تحول وقود السكر إلى أسيتيل‑CoA، اللبنـة الخلوية الأساسية. كانت مستويات PDHA1 أعلى في الأورام المقاومة، مرتبطة ببقاء أسوأ ومرض أكثر عدوانية، وكانت مرتفعة أيضًا بفعل إنزالوتاميد نفسه. في تجارب مخبرية، أدى خفض PDHA1 إلى جعل الخلايا السرطانية أكثر حساسية بكثير لكل من إنزالوتاميد ودواء مُحدث للموت بالنحاس، بينما جعل رفع مستويات PDHA1 إزالتها أصعب. في الفئران، تقلصت الأورام ذات PDHA1 المنخفضة بشكل أكبر تحت علاج إنزالوتاميد، ما يؤكد أن هذا الإنزيم يساعد الأورام على الصمود أمام العلاج في كائنات حية.
درع استقلابي وفوق جيني ضد العلاج
ثم كشف الفريق كيف يبني PDHA1 هذا الدرع. بما أن PDHA1 يزود إنتاج أسيتيل‑CoA، اختبروا ما إذا كان قد يغير كيفية تغليف وقراءة الحمض النووي. عندما كانت مستويات PDHA1 مرتفعة، ارتفعت مستويات أسيتيل‑CoA والوسوم الكيميائية «الأسيتيلية» على بروتينات الهيستون، خصوصًا وسم مرتبط بالجينات النشطة. أحد المستفيدين الرئيسيين كان SLC7A11، ناقل يجلب السيستين إلى الخلايا لصنع الغلوتاثيون، مضاد أكسدة رئيسي. مع مزيد من PDHA1، أنتجت الخلايا مزيدًا من الغلوتاثيون؛ ومع نقص PDHA1، انخفضت السيستين والغلوتاثيون. ثم ارتبط الغلوتاثيون بالنحاس وعاكس سميته، مخففًا الإجهاد الذي يطلق الموت بالنحاس. إعادة الغلوتاثيون أو SLC7A11 يمكن أن تُلغي زيادة إجهاد النحاس التي لوحظت عند حجب PDHA1، ما يبرز أن سلسلة PDHA1–أسيتيل‑CoA–هيستون–SLC7A11–غلوتاثيون تتيح للخلايا السرطانية امتصاص النحاس وتجنب الموت.
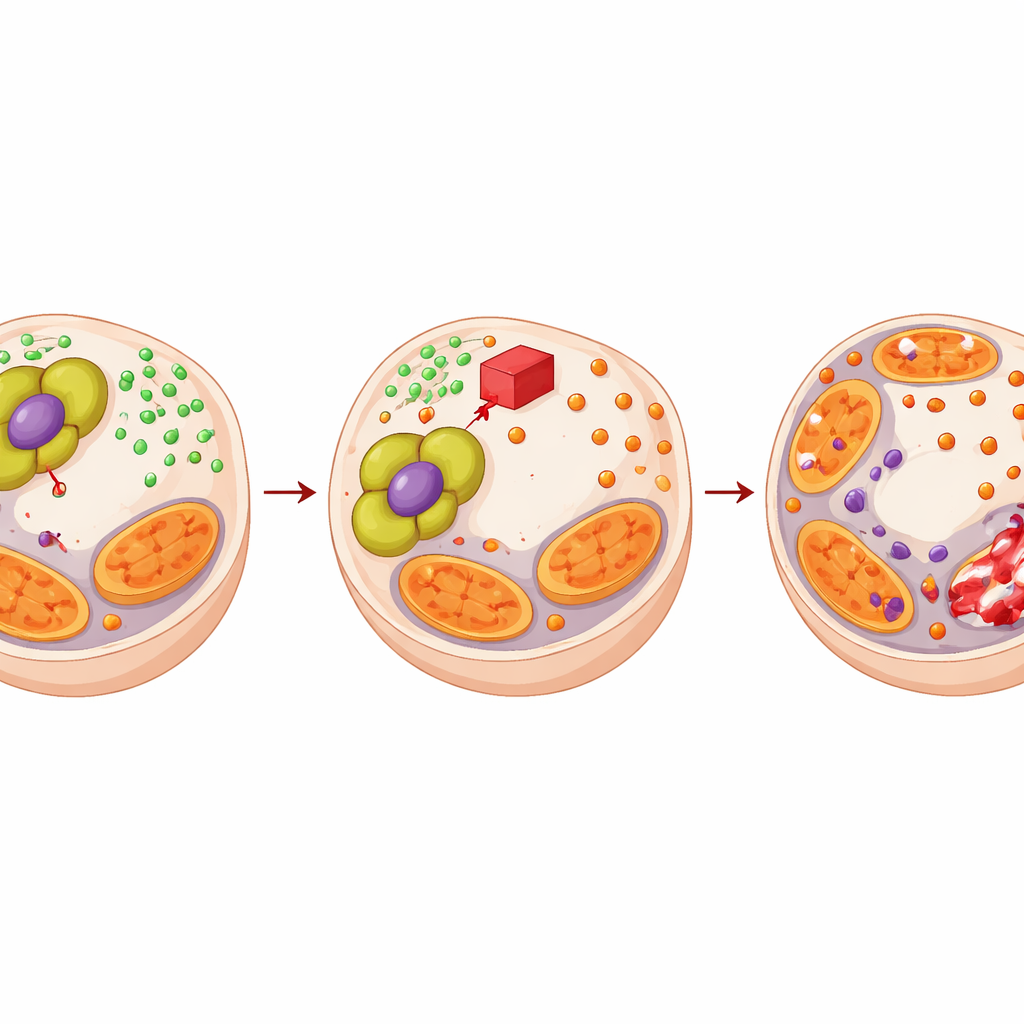
تحويل هذه الضعف إلى استراتيجية علاجية
لأن PDHA1 يساعد الأورام على مقاومة إنزالوتاميد من خلال تقوية نظام عازلة للنحاس هذا، تساءل الباحثون ما إذا كان دواء يستهدف PDHA1 يمكن أن يقلب الموقف. استخدموا CPI‑613، مركبًا يخلّ بتعقيد استقلابي مماثل. زاد CPI‑613 وحده من إجهاد النحاس وأتلف بروتينات الميتوكوندريا في خلايا سرطان البروستاتا لكنه لم يؤذِ خلايا البروستاتا الطبيعية. عند الجمع بينه وبين إنزالوتاميد، قلل CPI‑613 من نمو الخلايا السرطانية أكثر بكثير من أي من العلاجين بمفرده، مع تحليل رياضي يؤكد تآزرًا حقيقيًا. في نماذج أورام الفئران وزرعات أورام مشتقة من مرضى، أنتج الزوج العلاجي أورامًا أصغر وأنسجة ميتة أكثر وخلايا منقسمة أقل وبصمات أقوى للموت المحفز بالنحاس.
ماذا يعني هذا للمرضى
معًا، تُظهر هذه النتائج أن بعض سرطانات البروستاتا تهرب من إنزالوتاميد عن طريق إعادة برمجة استقلابها لإنتاج مزيد من أسيتيل‑CoA، وإعادة كتابة نشاط الجينات، وزيادة الغلوتاثيون الذي يمتص النحاس السام ويمنع الموت بالنحاس. من خلال تثبيط PDHA1، يمكن تفكيك هذه الدائرة الوقائية، مما يسمح للموت المحفز بالنحاس بالمضي قدمًا وإعادة تأثير العلاج المانع للهرمونات. رغم أن التجارب السريرية لا تزال مطلوبة، فإن العمل يشير إلى استراتيجية ملموسة وقابلة للاختبار: مزامنة إنزالوتاميد مع أدوية تستهدف PDHA1 مثل CPI‑613 لتجاوز المقاومة لدى الرجال المصابين بسرطان البروستاتا المتقدم والصعب العلاج.
الاستشهاد: Zhuang, R., Zhou, Q., Cheng, B. et al. PDHA1–acetylation signaling suppresses cuproptosis to attenuate anti-androgen effect in prostate cancer. Cell Death Dis 17, 243 (2026). https://doi.org/10.1038/s41419-026-08462-1
الكلمات المفتاحية: سرطان البروستاتا, مقاومة الأدوية, موت الخلايا المحفز بالنحاس, استقلاب السرطان, تنظيم فوق جيني