Clear Sky Science · ar
الازالة المتحدة لليوبيكويتين عبر USP30 تتحكم في مصير الجلوكوز الأيضي وتقدّم الورم
كيف تعيد الخلايا السرطانية توصيل استخدام السكر
الخلايا السرطانية مشهورة بـ«شهوتها للحلوى»: فهي تحرق السكر بطرق غير عادية لتغذية النمو السريع. تكشف هذه الدراسة عن مفتاح جديد، بروتين اسمه USP30، يساعد خلايا الورم على تقرير كيفية استخدام الجلوكوز. عبر ضبط بروتين آخر، هكسوكيناز 2 (HK2)، يستطيع USP30 دفع الخلايا السرطانية لحرق مزيد من السكر والنمو بسرعة أكبر، مما يشير إلى هدف جديد محتمل للأدوية المضادة للسرطان في المستقبل. 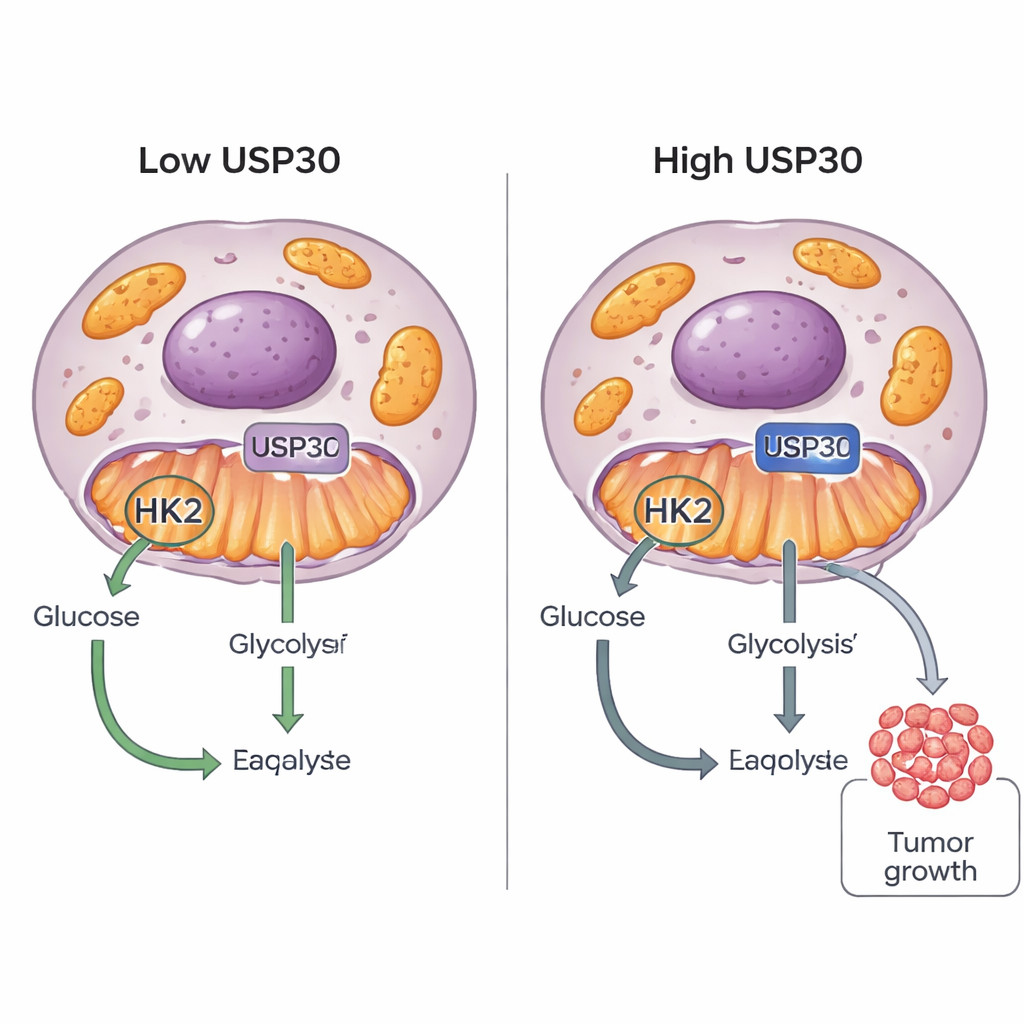
أسلوب حياة متعطش للسكر داخل الأورام
تستخرج معظم الخلايا السليمة الطاقة من المغذيات بكفاءة، لكن العديد من الخلايا السرطانية تفضّل مسارًا سريعًا وبسيطًا يُسمى التحلل السكري الهوائي، المعروف أيضًا بتأثير واربورغ. تمتص هذه الخلايا كميات كبيرة من الجلوكوز وتحوله بسرعة إلى لاكتات حتى عند توفر الأكسجين. هذه الاستراتيجية لا توفر طاقة فقط: بل تزود اللبنات الأساسية للحمض النووي والدهون والبروتينات، وتساعد الأورام على مقاومة الضغوط، وقد تضعف أيضًا هجمات الجهاز المناعي. عند بوابة هذا المسار يقف الهكسوكيناز، إنزيم يعلّم الجلوكوز الوارد بمجموعة فوسفات، ملزمًا إياه بالتفكك اللاحق والكيمياء الداعمة للنمو.
أنزيم ميتوكوندري يتصدر المشهد
USP30 هو إنزيم مستقر على السطح الخارجي للميتوكوندريا، مصانع طاقة الخلية. ينتمي إلى عائلة «المزيلات اليوبيكويتينية» التي تزيل علامات صغيرة تسمى يوبيكويتين من بروتينات أخرى، مما يغير غالبًا استقرارها أو موقعها أو نشاطها. كان معروفًا عن USP30 أدوار في خلايا الدماغ وفي ضبط جودة الميتوكوندريا، لكن تأثيره على السرطان لم يكن واضحًا. عبر التنقيب في قواعد بيانات جينية واسعة للسرطان، لاحظ الباحثون أن الأورام ذات مستويات أعلى من USP30 تميل إلى إبداء توقيعات أقوى لحرق الجلوكوز وضعف لتوقيعات حرق الدهون، مما يوحي بأن USP30 قد يساعد السرطانات على الانتقال نحو نمط حياة معتمد على السكر.
ربط USP30 بحراس السكر في الخلية
لاستكشاف هذا الرابط، خفض الفريق أو أزال USP30 في عدة خطوط خلوية سرطانية وقيَّم كيفية معالجتها للطاقة. باستخدام أجهزة تتعقب إنتاج الحمض واستهلاك الأكسجين في الزمن الحقيقي، وجدوا أن فقدان USP30 قلل بشكل حاد كلا من التحلل السكري والتنفس الميتوكوندري. انخفض إنتاج اللاكتات واستهلاك الجلوكوز، مما أظهر أن محرك حرق السكر لدى الخلايا تباطأ. سلسلة من تجارب قياس الطيف الكتلي كشفت بعد ذلك أن USP30 يتفاعل فعليًا مع عدة إنزيمات مرتبطة باستقلاب الجلوكوز، وخصوصًا الهكسوكينازات HK1 وHK2. أظهرت اختبارات لاحقة أن هذا التفاعل يعتمد على النشاط التحفيزي لـUSP30 ويحدث مباشرة، وليس عبر شركاء وسطيين فقط.
مقبض جزيئي دقيق على هكسوكيناز 2
تعميقًا في التفاصيل، وجدت الدراسة أن USP30 يزيل أنواعًا محددة من سلاسل اليوبيكويتين — روابط غير نمطية — من HK1 وHK2. بالنسبة لـHK2، يحدث هذا التحرير عند حمض أميني حاسم واحد، الليسين 144 (K144). عندما يتحور K144 بحيث لا يمكنه حمل اليوبيكويتين، يصبح HK2 أكثر استقرارًا، ويرتبط بقوة أكبر ببروتين القناة VDAC1 على الميتوكوندريا، ويظهر نشاط إنزيميًا أعلى. الخلايا المعدلة حملت هذا التغير K144 أرسلت المزيد من HK2 إلى الميتوكوندريا، حرقت مزيدًا من الجلوكوز، أطلقت المزيد من اللاكتات، وأظهرت نموًا وحركة أسرع في أطباق المختبر. في الفئران، نمت الأورام المشتقة من خلايا تحمل HK2 المتحول عند K144 أكبر وأسرع من تلك ذات HK2 الطبيعي، مما يبرز قوة هذا المفتاح الجزيئي الصغير. 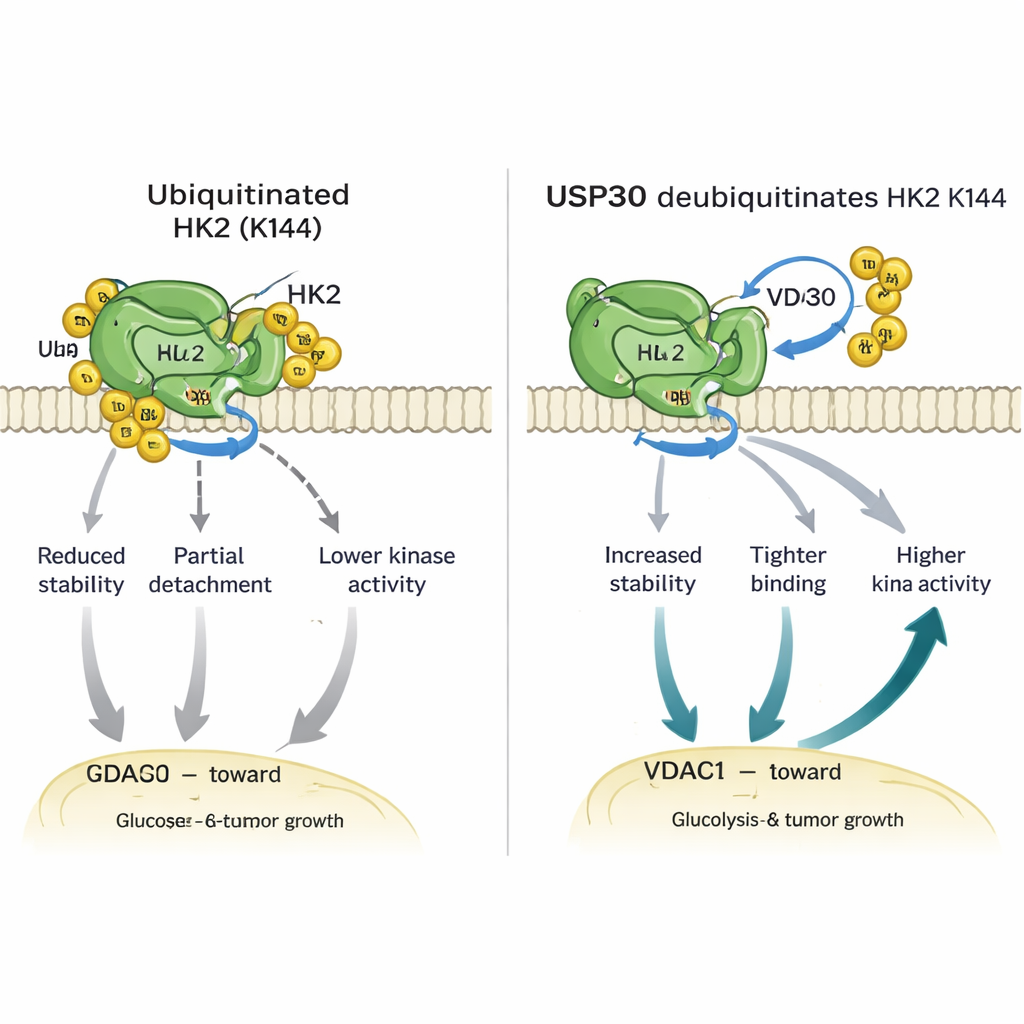
تحويل مفتاح أيضي إلى ميزة نمو
ترسم هذه النتائج سلسلة واضحة من الأحداث: يربط USP30 بـHK2، ويجرد موقع K144 من علامات اليوبيكويتين، وبذلك يحافظ على HK2 نشطًا ومرابطًا على الميتوكوندريا. هذا يعزز التحلل السكري، يزود انقسام الخلايا السرطانية وهجرتها، وفي النهاية يسرع نمو الورم. عندما يغيب USP30 أو يكون غير نشط، يصبح HK2 أقل استقرارًا وأقل فعالية، وتفقد الخلايا السرطانية جزءًا من ميزتها الأيضية. من منظور مبسط، يعمل USP30 كميكانيكي يبقي محرك سكر الخلية السرطانية مضبطًا ومثبتًا — أزل الميكانيكي، ويتعثر المحرك.
ما الذي يعنيه هذا لعلاجات السرطان المستقبلية
للغير متخصص، الخلاصة الأساسية أن الخلايا السرطانية تعتمد على تحكم دقيق في كيفية حرقها للسكر، وUSP30 هو مقبض جديد مكتشف على لوحة التحكم هذه. عبر تثبيت HK2 عند موقع محدد واحد، يساعد USP30 الأورام على تشغيل استقلابها الجلوكوزي الجشع والنمو بشكل أشرس. قد تضعف الأدوية التي تمنع USP30، أو التي تعطل تماسكه مع HK2 عند الليسين 144، الأورام عبر تجويع محرك السكر دون بالضرورة إلحاق مضار كبيرة بالخلايا الطبيعية بنفس الدرجة. لذلك تضيف هذه الدراسة قطعة مهمة لفهم كيف تعيد السرطان تركيب الاستقلاب وتقترح زاوية واعدة جديدة للعلاجات المستهدفة.
الاستشهاد: Haowei, Z., Li, X., Liao, W. et al. USP30-mediated Deubiquitination of Hexokinase 2 controls the metabolic fate of glucose and tumor progression. Cell Death Dis 17, 225 (2026). https://doi.org/10.1038/s41419-026-08459-w
الكلمات المفتاحية: استقلاب السرطان, التحلل السكري, هكسوكيناز 2, USP30, تأثير واربورغ