Clear Sky Science · ar
النسخ الحذفية المحددة للبويضات لوحدات eIF2 تسبب موتًا مبرمجًا لبويضات الفئران داخل الجريبات النامية المبكرة عبر خلل وظيفي ميتوكوندري وتلف الحمض النووي
لماذا تهم حياة الخلايا البيضية
تولد النساء ومعهن كل الخلايا البيضية التي سيملكنها طوال العمر، مخزنة داخل هياكل دقيقة في المبيض تسمى الجريبات. عندما تُفقد هذه الجريبات بسرعة كبيرة، قد تتطور لدى المرأة حالة قصور المبايض المبكر (POI)، وهي حالة تؤدي إلى العقم المبكر وغالبًا أعراض شبيهة بانقطاع الطمث في سن مبكرة. تسأل هذه الدراسة في الفئران سؤالًا أساسيًا لكنه حاسم: ماذا يحدث داخل الخلايا البيضية عندما يخطئ خطوة رئيسية في صنع بروتينات جديدة، وكيف يمكن لذلك أن يؤدي إلى فقدان الخصوبة المبكر؟
مفتاح بدء صنع البروتين في الخلية
للبقاء بصحة جيدة، يجب أن تصنع الخلايا البيضية باستمرار البروتينات الصحيحة في الوقت المناسب. جزء مركزي من هذه العملية هو آلة جزيئية ثلاثية الأجزاء تُسمى eIF2، التي تساعد على إطلاق عملية صنع البروتين من الرسائل الوراثية. قام الباحثون بإيقاف تشغيل اثنين من أجزاء eIF2 بشكل انتقائي، المسماة eIF2α وeIF2β، فقط في بويضات الفئران في المراحل المبكرة من نمو الجريب. عندما كان أي من هذين الجزأين مفقودًا، أصبحت الفئران الإناث عقيمة تمامًا. كانت مبايضهن أصغر حجمًا، وتقدّم الجريبات من المراحل المبكرة إلى الجريبات الناضجة المفرزة للبويضات توقف إلى حد كبير، مع عدد أقل بكثير من الجريبات في كل مرحلة لاحقة. مع مرور الوقت، استُنزفت جميع الجريبات تقريبًا، مما يحاكي حالة شديدة تشبه قصور المبايض المبكر في مرحلة مبكرة.
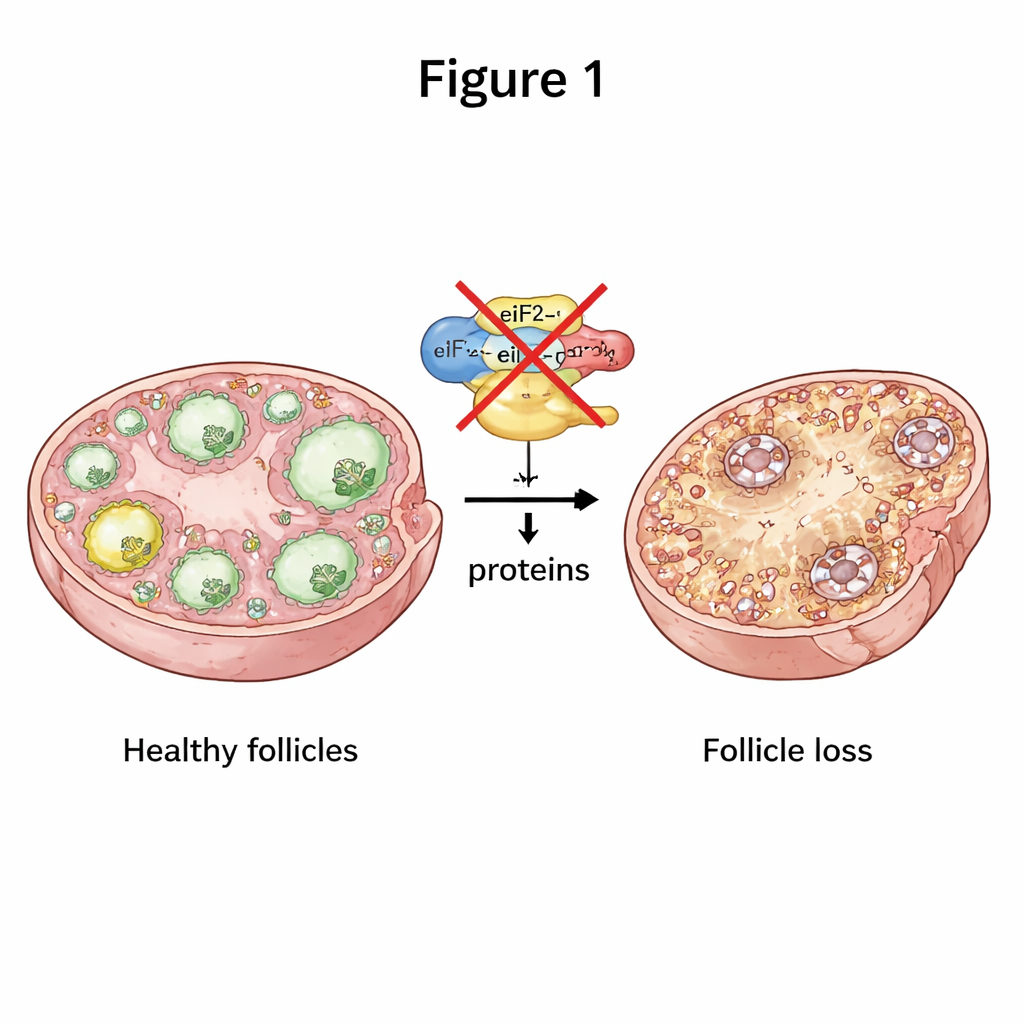
عندما تنهار الاتصالات في المبيض
الجريبات ليست مجرد بويضات عائمة بمفردها؛ بل شراكات وثيقة بين البويضة وخلايا مساعد حولها تُدعى خلايا الحبيبات. وجد الفريق أنه بدون eIF2β، أنتجت البويضات كمية أقل بكثير من عدة بروتينات إشارية حاسمة التي تدعم نمو خلايا الحبيبات وتوفير المغذيات. كانت الجسور الفيزيائية بين البويضة وخلايا الحبيبات مفككة ومختصرة، وبدا أن الأهداب السطحية للبويضة متثلمة ومتضررة تحت المجهر الإلكتروني. قسمت خلايا الحبيبات في هذه الجريبات أقل وماتت بمعدل أعلى. أدى هذا الانهيار في التواصل ذي الاتجاهين إلى عدم قدرة الجريبات على النمو بشكل صحيح، مما دفع المبيض نحو فقدان الجريبات.
فشل الطاقة في بطاريات البويضة
تعد الميتوكوندريا، التي يُطلق عليها غالبًا محطات طاقة الخلية، مهمة بشكل خاص في الخلايا البيضية لأنها توفر الطاقة اللازمة للنمو والتطور الجنيني لاحقًا. في بويضات ناقصة eIF2β، انخفض معدل إنتاج البروتين الجديد بشكل عام، وانخفضت مستويات العديد من البروتينات المرتبطة بالميتوكوندريا. أصبحت الميتوكوندريا طويلة بشكل شاذ، وتكتلت بالقرب من سطح الخلية، وأظهرت فرقًا أضعف في الجهد الغشائي، وانخفاضًا في الطاقة (ATP)، وعددًا أقل من نسخ الحمض النووي الميتوكوندري. في الوقت نفسه، تراكمت في الخلايا مستويات عالية من أنواع الأكسجين التفاعلية (ROS)، وهي جزيئات أكسجينية مهاجمة يمكنها إتلاف مكونات الخلية. معًا كشفت هذه التغيرات عن انهيار عميق في ديناميكيات ووظيفة الميتوكوندريا.
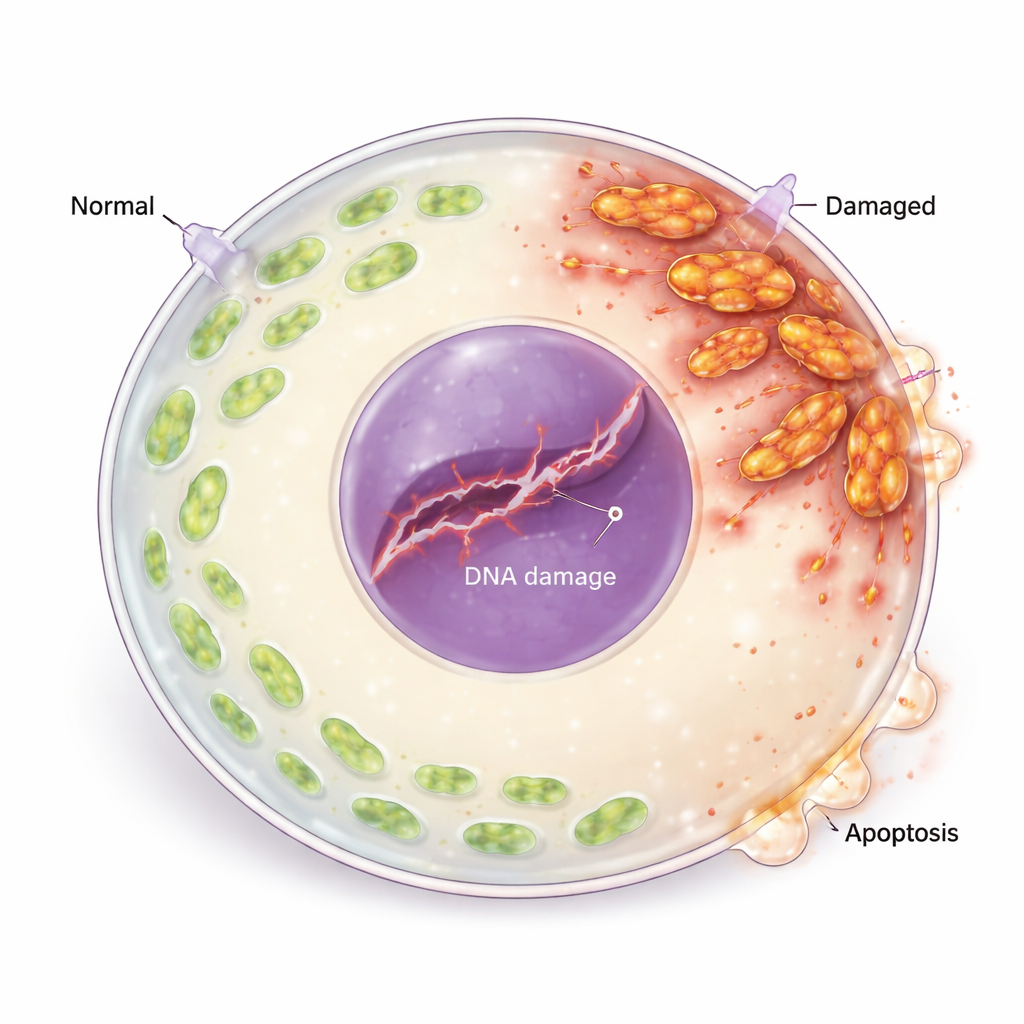
من الإجهاد التأكسدي إلى تلف الحمض النووي وموت الخلايا
لم تضر أنواع الأكسجين التفاعلية المفرطة الميتوكوندريا فحسب؛ بل أضرت أيضًا بالمادة الوراثية للبويضة. رصد الباحثون زيادة في علامات انكسار سلاسل الحمض النووي وتنشيط آليات استجابة تلف الحمض النووي في الخلية، بما في ذلك بروتينات تستشعر وتبليغ الإصابة الوراثية. انخفض بروتين إصلاح رئيسي، مما يشير إلى أن التلف لم يكن يُصلح بكفاءة. بعد ذلك، انقلب توازن منظمي الحياة والموت: ارتفعت البروتينات المروجة للموت بينما انخفضت البروتينات الواقية، وأظهرت البويضات علامات واضحة على الموت المبرمج للخلايا (الاستماتة). عندما عالج الفريق البويضات بمضاد أكسدة (N-أسيتيل سيستين)، انخفضت مستويات ROS، وتناقصت معالم تلف الحمض النووي والاستماتة، وتحسّن نضوج البويضات، مما ربط الإجهاد التأكسدي مباشرة بفقدان الخلايا البيضية.
ماذا يعني هذا بالنسبة لفشل المبيض المبكر
من خلال تتبع الأحداث ابتداءً من مركب جزيئي واحد (eIF2) إلى إنتاج بروتين معطّل، وانهيار الميتوكوندريا، والإجهاد التأكسدي، وتلف الحمض النووي، وأخيرًا موت البويضة، تقدم هذه الدراسة سلسلة مفصلة من الأحداث التي يمكن أن تدمر مخزون المبيض. تعزز الدراسة الفكرة القائلة إن الطفرات في عوامل بدء الترجمة، التي لوحظت بالفعل لدى بعض النساء المصابات بـPOI، يمكن أن تضر البويضات مباشرة عبر هذا المسار. وتشير أيضًا إلى طرق محتملة للمساعدة: قد تدعم مضادات الأكسدة، أو معدلات استجابة الإجهاد، أو علاجات تحمي الجريبات المبكرة (مثل هرمون مضاد ميولر الذي حافظ جزئيًا على الجريبات النائمة في هذه الفئران) الخصوبة يومًا ما لدى المرضى الذين تكون مبايضهم عرضة لضغوط مماثلة.
الاستشهاد: Liu, H., Wang, W., Li, B. et al. Oocyte-specific knockout of eIF2 subunits causes apoptosis of mouse oocytes within the early growing follicles via mitochondrial dysfunctions and DNA damage. Cell Death Dis 17, 196 (2026). https://doi.org/10.1038/s41419-026-08449-y
الكلمات المفتاحية: قصور المبايض المبكر, موت بويضات مبرمج, خلل وظيفي ميتوكوندري, ترجمة البروتين, أنواع الأكسجين التفاعلية