Clear Sky Science · ar
كبح ابتلاع مستقبلات الخلايا البائية المحفَّزة بمولدات الذات (BCR) كاستراتيجية علاجية في لمفوما الخلايا البائية كبيرة الحجم المنتشرة (DLBCL)
لماذا هذا مهم للمرضى
تُعد لمفوما الخلايا البائية كبيرة الحجم المنتشرة (DLBCL) أكثر سرطانات الدم سريعة النمو شيوعًا بين البالغين، ولا يزال العديد من المرضى يعانون من نكس بعد العلاج الكيميائي‑المناعي المعياري. تستكشف هذه الدراسة نقطة ضعف مفاجئة في شريحة رئيسية من هذه الأورام: اعتمادها على مستقبل سطحي للخلايا يسمى مستقبل الخلايا البائية (BCR). من خلال إظهار أن حجب آلية سحب هذا المستقبل داخل الخلية يمكن أن يقوّض بقاء الخلايا السرطانية، تفتح النتائج الباب أمام إعادة استخدام أدوية مضادة للغثيان ومضادات ذهان قديمة كمساعدات مستهدفة ضد اللمفوما.
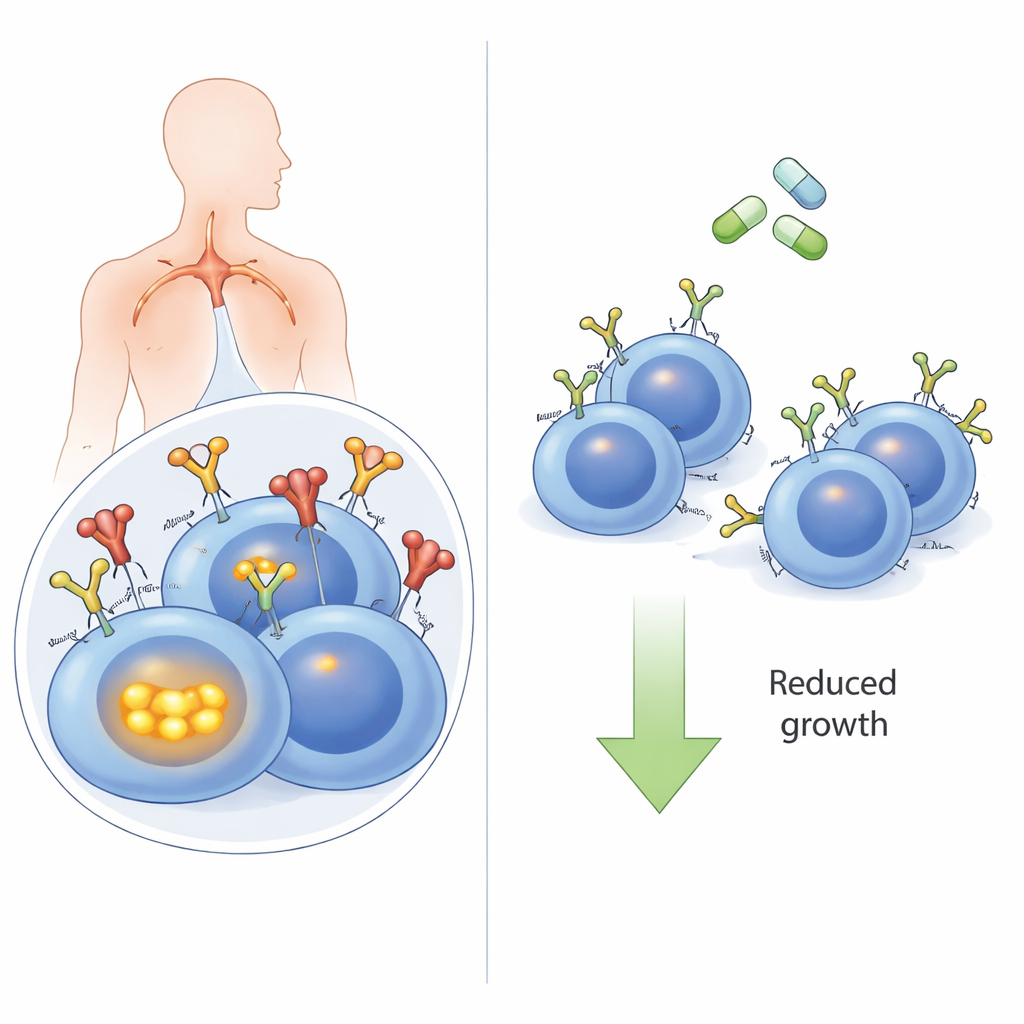
الهوائي الخلوي للسرطان
تستخدم الخلايا البائية، وهي نوع من خلايا الدم البيضاء، مستقبل الخلايا البائية الموجود على سطحها للتعرّف على التهديدات. في العديد من حالات DLBCL، وخاصة النمط عالي المخاطر المعروف باسم «الخلايا البائية المنشطّة» (ABC)، يتم اختطاف هذا المستقبل لإرسال رسائل دائمة «البقاء والنمو». كثيرًا ما تتعرف هذه المستقبلات على جزيئات من جسم المريض نفسه (مولدات ذات)، والتي تعمل مثل جرس باب عالق. عندما يرتبط مولد الذات، لا يقتصر دور BCR على الإشارة عند السطح فحسب: بل يُسحب إلى داخل الخلية وينضم إلى مجموعة بروتينية داخلية تحتوي على مجسّات مثل TLR9 وMYD88. ثم يشغّل هذا المركب الضخم مسار الإشارة القوي NFκB المحفّز للنمو. حتى الآن، لم يكن واضحًا ما إذا كانت هذه الرحلة الداخلية للمستقبل ضرورية فعلاً للإشارات المحرِّكة للسرطان.
إعادة برمجة الهوائي لاختبار حدوده
للإجابة عن هذا السؤال، استخدم الباحثون تعديل الجينات بتقنية كريسبر لتغيير «نهايات» BCR بدقة في خطوط خلايا اللمفوما. استبدلوا مناطق التعرّف الطبيعية المفعمة بالتفاعل الذاتي بنُسخ تتعرف على البيضين (ovalbumin)، وهو بروتين بيض غير ضار يُستخدم كأداة مختبرية. لم تعد هذه المستقبلات المعدّلة تمسك بمولدات الذات المعتادة، لكنها ظلت قابلة للتحفيز بشكلٍ مُراقَب بإضافة البيضين. في خلايا لمفوما من نمط ABC التي تعتمد عادةً على ربط مولد الذات، أدّت هذه التبديلة إلى خفض حاد في نشاط العديد من الإنزيمات الإشارية الرئيسية وتراجع في جينات المستجيبة لـNFκB. نمت الخلايا ببطء أكبر، على الرغم من وجود كمية أكبر من BCR على السطح، مما يوضح أن الارتباط المستمر بمولدات الذات والإشارات الداخلية اللاحقة حاسمان لبقائها.
سحب المستقبلات إلى الداخل: خطوة حاسمة
ثم نظر الفريق مباشرةً فيما يحدث لـBCR بعد التقاءه بمولده. في نماذجهم المهندَسة، تسبَّب كل من المحفزات المبنية على الأجسام المضادة والبياض البيض في اختفاء المستقبل من سطح الخلية خلال دقائق، مؤكِّدين الابتلاع السريع. حدث هذا ليس فقط عندما كان المستضد معلقًا خارج الخلية، بل أيضًا عندما عُرض اصطناعيًا على غشاء نفس الخلية، محاكيًا حالات ورمية حقيقية معينة. إبقاء هذا المرور الداخلي محجوبًا وراثيًا، باستخدام شكل سائد‑سلبي لبروتين يسمى دينامين‑2 الضروري للابتلاع المعتمد على الكلاثرين، أبقى BCR على السطح، وقصَّر مركبات BCR–TLR9–NFκB الداخلية، وخفّض جينات NFκB المستهدفة، وأبطأ نمو الخلايا. ومن المثير للاهتمام أنه عند حجب الابتلاع، زادت بعض إشارات BCR «الخلفية» على السطح، مما يشير إلى أن الخلايا السرطانية قد تحاول التعويض عن طريق تعزيز وضع إشاري أضعف ومحيطي.
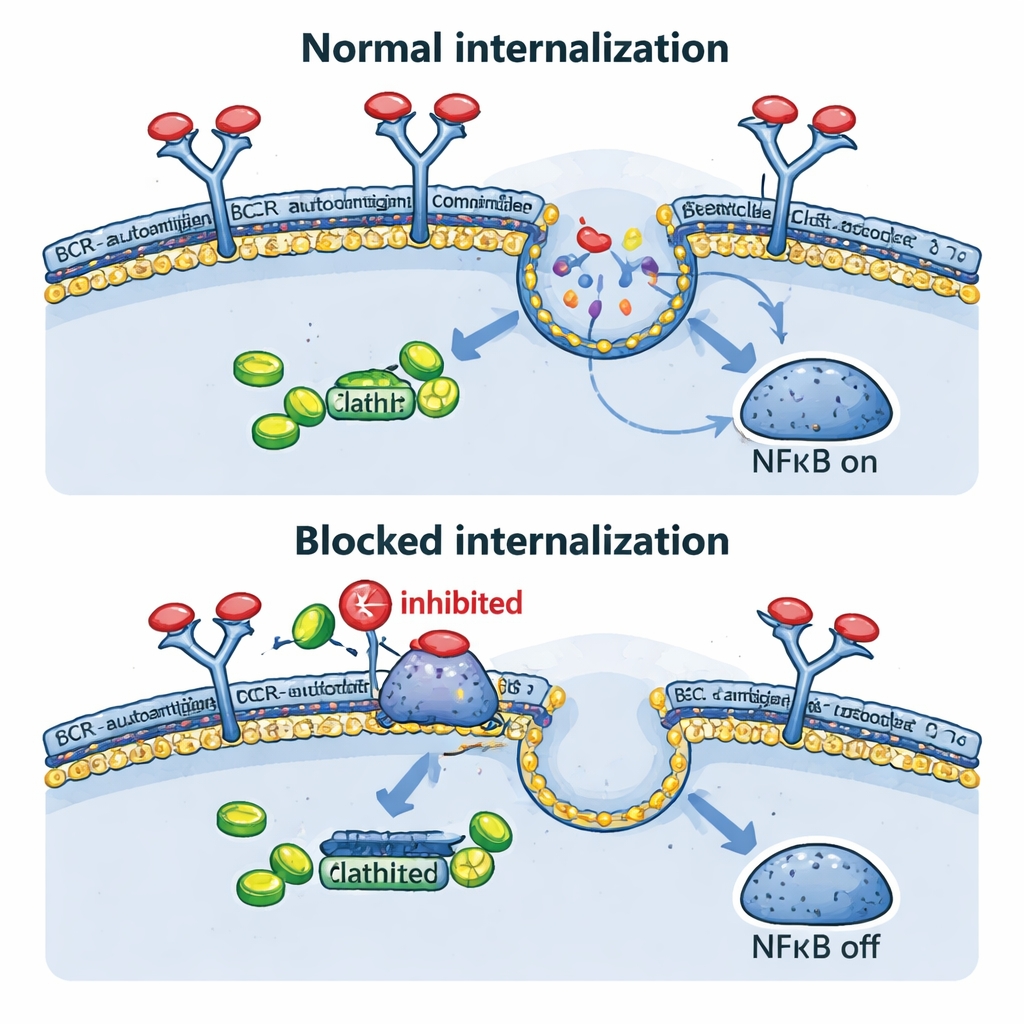
أدوية قديمة، حيل جديدة
نظرًا لأن تطوير أدوية جديدة بطيء ومكلف، تساءل المؤلفون عما إذا كانت الأدوية الموجودة التي تُعيق الابتلاع يمكن أن تحاكي التجارب الوراثية. تُعرف فينوثيازينات، وهي عائلة من الأدوية المضادة للذهان ومضادة للغثيان، بأنها تثبط دينامين‑2 والامتصاص المعتمد على الكلاثرين للمستقبلات. في خلايا اللمفوما، رفعت مركبات مثل البروكلوربيرازين والكلوربرومازين مستويات BCR على السطح وقلّلت بشدة من الابتلاع الناتج عن المستضد. أدّى ذلك إلى انخفاض نشاط الجينات المدفوعة بواسطة NFκB وتراجع قابلية بقاء خلايا DLBCL من نوع ABC، لا سيما تلك التي تملك مكونات BCR سليمة. في فئران تحمل زراعات ليمفوما بشرية، بطّأ البروكلوربيرازين عند جرعات قابلة للتحقيق سريريًا نمو الورم بشكل ملحوظ. علاوة على ذلك، أنتجت مزامنة الفينوثيازينات مع أدوية تحجب إنزيمات مرتبطة بـBCR مثل SYK وPI3Kδ تأثيرات قتل سرطانية أقوى مما تحققه أي معالجة بمفردها.
ماذا قد يعني هذا للعلاج
بشكل عام، تُظهر الدراسة أنه لفرع كبير من حالات DLBCL، فإن الإشارات المحرِّكة للسرطان لا تنبع ببساطة من مستقبلات على سطح الخلية؛ بل تعتمد بشكل حاسم على سحب مركب BCR–المستضد إلى الداخل عبر مسار ابتلاع محدد. يقوّض تعطيل هذه الخطوة—إما بحيل جينية أو بأدوية فينوثيازين—إشارات NFκB ويضعف بقاء الخلايا الورمية، مع احتمال زيادة حساسية الخلايا لمثبطات مسار BCR القائمة. وبما أن فينوثيازينات لديها بالفعل جرعات وسلامة مفهومة جيدًا كأدوية مضادة للغثيان، فإن هذا العمل يوفر مخططًا واقعيًا للتجارب السريرية التي تختبرها منفردة أو بالاشتراك، لدى مرضى تظهر أورامهم نشاط BCR معتمدًا على مولدات الذات.
الاستشهاد: Górniak, P., Polak, A., Rams, A. et al. Inhibition of autoantigen-induced B-cell receptor (BCR) internalization as a therapeutic strategy in diffuse large B cell lymphoma (DLBCL). Cell Death Dis 17, 216 (2026). https://doi.org/10.1038/s41419-026-08446-1
الكلمات المفتاحية: لمفوما الخلايا البائية كبيرة الحجم المنتشرة, مستقبل الخلايا البائية, الابتلاع الخلوي, فينوثيازينات, إشارة NFkB