Clear Sky Science · ar
تحليل متعدد - أوميقي زمني لتعرّض الخلايا لباسليتاكسيل في خلايا عصبية حسية مشتقة من الخلايا الجذعية المحفزة البشرية يكشف آليات الاعتلال العصبي المحيطي الناجم عن العلاج الكيماوي
لماذا تسبب بعض أدوية السرطان ألماً للأعصاب
ساعدت العلاجات الكيماوية ملايين الأشخاص على النجاة من السرطان، لكن كثيراً من المرضى يدفعون ثمناً خفيّاً: شهوراً أو سنوات من الألم الحارق والوخز والخدر في اليدين والقدمين. تطرح هذه الدراسة سؤالاً بسيطاً لكنه مهمّاً: ماذا يفعل دواء السرطان واسع الاستخدام باسليتاكسيل بالضبط لخلايا الأعصاب الحسية البشرية، وهل يمكن أن يؤدي فهم تلك التغيرات إلى سبل أفضل للوقاية من هذا التلف العصبي وعلاجه؟
من خلايا المرضى إلى أعصاب حسية مُنموّة مخبرياً
بدلاً من الاعتماد على تجارب حيوانية، بدأ الباحثون بخلايا مأخوذة من خمسة متبرعين بشريين، بينهم مرضى سرطان الثدي الذين تلقوا باسليتاكسيل. أعادوا برمجة هذه الخلايا إلى خلايا جذعية محفّزة ثم وجهوها لتتحول إلى خلايا عصبية حسية—وهي نفس نوع الخلايا العصبية التي تنقل إشارات اللمس والألم من الجلد إلى الحبل الشوكي. شكّلت هذه الخلايا العصبية المُنموّة مخبرياً أليافاً طويلة وهشة وأظهرت نشاطاً كهربائياً يشبه إلى حد كبير أعصاب الإحساس بالألم الحقيقية في الجسم. ثم عرض الفريق هذه الخلايا لجرعات متزايدة من باسليتاكسيل، محاكيين مستويات الدواء التي تُرى لدى المرضى، وتتبعوا صحة الخلايا على مدى عدة أيام. عند تراكيز منخفضة تعايشت الخلايا العصبية جيداً، لكن عند جرعة ذات صلة سريرية (100 نانومول) بدأت قابليتها على البقاء بالانخفاض بعد حوالي يومين، ما يشير إلى بداية الضرر العصبي السام.
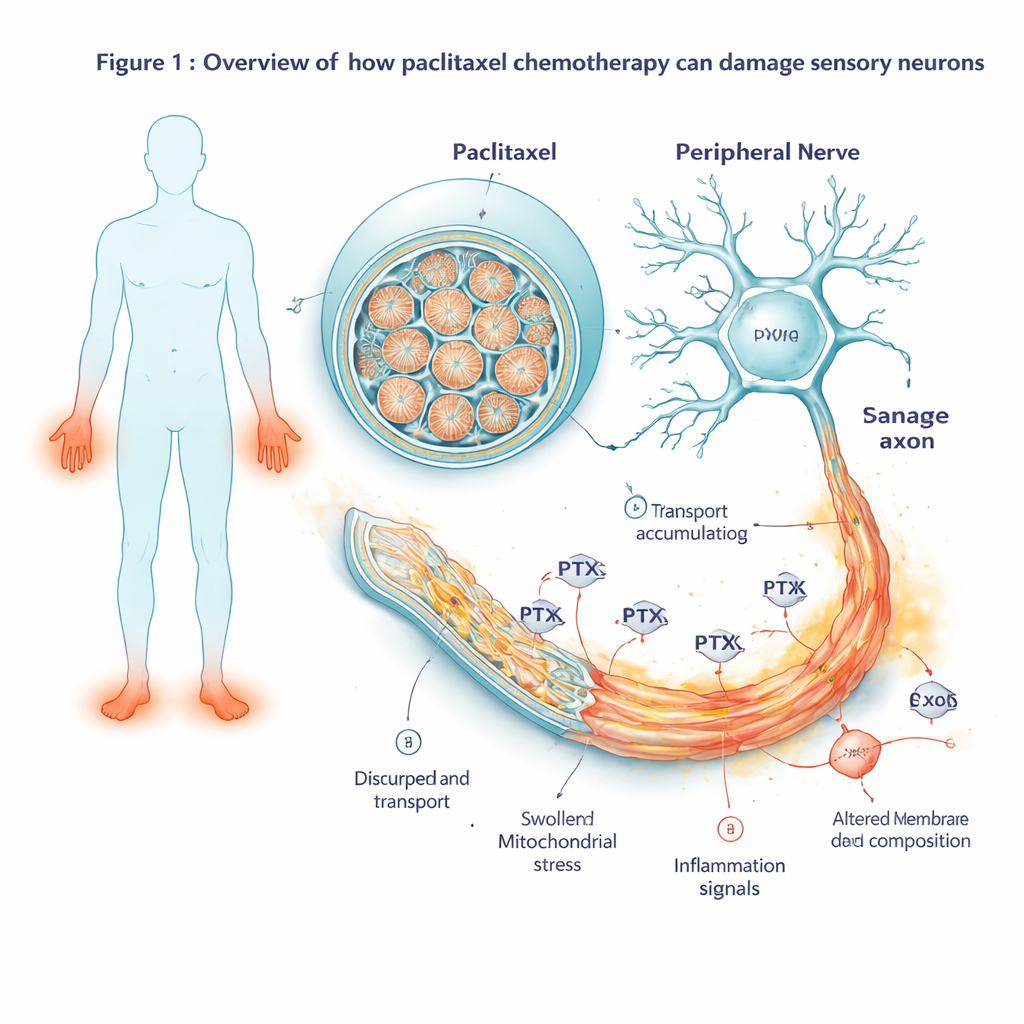
مراقبة تغيّر نشاط الجينات بمرور الوقت
لرؤية كيفية استجابة الخلايا قبل أن تتدهور ظاهرياً، قاس العلماء أي الجينات تُشغّل أو تُطفأ عند نقاط زمنية متعددة من ساعتين بعد التعرض للدواء إلى عدة أيام بعد غسل الدواء. في المراحل المبكرة لاحظوا تنشيط برنامج خلوي كلاسيكي مرتبط بالإجهاد يتركز حول جين يسمى JUN. مع استمرار التعرض، امتد هذا الإشارة الضاغطة إلى شلالة مدمرة ذاتيّاً: جينات تدفع الخلايا نحو الموت المبرمج اشتُغلت بقوة بينما غُمرت العوامل الوقائية. وفي الوقت نفسه أصبحت الجينات المرتبطة بالالتهاب وإشارات الألم أكثر نشاطاً. بدأت الخلايا العصبية في إنتاج رسائل التهابية أكثر، وببتيدات ومستقبلات مرتبطة بالألم تجعل الخلايا أكثر حساسية للمؤثرات الضارة—تغيّرات تعكس ما يُرى في اضطرابات الأعصاب المؤلمة.
نظرة معمقة على البروتينات والدهون داخل الخلايا العصبية
لأن الجينات ليست سوى مخططات، فحص الفريق أيضاً البروتينات الموجودة فعلياً في الخلايا العصبية بالإضافة إلى تركيبها الدهني. بعد 48 ساعة من التعرض لباسليتاكسيل ظهرت العديد من إشارات الإجهاد والالتهاب التي رُصدت على مستوى الرنا كزيادة في البروتينات أيضاً، مؤكدة أن الخلايا العصبية كانت تنفّذ هذه البرامج الضارة. ولافت للنظر أن البروتينات اللازمة للنقل المحوري—المحركات الجزيئية والهياكل التي تحرك الحمول على طول الألياف العصبية الطويلة—تقلصت بشكل حاد. شمل ذلك الكينيزينات وبروتينات تنظيمية تحافظ على استقرار مسارات الميكروتيوب. وعلى المستوى الدهني أظهرت الخلايا العصبية انخفاضاً في اللبنات الأساسية لصنع الكوليسترول وليبيدات الأغشية، إلى جانب ارتفاع في الدهون المخزنة المسماة ثلاثي الغليسريدات. تقترح هذه التحولات مجتمعة أن باسليتاكسيل لا يحفّز مسارات موت الخلايا فحسب، بل يضعف أيضاً البنية المادية وتوازن الطاقة في الألياف العصبية.
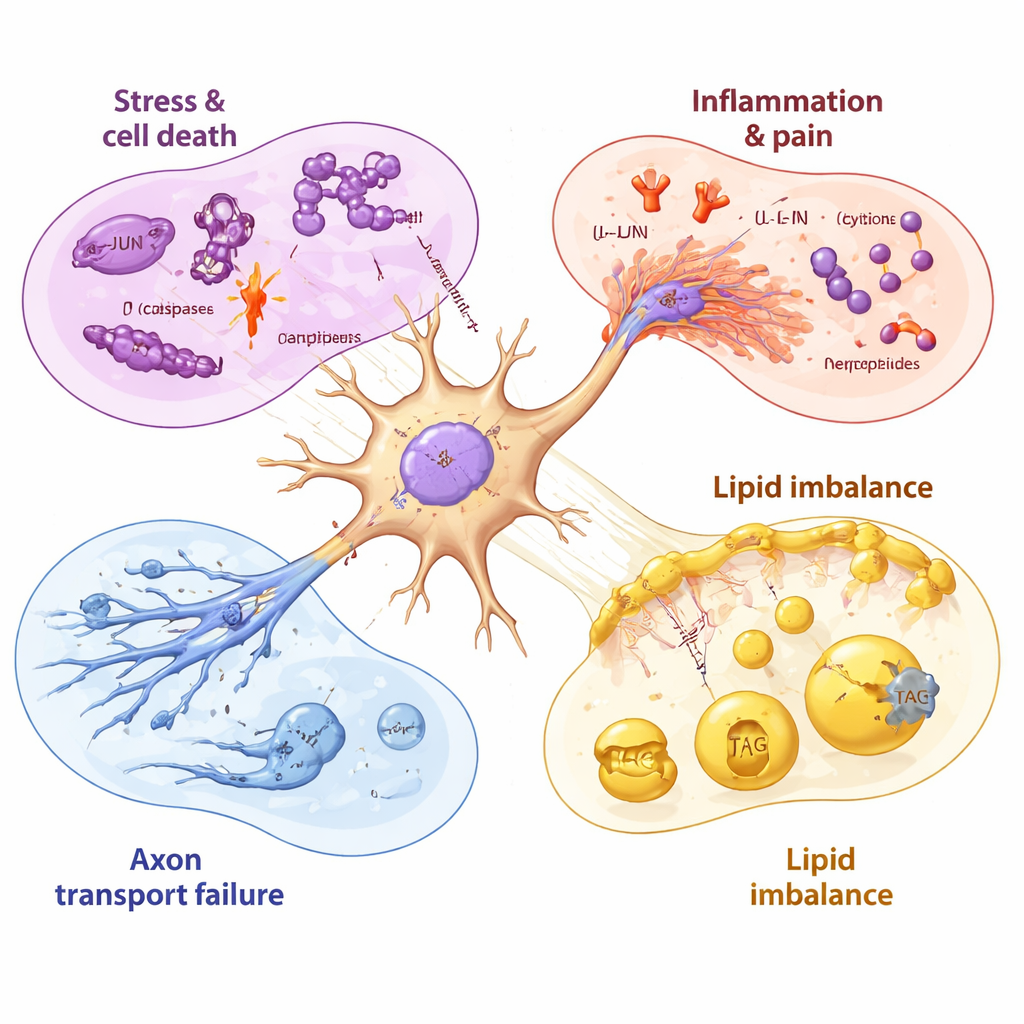
الخط الزمني للإصابة العصبية والتعافي غير الكامل
من خلال أخذ عينات من الخلايا العصبية قبل وأثناء وبعد التعرض للدواء، تمكن الباحثون من ترتيب هذه الأحداث زمنياً. تعطلّت جينات الميتوكوندريا (المتعلقة بالطاقة) خلال ساعات، تلاها جين الإجهاد JUN، ثم نشطت برامج أقوى للموت الخلوي والالتهاب مع بدء انخفاض قابلية الخلايا على البقاء. حتى بعد إزالة باسليتاكسيل، ظلت العديد من الإشارات الضارة مرتفعة لأيام، في حين استمرت الجينات اللازمة لصنع ليبيدات غشائية صحية في التراجع. بعض الجزيئات التي ارتفعت متأخراً، مثل مضخّة طرد الدواء التي قد تطرد باسليتاكسيل وبعض عوامل النمو، لمّحت إلى محاولة الخلايا العصبية الحماية وإصلاح نفسها—لكن بدت هذه الاستجابات بطيئة وغير كاملة نسبياً مقارنة بالدفع المبكر والسريع نحو التلف.
ماذا يعني هذا للمرضى الذين يعيشون مع ألم عصبي
بالنسبة للقارئ العام، الرسالة هي أن باسليتاكسيل يضر الخلايا العصبية الحسية عبر سلسلة من الضربات الممنهجة: يجهد أنظمتها الطاقية، يبدّل مفاتيح جينية نحو موت الخلايا، يثير الالتهاب وإشارات الألم، يربك "الطرق النقلية" الداخلية داخل الألياف العصبية، ويغيّر الدهون التي تحافظ على استقرار أغشية الأعصاب. من خلال رسم هذه التغيرات في خلايا عصبية مشتقة من البشر بتفصيل دقيق، تبرز الدراسة أهدافاً ملموسة قابلة للعلاج—مثل منظمات الضغط الخلوية المحددة، ومستقبلات الالتهاب، وإنزيمات صنع الدهون—يمكن حجبها أو دعمها لحماية الأعصاب دون إضعاف العلاج من السرطان. وبينما ستتطلب العلاجات الجديدة اختبارات إضافية، يقدم هذا العمل خارطة طريق أوضح للوقاية أو التخفيف من تلف الأعصاب الناجم عن العلاج الكيماوي، مما يحسّن جودة الحياة لدى الناجين من السرطان.
الاستشهاد: Schinke, C., Maierhof, S.K., Hew, L. et al. Time‑resolved multi-omic analysis of paclitaxel exposure in human iPSC‑derived sensory neurons unveils mechanisms of chemotherapy‑induced peripheral neuropathy. Cell Death Dis 17, 211 (2026). https://doi.org/10.1038/s41419-026-08445-2
الكلمات المفتاحية: الاعتلال العصبي المحيطي الناجم عن العلاج الكيماوي, باسليتاكسيل, الخلايا العصبية الحسية, الالتهاب العصبي, انحلال المحور العصبي