Clear Sky Science · ar
تعديل ميثلة الأرجينين القابل للعكس ينظم نشاط IDH2 الميتوكوندري: تحكم منسق بواسطة CARM1 وKDM3A/4A
ضبط دقيق لمصانع الطاقة الخلوية
تقوم الميتوكوندريا، التي تُسمى غالبًا مصانع الطاقة في خلايانا، بأدوار تفوق إنتاج الطاقة فقط. فهي تضبط باستمرار كيفية استهلاك الوقود لتلبية احتياجات الجسم، وعندما يختل هذا التوازن يمكن أن يساهم في أمراض مثل السكري وفشل القلب والسرطان. تكشف هذه الدراسة عن «مفتاح تعتيم» خفي داخل الميتوكوندريا: وسم كيميائي صغير على بُنى أساسية في إنزيم رئيسي، IDH2، يساعد في تقرير ما إذا كانت الميتوكوندريا تعمل بمعدل منخفض أم ترفع إنتاجها من الطاقة.
وسم صغير بعواقب كبيرة
البروتينات في خلايانا ليست جامدة؛ تُعدَّل كثيرًا بمجموعة من الوحدات الكيميائية الصغيرة التي تغيّر سلوكها. وبينما تُعرف العديد من هذه التعديلات في نواة الخلية والسيتوبلازما جيدًا، فإن التعديلات داخل الميتوكوندريا أقل استكشافًا. ركز الباحثون على نوع محدد من الوسوم يُدعى ميثلة الأرجينين وتساءلوا عما إذا كان يمكن أن يتحكم في عمل إنزيمات الميتوكوندريا. وجّهوا اهتمامهم إلى إنزيم يُدعى IDH2، وهو عنصر فعال في دورة حمض الستريك (TCA)، يساعد في تحويل المغذيات إلى طاقة ولبنات بناء أيضية مهمة. باستخدام أدوات بيوكيميائية وقياس الطيف بالكتلة، وجدوا أن IDH2 يحمل علامة ميثلة محددة على حمض أميني واحد، الأرجينين رقم 188، وأن هذه العلامة توضع بواسطة إنزيم يُدعى CARM1 يعمل، على نحو مفاجئ، داخل الميتوكوندريا.
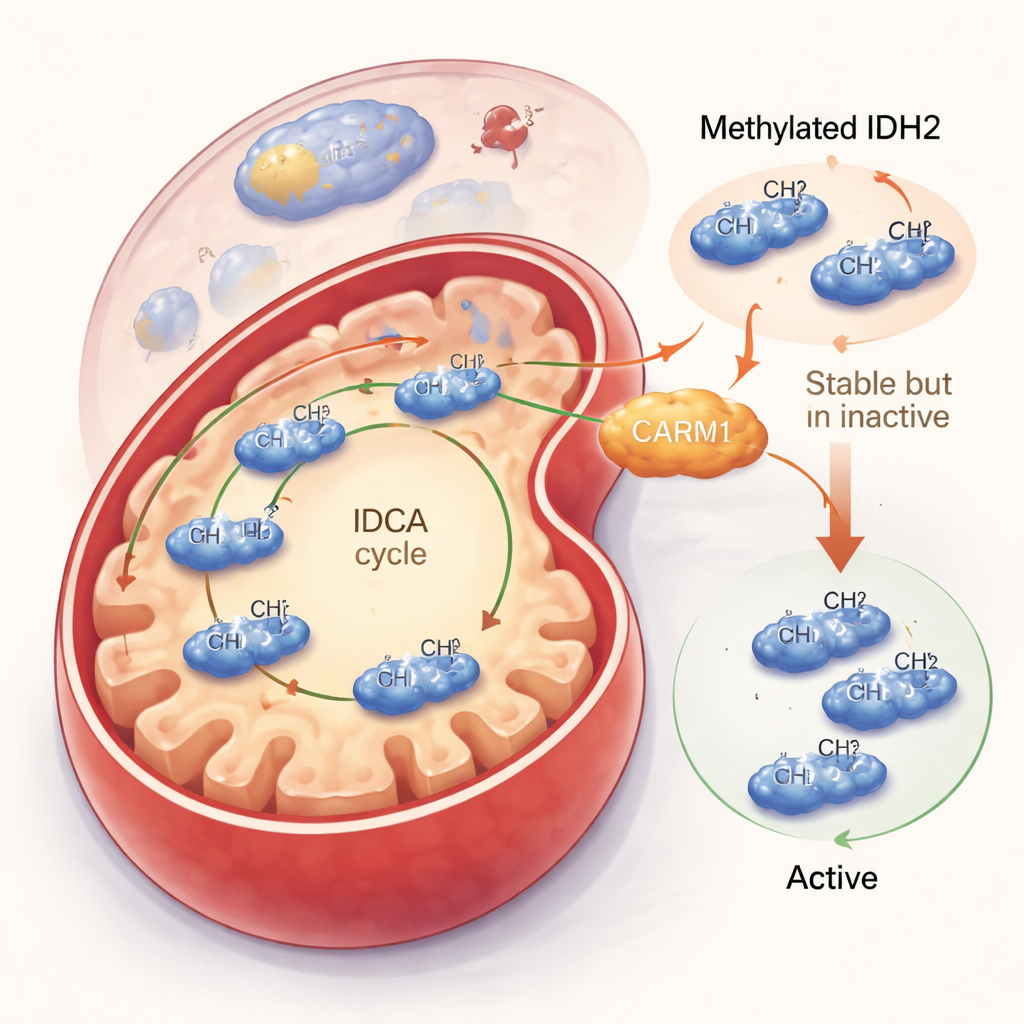
خفض نشاط IDH2 مع إطالته في العمر
سأل الفريق بعد ذلك عما تفعله هذه الميثلة فعليًا. عندما كان CARM1 نشطًا وقادرًا على مثيلة IDH2، أصبح بروتين IDH2 أكثر استقرارًا وبقي لفترة أطول داخل الخلية. لكن هذه الميزة صاحَبَتها مقايضة: كان IDH2 المثيّل أقل نشاطًا. في تجارب خلوية وعلى بروتين منزوع وعاء، أنتج IDH2 المثيّل كميات أقل من ناتجه الرئيسي، ألفا-كيتوغلوتارات، وولّد أقل من الجزيء الوقائي NADPH. بالمقابل، شكلت نسخة من IDH2 لا يمكن مثيلتها عند الأرجينين 188 شكل ثنائي أكثر نشاطًا، عملت بسرعة أكبر، وعزّزت مستويات كل من ألفا-كيتوغلوتارات وNADPH. وحتى مع وجود كمية إجمالية أقل من هذا IDH2 غير المثيَل، كانت كل جزيئة تقوم بعمل أكبر، مما أدى إلى زيادة صافية في إنتاج الميتوكوندريا.
مفتاح قابل للعكس مع ممحوتين
وبشكل جوهري، ليست هذه العلامة الميثيلية دائمة. أظهر الباحثون أن إنزيمين يُعرفان عادة بإزالة نوع آخر من الوسوم—مزيلات مثيلة الليسين KDM3A وKDM4A—يمكنهما أيضًا محو علامة ميثلة الأرجينين من IDH2. عندما وُجدت هذه المزيلات، فقد الأرجينين عند الموضع 188 مجموعاته الكيميائية الإضافية، فأصبح IDH2 أقل استقرارًا لكنه أكثر نشاطًا، وزاد الشكل الثنائي له. أظهرت الخلايا ذات مستويات أعلى من KDM3A أو KDM4A جهد غشاء ميتوكوندري أعلى واستهلاكًا أكبر للأكسجين، علامات تشير إلى أن ميتوكوندرياتها تعمل بطاقة أكسيدية أعلى. وعندما انخفضت مستويات هذه الإنزيمات، حدث العكس: تراجعت نشاطات IDH2 وأداء الميتوكوندريا، مما يؤكد أن هذه آلية تحكم قابلة للعكس وليست تغييرًا أحادي الاتجاه.
ربط الأيض بالمرض
نظرًا لارتباط IDH2 بالسرطان واضطرابات أخرى، فحص المؤلفون كيف يمكن أن تكون لهذه المفاتيح الميثيلية أهمية في حالات شبيهة بالمرض. في خطوط خلوية طبيعية ومسرطنة مختلفة، لاحظوا أن المستويات الأعلى من بروتين IDH2 غالبًا ما صاحَبها مزيد من المثيلة ونشاط إنزيمي أقل بشكل مفاجئ، مما يشير إلى أن «المزيد من البروتين» لا يعني دائمًا «المزيد من الوظيفة». في مجموعات بيانات سرطان الثدي، كان المرضى ذوو مستويات بروتين IDH2 الأعلى يميلون إلى بقاء أسوأ، رغم أن نشاط جين IDH2 لم يتتبع هذه النتيجة. تدعم النتائج نموذجًا تقضي فيه مثيلة يقودها CARM1 بإبطاء دورة TCA وتوجيه الخلايا نحو طرق بديلة مفضلة في السرطان لاستخدام المغذيات، في حين يمكن لمزيلات الميثلة مثل KDM3A وKDM4A دفع الخلايا مرة أخرى نحو إنتاج طاقة أكثر كفاءة.
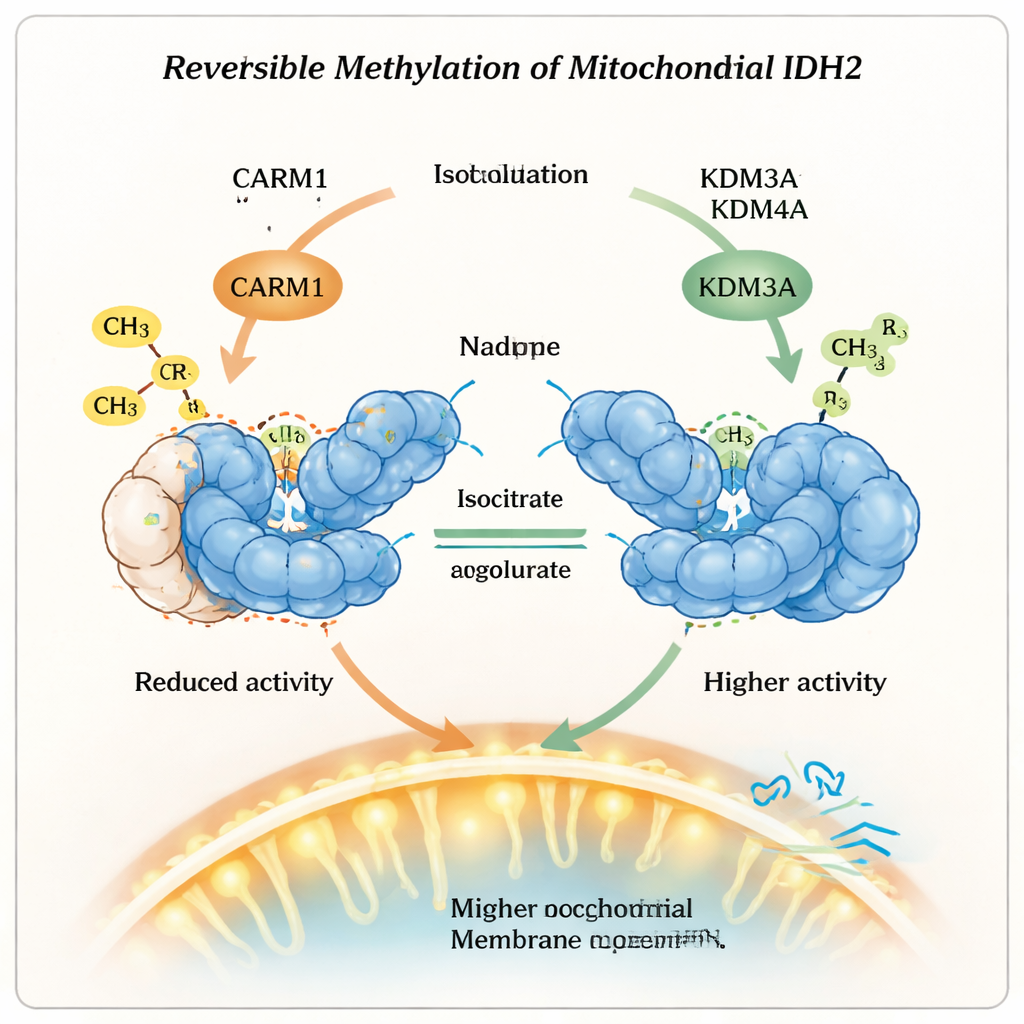
ماذا يعني هذا للصحة والعلاج
بعبارة بسيطة، تبين هذه الدراسة أن الميتوكوندريا لا تكتفي بتشغيل الإنزيمات أو إيقافها، بل تستخدم وسوما كيميائية قابلة للعكس كأقراص تحكم دقيقة. بإضافة مجموعة ميثيل، يجعل CARM1 IDH2 أطول عمرًا ولكن أقل نشاطًا؛ وبإزالة تلك العلامة، تتخلى KDM3A وKDM4A عن بعض الاستقرار لكسب إنتاجية أعلى. يؤثر هذا التوازن في كيفية اختيار الخلايا بين احتراق الجلوكوز السريع لكن غير الكفوء والطريقة الأبطأ والأكثر كفاءة لإنتاج الطاقة. إن فهم هذا «مفتاح التعتيم» الميثيلي على IDH2 يفتح إمكانيات علاجية جديدة تهدف إلى تصحيح أخطاء الأيض الميتوكوندري في حالات مثل السرطان والاضطرابات الأيضية، من خلال استهداف الإنزيمات التي تضع وتمحو هذه الوسوم الصغيرة لكنها القوية.
الاستشهاد: Cho, Y., Winarto, J., Song, DG. et al. Reversible arginine methylation regulates mitochondrial IDH2 activity: coordinated control by CARM1 and KDM3A/4A. Cell Death Dis 17, 195 (2026). https://doi.org/10.1038/s41419-026-08444-3
الكلمات المفتاحية: الميتوكوندريا, IDH2, ميثلة الأرجينين, الأيض الخلوي, CARM1