Clear Sky Science · ar
الهونوكول يوقف تطور الأورام والانتقال عن طريق تأثيرات موجهة إلى الميتوكوندريا
تحويل مركب شجري إلى مقاتل للسرطان
ينبع العديد من أدوية السرطان من النباتات، ولا يزال العلماء يكشفون كيف تعمل بعض هذه الجزيئات الطبيعية داخل خلايانا. تركز هذه الدراسة على الهونوكول، مادة موجودة في لحاء شجرة الماغنوليا والتي استخدمت طويلاً في الطب التقليدي، وتُظهر كيف يمكن لها استهداف المصانع الصغيرة للطاقة داخل خلايا السرطان مباشرةً لإبطاء نمو الورم ومنع الانتشار، مع الحفاظ إلى حد كبير على سلامة الخلايا الطبيعية.
محطات الطاقة داخل خلايانا
تعتمد كل خلية على الميتوكوندريا، التي غالباً ما تُسمى «محطات الطاقة» في الخلية، لتوليد جزيء الطاقة ATP. في السرطان، تقوم الميتوكوندريا بأكثر من إنتاج الوقود—فهي تساعد في تقرير ما إذا كانت الخلية ستبقى حية أم تموت. يوجد جهاز جزيئي كبير واحد، إنزيم تخليق ATP، في الغشاء الداخلي للميتوكوندريا ويصنع ATP. غالباً ما تُنتج الخلايا السرطانية بكميات زائدة بروتين شريك يُدعى IF1 الذي يلتصق بإنزيم تخليق ATP ويعمل كقفل أمان، مما يساعد الأورام على مقاومة شكل من أشكال الانتحار الخلوي المعروف بالانتقال النفاذي الميتوكوندري والموت الخلوي اللاحق.
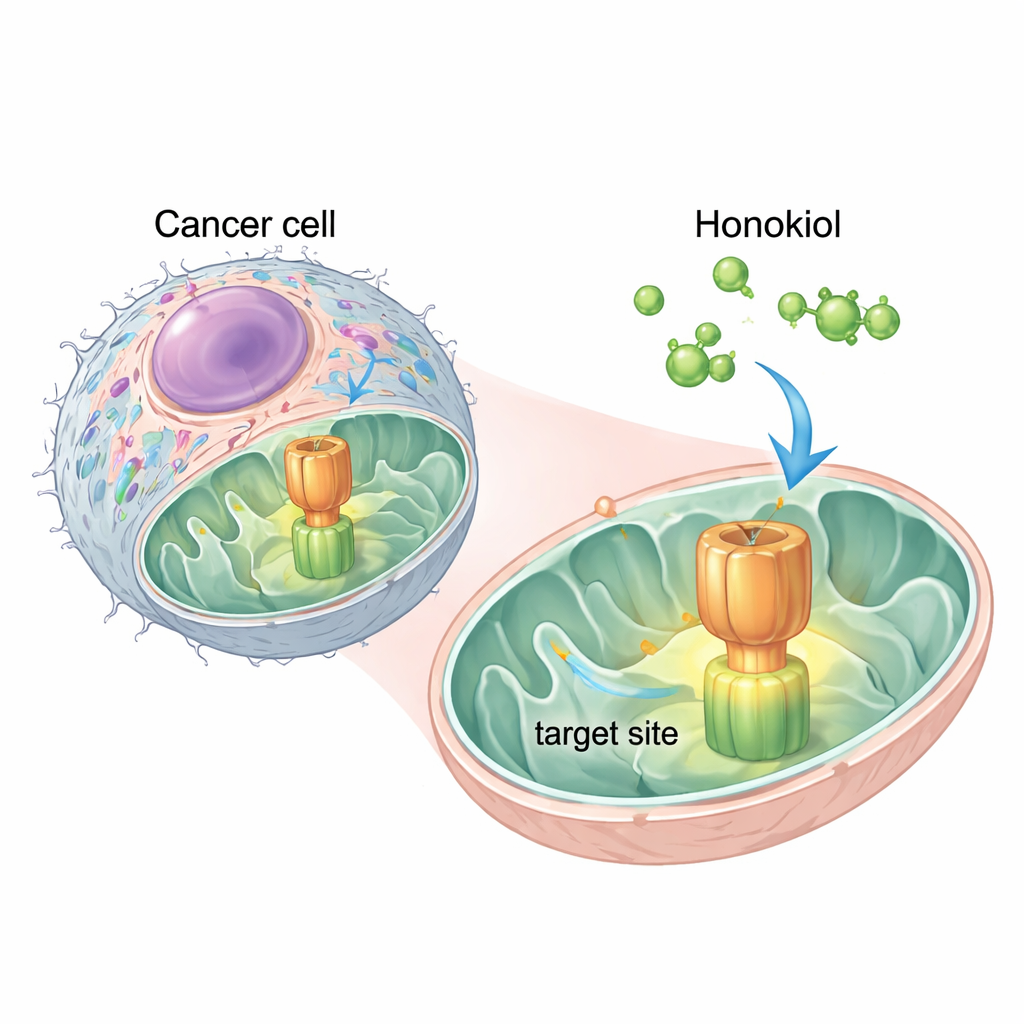
جزيء طبيعي يجد مفتاحاً حاسماً
استخدم الباحثون محاكاة حاسوبية لمعرفة أين قد يرتبط الهونوكول على إنزيم تخليق ATP. وجدوا موقعين واعدين للربط على أحد مكوناته، منطقة تُدعى OSCP. تغلّب أقوى موقع تراكباً مع نفس الرقعة التي يستخدمها IF1 للالتصاق بإنزيم تخليق ATP. هذا اقترح أن الهونوكول قد يعمل كوتد جزيئي، يندفع داخل OSCP ويدفع IF1 بعيداً. أكدت تجارب على خلايا هيلا البشرية لسرطان عنق الرحم هذه الفكرة: إذ خفض إضافة الهونوكول الاتصال الفيزيائي بين IF1 وOSCP، دون تعطيل أجزاء أخرى من الإنزيم، مما أظهر أن التأثير كان محدداً.
من الخلايا إلى الحيوانات الحية: أورام أقل، وانتشار أقل
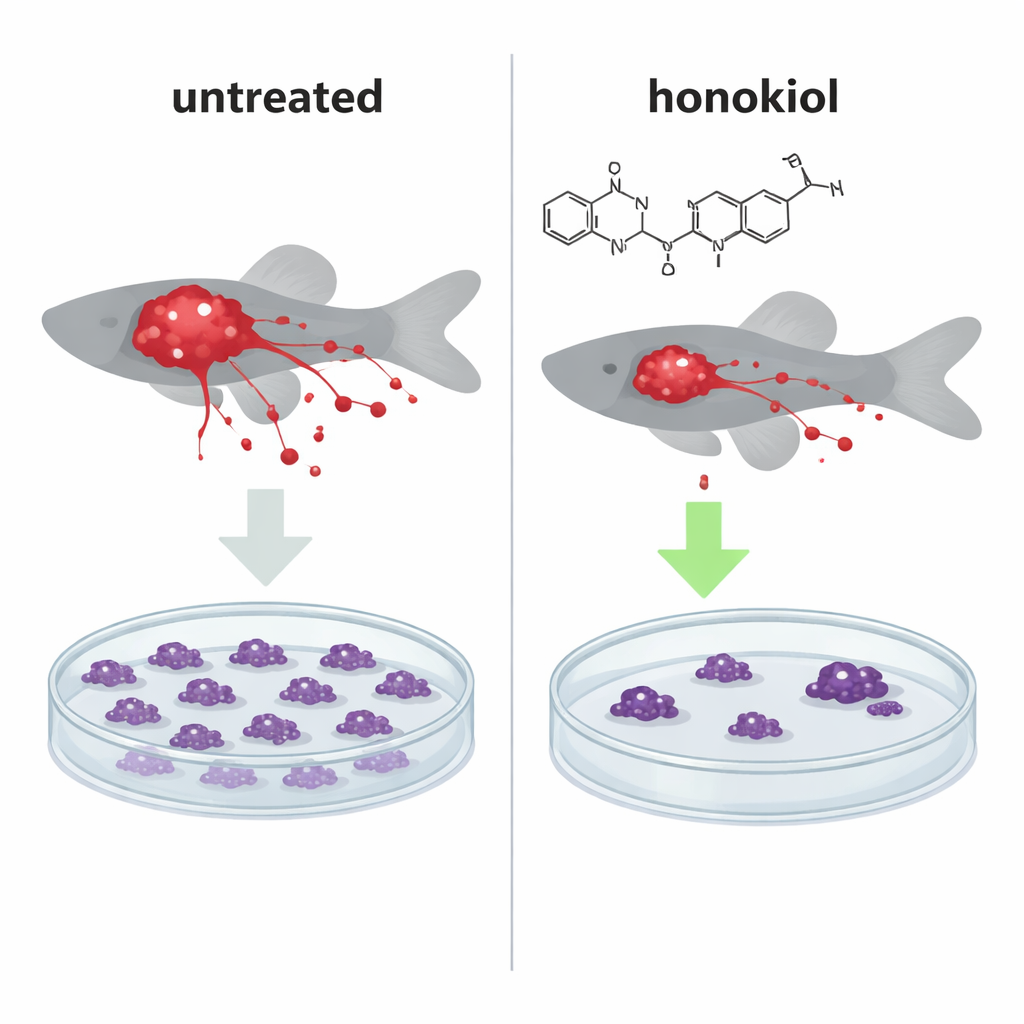
لمعرفة ما إذا كان هذا الدفع الجزيئي له تأثير في العالم الواقعي، زرع الفريق خلايا سرطانية بشرية متوهجة في أجنة زراعة السمك الزيبرا الصغيرة، وهو نموذج حيواني معتمد لتتبع نمو الورم والانتقال النقيلي. في الأسماك التي حُقنت بخلايا هيلا الغنية بـIF1، أدى علاج الهونوكول إلى انكماش الكتل الورمية بشكل ملحوظ وتقليل عدد الخلايا السرطانية التي انتشرت إلى مناطق بعيدة، مما جعل النمط يشبه الأسماك المحقونة بخلايا تعاني من حذف IF1 التي تفتقد البروتين الحامي. ومن المثير للاهتمام أن الهونوكول خفض أيضاً عدد الخلايا المنتقلة حتى عندما غاب IF1، مما يشير إلى آلية ثانية للحد من الانتقال تعتمد على شيء مستقل عن IF1.
إجبار محطات طاقة معطلة على تفعيل الانتحار الذاتي
في أطباق المختبر، خفض الهونوكول قدرة خلايا السرطان على تشكيل مستعمرات كبيرة في أغار لينين ناعم، وهو اختبار يحاكي ظروف الإجهاد وانخفاض الأكسجين داخل الأورام الصلبة. حدث هذا دون تباطؤ كبير في الانقسام الخلوي العادي أو في التنفس الميتوكوندري الأساسي، مما يشير بدلاً من ذلك إلى تغير في كيفية اتخاذ الميتوكوندريا قرار الحياة أو الموت. أظهرت قياسات التعامل مع الكالسيوم أن الهونوكول جعل الميتوكوندريا تفتح المسام النفاذية الانتقالية عند مستويات كالسيوم أقل، وهو محفز معروف للانتفاخ وإطلاق عوامل تعزيز الموت. عند جرعات معتدلة اعتمد هذا التأثير على إزاحة IF1؛ أما عند جرعات أعلى فعمل الهونوكول عبر موقع الربط الثاني على OSCP ومن خلال زيادة أنواع الأكسجين التفاعلية، ما جعل حتى الخلايا التي تفتقر إلى IF1 حساسة للموت المبرمج.
إيقاف خلايا السرطان عن الحركة
يصبح السرطان أخطر عندما تفصل الخلايا وتهاجر إلى أعضاء جديدة. في اختبارات الخدش الشبيهة بالجروح، أبطأ الهونوكول بشدة هجرة صفائح الخلايا السرطانية بشكل جماعي وخفض مؤشرات الانتقال الظهاري-ال mezenchymal، وهي عملية تزود خلايا الورم بالقدرة على الحركة والغزو. كشفت صور مجهر إلكتروني مفصلة أن الخلايا المهاجرة عادةً ما تكبر وتعيد تشكيل ميتوكوندرياتها، مضيفة طيات داخلية لتلبية متطلبات الطاقة العالية عند الحافة الأمامية. مع الهونوكول، أصبحت هذه الميتوكوندريا المتقدمة منتفخة وتعرضت لضرر هيكلي—علامات لفتح المسام النفاذية الانتقالية—بينما كانت ميتوكوندريا المناطق غير المتحركة أقل تعرضاً أو حتى زادت في العدد، اعتماداً على وجود IF1.
ماذا يعني هذا لعلاجات السرطان في المستقبل
ببساطة، تُظهر هذه الدراسة أن الهونوكول يمكنه التركيز على منطقة تنظيمية صغيرة في آلة إنتاج ATP الميتوكوندرية وقلب مفتاح أمان مدمج غالباً ما تبقيه الخلايا السرطانية مقفلاً. من خلال إزاحة IF1 ودفع المسام نحو الفتح مباشرةً، يشجع الهونوكول خلايا الورم على الانتحار الذاتي ويجعل من الصعب عليها الهجرة وبذر النقائل. ونظراً لأن هذه التأثيرات تنبع من خصائص يتشاركها العديد من الأورام—بدلاً من علامة سطحية واحدة—قد يلهم استهداف منطقة OSCP من إنزيم تخليق ATP فئة جديدة من العلاجات التي تستغل نقاط ضعف محطات طاقة الخلايا السرطانية مع الحد من الأذى للأنسجة الصحية.
الاستشهاد: Grandi, M., Boldrin, F., Risato, G. et al. Honokiol blocks tumor development and metastasis through mitochondrion-targeted effects. Cell Death Dis 17, 186 (2026). https://doi.org/10.1038/s41419-026-08441-6
الكلمات المفتاحية: هونوكول, الميتوكوندريا, إنزيم تخليق ATP, الانتحار الخلوي (الاستماتة), الانتقال النقيلي