Clear Sky Science · ar
يتعاون KDM5B مع مركب CRL4B لتعزيز تكون الأورام في سرطان الثدي إيجابي مستقبلات الإستروجين عبر تنظيم أيض الكوليسترول
لماذا تهم هذه الدراسة الصحة اليومية
سرطان الثدي هو أكثر أنواع السرطان شيوعًا بين النساء، والعديد من الأورام تنمو استجابة لهرمون الإستروجين. هذه الأنواع من السرطانات لا تكتفي بالتكاثر السريع فحسب — بل تعيد أيضًا برمجة طريقة استخدامها للدهون مثل الكوليسترول. تكشف هذه الدراسة كيف أن بروتينًا منظمًا للجينات يُسمى KDM5B يتعاون مع مركب بروتيني آخر، CRL4B، لزيادة مستويات الكوليسترول داخل خلايا سرطان الثدي الإيجابية لمستقبلات الإستروجين (ER+). من خلال فهم هذه الشراكة الخفية، يأمل العلماء في إيجاد طرق جديدة لإبطاء نمو الأورام وتحسين العلاجات القائمة مثل العلاج الهرموني والأدوية الخافضة للكوليسترول.
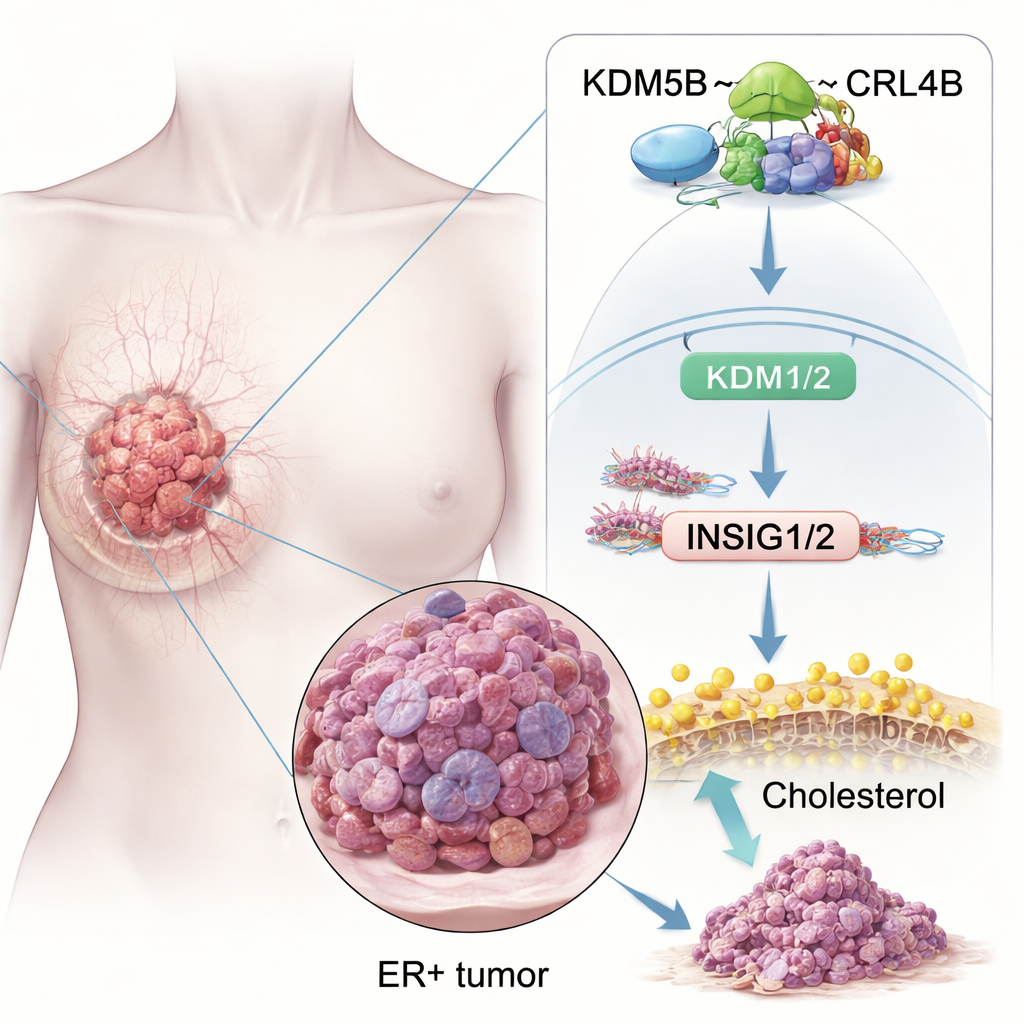
بروتين يميل الميزان نحو السرطان
سأل الباحثون أولًا ما إذا كان وجود KDM5B في سرطانات الثدي الإيجابية لمستقبلات الإستروجين مجرد حضور أم أنه يسهم في قيادتها بالفعل. من خلال تحليل قواعد بيانات سرطانية واسعة وعينات نسيجية، وجدوا أن مستويات KDM5B أعلى في أورام الثدي مقارنة بالنسيج الثديي الطبيعي، وتكون مرتفعة بشكل خاص في الأورام الإيجابية لمستقبلات الإستروجين. المرضى الذين تنتج أورامهم مستويات أعلى من KDM5B يميلون إلى الحصول على نتائج بقاء أسوأ، حتى عند تلقيهم العلاج الكيميائي القياسي أو العلاج الهرموني. في تجارب الخلايا في المختبر، أدت زيادة KDM5B إلى تسريع نمو خلايا سرطان الثدي ER+، وزيادة قدرتها على غزو الأنسجة المحيطة وتشكيل تجمعات أشبه بالخلايا الجذعية، والتي يُعتقد أنها تؤسس أورامًا جديدة. أما خفض KDM5B فكان له التأثير المعاكس، حيث تقلصت المستعمرات في الأطباق والأورام في الفئران.
شراكة قوية داخل الخلايا السرطانية
لمعرفة كيف يمارس KDM5B هذه التأثيرات، بحث الفريق عن شركائه البروتينيين. اكتشفوا أن KDM5B يرتبط فعليًا بأجزاء من آلة جزيئية تُسمى مركب CRL4B، وهو نظام إنزيمي يعلّم البروتينات ويتدخل أيضًا في كيفية تعبئة الحمض النووي. أظهرت اختبارات بيوكيميائية مفصلة أن KDM5B يتفاعل مباشرة مع مكونين من CRL4B، هما CUL4B وDDB1، عبر مناطق محددة في كل بروتين. في خلايا سرطان الثدي ER+، يعمل مركب KDM5B–CRL4B على العديد من الجينات عند مفاتيح تشغيلها/إيقافها. باستخدام رسم خرائط على مستوى الجينوم، وجد المؤلفون أن KDM5B وCUL4B غالبًا ما يتواجدان معًا عند محفزات الجينات، حيث يغيران العلامات الكيميائية على بروتينات الهيستون — البكرات التي يلتف حولها الحمض النووي — لكتم التعبير الجيني.
رفع فرامل الكوليسترول
من بين المسارات المتأثرة، برز أيض الكوليسترول. تحتاج الخلايا السرطانية إلى كوليسترول إضافي لبناء الأغشية ومقاومة الإجهاد، وتستخدم الأورام ER+ أيضًا جزيئات مشتقة من الكوليسترول لتقليد تأثير الإستروجين. تُظهر الدراسة أن مركب KDM5B–CRL4B يرتبط مباشرة بمناطق التحكم في جينين رئيسيين يعملان كـ«فرامل»، هما INSIG1 وINSIG2. هذه الجينات عادةً تساعد في إبقاء منظم رئيسي للكوليسترول، SREBP2، تحت السيطرة. يضيف مركب KDM5B–CRL4B علامة كبح (H2AK119ub1) ويزيل علامة تنشيط (H3K4me3) على الهيستونات عند محفزات INSIG1/2، مما يخفض نشاط هذه الجينات. مع انخفاض بروتينات INSIG1/2، يتحرر SREBP2 ليشغّل جينات تصنيع الكوليسترول، ما يرفع مستويات الكوليسترول داخل خلايا سرطان الثدي ER+ ويعزز سلوكها الغازي. عندما عطل الباحثون KDM5B أو CRL4B، ارتفعت INSIG1/2، انخفض نشاط SREBP2، وتراجع إجمالي الكوليسترول داخل الخلايا.
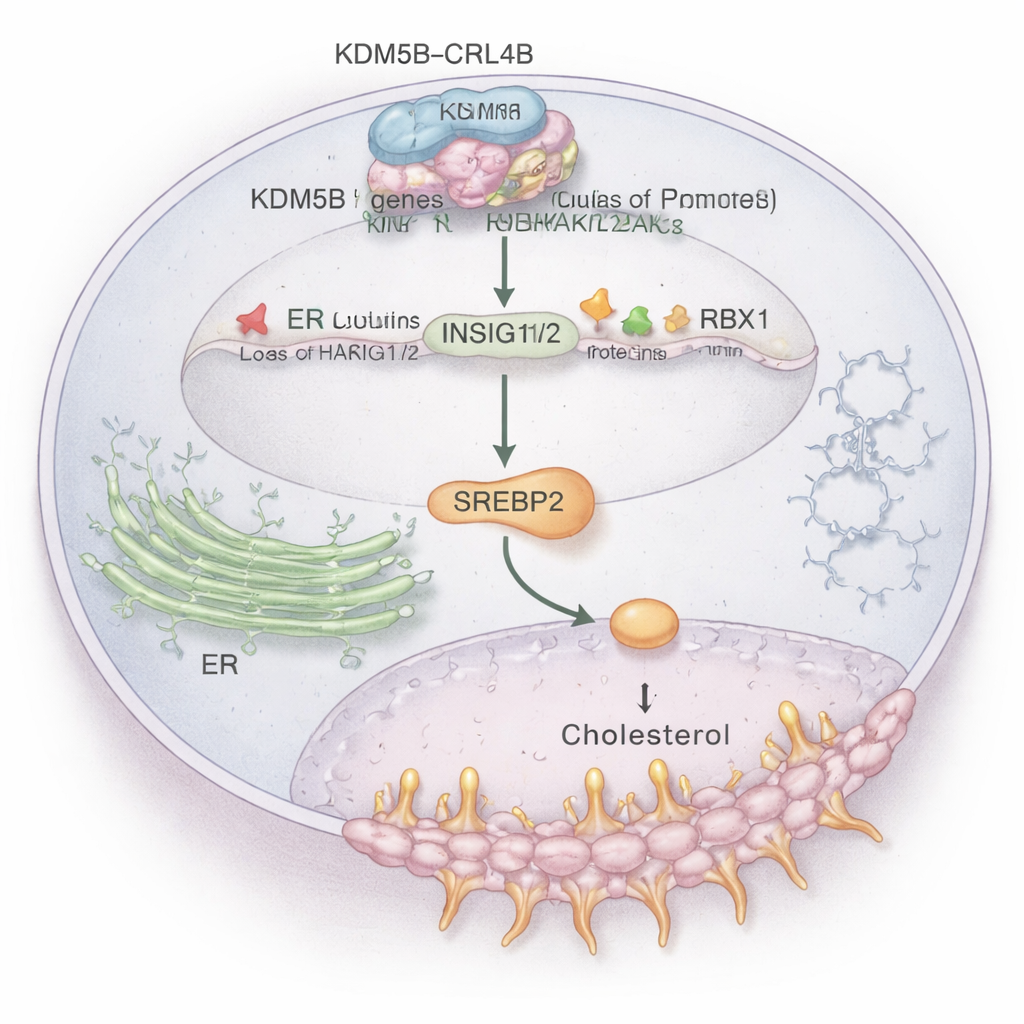
التقاطع بين أدوية الكوليسترول وإشارات السرطان
تربط الدراسة أيضًا هذا المسار بإشارة مشتقة من الكوليسترول تُدعى 27‑هيدروكسيكوليسترول (27‑HC)، وهو جزيء معروف بالفعل بتعزيز سرطان الثدي ER+. أدى معالجة خلايا ER+ بـ27‑HC إلى زيادة مستويات KDM5B ومزيد من قمع INSIG1/2، مما دفع الخلايا نحو مزيد من النمو والغزو. والأهم أن تعطيل KDM5B أو CRL4B قلل من هذه التأثيرات العدوانية، مما يشير إلى أن 27‑HC يعمل جزئيًا عبر تعزيز محور KDM5B–CRL4B. بشكل منفصل، أظهر الباحثون أن السيمفاستاتين، الستاتين واسع الاستخدام لخفض الكوليسترول، أبطأ نمو خلايا سرطان الثدي، وعند الجمع بينه وبين مثبط لـKDM5B، كان التأثير المضاد للورم أقوى. هذا يشير إلى أن الجمع بين أدوية تستهدف إنتاج الكوليسترول وأدوية تعيق نشاط KDM5B في التحكم الجيني قد يكون استراتيجية علاجية واعدة.
ما معنى هذا للمرضى والعلاجات المستقبلية
تكشف هذه الدراسة عن سلسلة جديدة من الأحداث داخل خلايا سرطان الثدي ER+: إشارة متعلقة بالكوليسترول (27‑HC) تزيد KDM5B؛ يتعاون KDM5B مع مركب CRL4B لإغلاق INSIG1 وINSIG2؛ يطلق ذلك SREBP2، ويعزز إنتاج الكوليسترول، ويساعد الأورام على النمو والغزو والحفاظ على خصائص شبيهة بالخلايا الجذعية. وبما أن KDM5B أيضًا مرتفع ومرتبط بسوء البقاء في عدة سرطانات أخرى، فقد يوفر تعطيل هذا البروتين — أو استعادة فرامل INSIG1/2 — طرقًا جديدة للتحكم في نمو الأورام. وبينما يلزم المزيد من العمل قبل أن تُترجم هذه النتائج إلى رعاية روتينية، تبرز النتائج مدى ارتباط سلوك السرطان بجزيئات يومية مثل الكوليسترول، وكيف يمكن أن تُستخدم أدوية موجودة مثل الستاتينات مستقبلًا بالاقتران مع علاجات إبجينيتيكية لتحسين النتائج.
الاستشهاد: Yang, Y., Gao, T., Yuan, B. et al. KDM5B cooperates with CRL4B complex to promote the tumorigenesis of ER+ breast cancer via regulating cholesterol metabolism. Cell Death Dis 17, 207 (2026). https://doi.org/10.1038/s41419-026-08438-1
الكلمات المفتاحية: سرطان الثدي إيجابي المستقبلات الإستروجينية, أيض الكوليسترول, KDM5B, INSIG1/INSIG2, العلاج اللاجيني (ابيجينيتيكي)