Clear Sky Science · ar
تحوُّر TDP-43 يسبب اختلالات في النقل المحوري والتحلل السكري في نموذج خلية جذعية لفأر للخلايا العصبية الحركية لمرض التصلب الجانبي الضموري (ALS)
لماذا يهم هذا البحث مرضى التصلب الجانبي الضموري
التصلب الجانبي الضموري (ALS) هو مرض قاتل يسبب شللاً تدريجياً من خلال قتل الخلايا العصبية التي تتحكم في العضلات. يظهر لدى معظم المرضى تلف مرتبط ببروتين يُدعى TDP-43، ولكن العلماء لم يفهموا بالكامل كيف يسبب هذا التلف ضرراً للخلايا العصبية الحركية. تستخدم هذه الدراسة نموذج خلايا جذعية مستخرج من فأر، مصمم بعناية، لتحديد بعض أقدم المشكلات التي يتسبب بها شكل منقوص الصِّلة من TDP-43 المرتبط بالمرض، مقدِّمة أدلة قد تُوجه تطوير علاجات مستقبلية.
بناء خلايا عصبية حركية في طبق
لاستكشاف ALS في بيئة مسيطَر عليها، بدأ الباحثون بخلايا جذعية جنينية فأرية وحثّوها على التحول إلى خلايا عصبية حركية، وهي الخلايا الطويلة الشبيهة بالكابلات التي تنقل الإشارات من الحبل الشوكي إلى العضلات. أدخلوا نسخة إضافية واحدة من جين الإنسان لـTDP-43 في هذه الخلايا، إما بصيغته الطبيعية أو حاملة لطفرة مرتبطة بالـALS تسمى M337V. أتاح وسم فلوري للفريق تتبُّع البروتين البشري داخل الخلايا. بحلول اليوم العشرين في الثقافة، نضجت كل من الخلايا الطبيعية والمتحوِّرة إلى خلايا عصبية حركية عبّرت عن علامات نموذجية، وشكّلت شبكات متفرعة، وأقامت اتصالات شبيهة بالمشابك، مُحاكية بشكل وثيق الخلايا العصبية الموجودة في الجهاز العصبي. 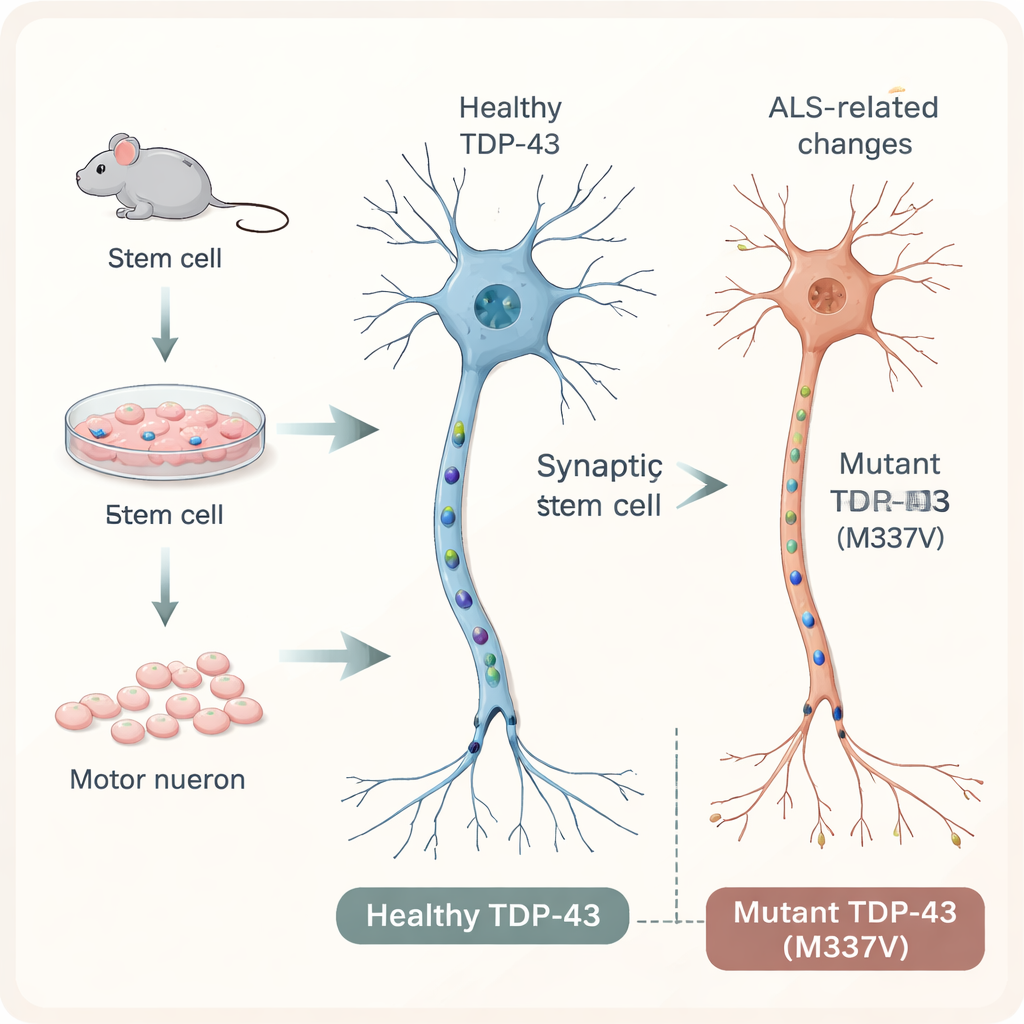
تلف خفي بلا تكتلات بروتينية مرئية
في مرضى ALS، غالباً ما ينتقل TDP-43 من موضعه الاعتيادي في النواة إلى الحاضنة الخلوية ويتجمع في تكتلات، وهو علامة مرضية كلاسيكية تُرى تحت المجهر. بشكل مفاجئ، في نموذج الخلايا الجذعية هذا، لم تُظهر نسخة TDP-43 المتحورة ازدياداً في الإزاحة الخلوية أو التجمع مقارنةً بالنسخة الطبيعية. بقي معظم البروتين في موضعه الصحيح. ومع ذلك كانت الخلايا العصبية أقل صحة بشكل واضح: أظهرت الثقافات التي تحتوي على البروتين المتحوِّر أجسام خلايا أقل، وشبكات ألياف عصبية أصغر، وانخفاضاً في قابلية البقاء العامة. وهذا يوحي بأن ضرراً جدياً للخلايا العصبية الحركية قد يحدث قبل، أو حتى دون، التكتلات البروتينية الدرامية التي تُرى في أدمغة وحبال شوكية المرضى.
اختناقات مرورية على "الطرق السريعة" العصبية
تعتمد الخلايا العصبية الحركية على أنظمة نقل سريعة وفعالة تحرك الشحنات الحيوية صعوداً ونزولاً على محاورها الطويلة. باستخدام أجهزة ميكروفلويدية تعزل المحاور في قنوات دقيقة، تتبّع الفريق حركة حزَم الإشارات (الحويصلات النهائية) والميتوكندريا المنتجة للطاقة في خلايا حية. في الخلايا العصبية الحاملة لـTDP-43 المتحور، استمرت هذه الشحنات بالحركة في الاتجاهات الصحيحة إلى حد كبير، لكنها تحرّكت بوتيرة أبطأ. أظهرت الحويصلات الإشارية سرعات مخفّضة عند التحرك عائدة نحو جسم الخلية، وتحركت الميتوكندريا ببطء أكبر في كلا الاتجاهين، مع زيادة الوقت الذي تقضيه متوقفة. والأهم أن الآلية الأساسية التي تحفز هذا الحركة — بروتينات المحرك التي تمشي على المسارات الداخلية — لم تبدُ أنها تغيرت في الكمية، مما يوحي بأن المشكلة تكمن في كيفية عمل هذه الآلية بدلاً من مقدارها.
عجز في طاقة احتراق السكر، وليس في الميتوكندريا
بما أن النقل المحوري يستهلك طاقة كبيرة، اختبر الباحثون كيف تصنع هذه الخلايا العصبية الطاقة وتستخدمها. قاسوا مصدرين رئيسيين: التنفّس الميتوكندري الذي يحرق الوقود باستخدام الأكسجين، والتحلل السكري الذي يكسر السكر في الوسط المحيط. بدت الميتوكندريا طبيعية من حيث العدد والشكل وجهد الغشاء، وقد بدا أن قدرتها العامة على إنتاج الطاقة لم تتغير في الخلايا المتحورة. بالمقارنة، أظهرت الخلايا العصبية ذات TDP-43 المتحور هبوطاً واضحاً في التحلل السكري الأساسي. أظهرت أبحاث سابقة أن التحلل السكري المحلي على طول المحاور يمكن أن يزوّد "وقوداً داخلياً" للنقل السريع للحويصلات. لذا قد تسهم القدرة المخفضة على حرق السكر هنا في تباطؤ حركة الشحنات، مضيفة طبقة إضافية من الضغط على الخلايا العصبية الحركية الضعيفة بالفعل.
ما يعنيه ذلك لعلاجات ALS المستقبلية
تشير الدراسة مجتمعة إلى أن حتى مستويات منخفضة من TDP-43 المتحور المرتبط بالـALS كافية لجعل الخلايا العصبية الحركية أضعف، وإبطاء حركة الشحنات الأساسية عبر محاورها، وتثبيط قدرتها على توليد الطاقة من السكر — كل ذلك دون التكتلات البروتينية الواضحة التي يبحث عنها علماء الأمراض عادة. للقراء غير المتخصصين، الرسالة الأساسية هي أن تغيّرات مبكرة ودقيقة في "تدفُّق المرور" الخلوي واستخدام الطاقة قد تمهّد لحدوث أضرار لاحقة أكثر دراماتيكية في ALS. يبرز هذا النقل المحوري ومسارات الطاقة الخلوية، وخصوصاً التحلل السكري، كأهداف واعدة للعلاجات التي تسعى لحماية الخلايا العصبية الحركية قبل وقوع الانحلال اللاحق الذي لا رجعة فيه. 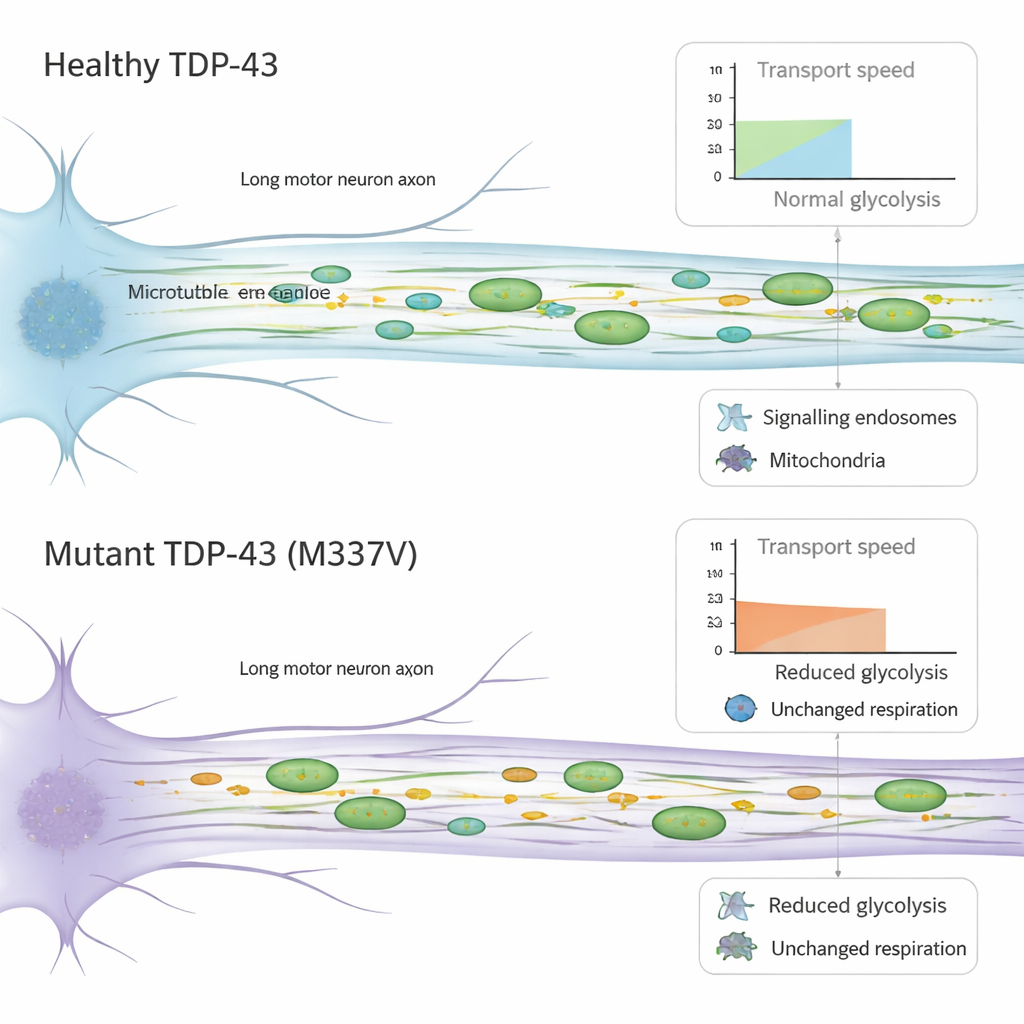
الاستشهاد: Carroll, E., Scaber, J., Pasniceanu, IS. et al. Mutant TDP-43 drives impairments in axonal transport and glycolysis in a mouse stem-cell-derived motor neuron model of amyotrophic lateral sclerosis (ALS). Cell Death Dis 17, 193 (2026). https://doi.org/10.1038/s41419-026-08437-2
الكلمات المفتاحية: التصلب الجانبي الضموري, TDP-43, الخلايا العصبية الحركية, النقل المحوري, طاقة خلوية