Clear Sky Science · ar
BCL-xL كهدف علاجي في سرطان القولون والمستقيم المقاوم للسيتوكسيماب
لماذا يهم هذا الأشخاص المصابين بسرطان القولون
يعد سرطان القولون والمستقيم من أكثر السرطانات شيوعًا على مستوى العالم، ويتلقى العديد من المرضى ذوي المرض المتقدم دواءً مناعيًَّا موجهًا يسمى سيتوكسيماب. قد يسبب هذا الدواء انكماش الأورام في البداية، لكن في معظم المرضى تجد الخلايا السرطانية سبلًا للهروب خلال أشهر، مما يترك للأطباء خيارات قليلة جيدة. تطرح هذه الدراسة سؤالًا ملحًا: عندما تتوقف أورام القولون عن الاستجابة للسيتوكسيماب، هل توجد نقطة ضعف أخرى يمكن للأدوية الجديدة استغلالها لإحداث موت خلايا السرطان؟
عندما يتوقف دواء موجه عن العمل
يعمل السيتوكسيماب عبر منع مستقبل سطحي على الخلايا السرطانية يسمى مستقبل عامل نمو البشرة (EGFR)، الذي يساهم في دفع نموها. أنشأ الفريق نموذج مقاومة في المختبر عن طريق تعريض سلالة خلايا سرطان القولون الحساسة (LIM1215) لجرعات متزايدة تدريجيًا من السيتوكسيماب على مدار ستة أشهر. نشأت مجموعتان مستقلتان من الخلايا المقاومة استمرت في النمو حتى في مستويات دوائية عالية، ومع ذلك بدت صحية وسريعة التكاثر تمامًا مثل الخلايا الأصلية عندما أُزيل الدواء. من المهم أن الخلايا المقاومة لا تزال تحمل هدف الدواء على سطحها وكان بإمكان السيتوكسيماب الارتباط به، ما يشير إلى أن السرطان لم "يخفي" أو يغير المستقبل ببساطة.
الخلايا المقاومة تعيد توجيه إشارات نموها
لفهم كيفية تجاوز الخلايا للسيتوكسيماب، فحص الباحثون مسارات النمو الرئيسية داخل الخلية. في الخلايا الأصلية، كان السيتوكسيماب يخفض عادة نشاط مسار MAPK، وهو محرك رئيسي لانقسام الخلايا. في الخلايا المقاومة ظل نشاط MAPK مرتفعًا حتى عند حجب EGFR، مما يُظهر أن إشارة النمو انفصلت عن المستقبل الأصلي. كشف تسلسل الحمض النووي الريبي للخلايا عن طفرات منشِطة جديدة في جين RAS آخر، HRAS، في مجموعات فرعية من الخلايا المقاومة، ولم توجد في المشتبه بهم المعتادين مثل KRAS أو NRAS أو BRAF. أدت محاولات إغلاق هذا المسار المعاد توجيهه باستخدام دواء مثبط لـ MEK (الذي يعمل أسفل RAS) إلى تقليل النمو بشكل طفيف فقط. أبرز ذلك أنه بدلًا من ملاحقة كل طفرة جديدة، قد يكون أكثر فعالية مهاجمة آليات البقاء والموت الخلوية المشتركة عبر الشُعب المقاومة المختلفة. 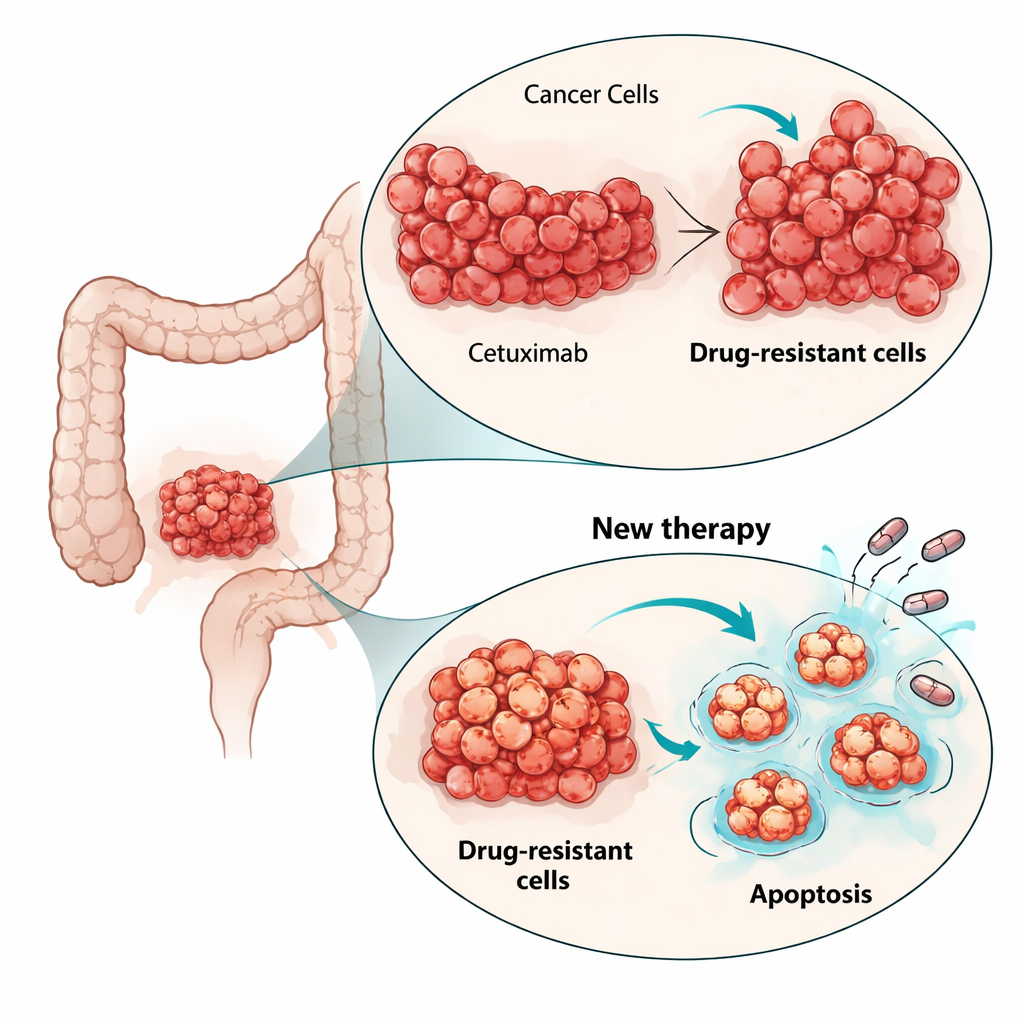
استهداف نظام دعم الحياة في السرطان
حوّل العلماء تركيزهم إلى الاستماتة، برنامج الانتحار الخلوي المدمج الذي تقمعه السرطانات غالبًا. أظهرت تحليلات التعبير الجيني أن مسارات متعلقة بالاستماتة تغيرت في الخلايا المقاومة. على وجه الخصوص، كان بروتين مقاومة الموت BCL-xL أعلى في إحدى المجموعات المقاومة ومتزايدًا بشكل متواضع في الأخرى، بينما كان بروتين بقاء آخر، MCL-1، موجودًا أيضًا. اختبر الفريق جزيئات صغيرة تعرف باسم محاكيات BH3 المصممة لحجب هذه البروتينات الباقية وإطلاق آلية الموت. في زراعات ثنائية الأبعاد، كانت الثلاث سلالات الخلوية — الأصلية والمقاومة — حساسة للأدوية التي تحجب BCL-xL أو MCL-1، لكن، بشكل لافت، جرعات أقل قتلت خلايا السيتوكسيماب المقاومة بفعالية أكبر. إضافة جرعة منخفضة من مثبط البروتيازوم بورتيزوميب، الذي يساعد على تراكم الإشارات المؤيدة للموت، عزز القتل أكثر، خاصة عند الجمع مع حاجز MCL-1.
من أطباق مسطحة إلى أورام مصغرة ثلاثية الأبعاد وأنسجة المرضى
لأن الطبقات الخلوية المسطحة لا تستطيع تمثيل الأورام في الجسم بشكل كامل، زرع الفريق الخلايا ككرات ثلاثية الأبعاد مضمّنة في هلام، لتعكس بشكل أفضل بنية الأورام الحقيقية وتحديات اختراق الدواء. مرة أخرى أدى حجب BCL-xL أو MCL-1 إلى تقليل قابلية بقاء الكرات، وتسبب الجمع بين هذه الأدوية وبورتيزوميب في انخفاضات دراماتيكية في النشاط الأيضي وعلامات واضحة لموت الخلايا. لاختبار ما إذا كانت هذه القابلية موجودة في نسيج ورمي بشري أكثر واقعية، استخدموا شرائح رقيقة من سرطانات القولون والمستقيم المقاومة للسيتوكسيماب نمت في فئران منزوعة الوداج من أورام مرضى (مغروسة من المرضى). كانت هذه النماذج كلها من نوع KRAS البري مثل خلايا LIM1215 الأصلية لكنها حملت طفرات إضافية متنوعة، بما في ذلك في BRAF وTP53، مما يعكس التنوع الجيني المرصود في العيادة. 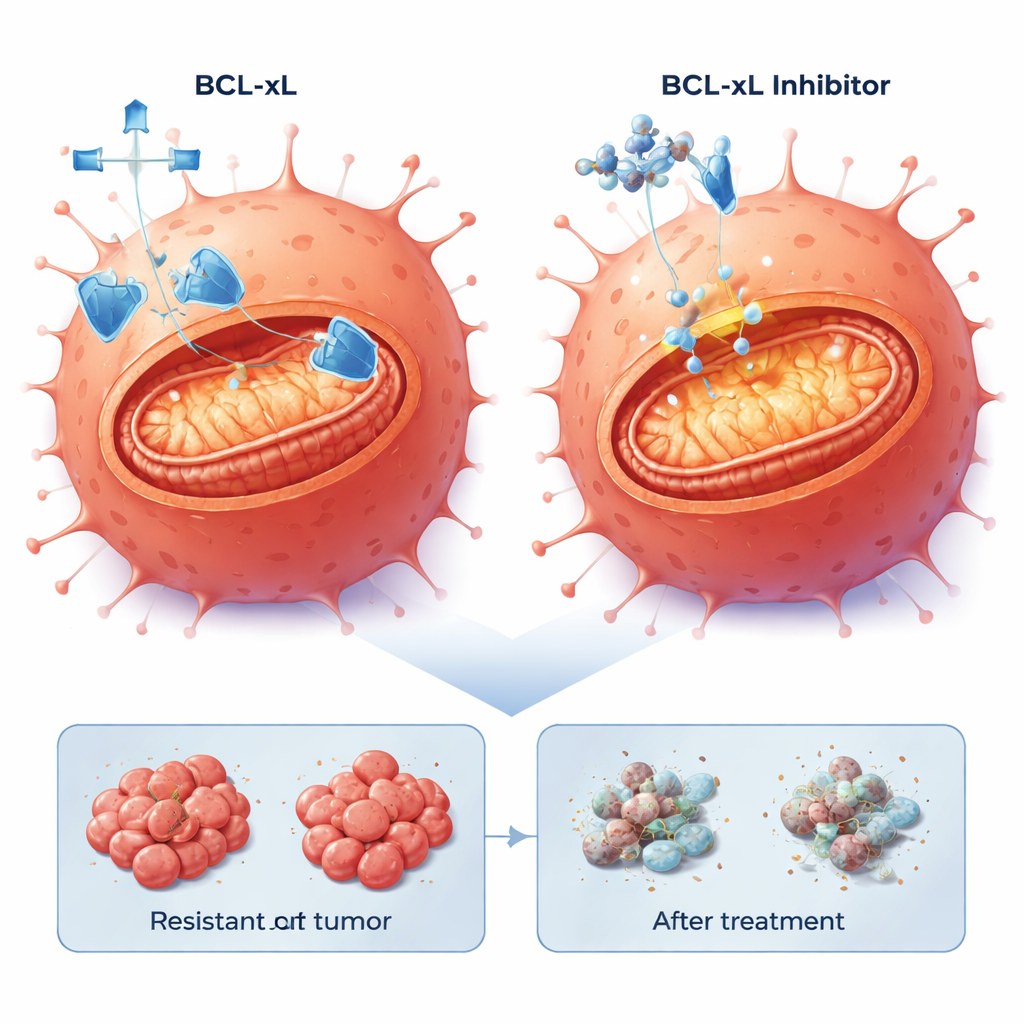
استهداف BCL-xL ينجح عبر أورام مقاومة ومتنوعة
في شرائح الأورام المستمدة من المرضى، أدت مجموعة مكوّنة من مثبط BCL-xL مع جرعة منخفضة من بورتيزوميب باستمرار إلى تحفيز موت خلوي قوي في 20–40% من خلايا الورم عبر أربعة نماذج مختلفة، بما في ذلك تلك ذات طفرات BRAF العدوانية. بالمقابل، أظهر حجب MCL-1 مع بورتيزوميب تأثيرات قوية فقط في مجموعة فرعية من الأورام. ومن المهم أن قدرة الخلايا المقاومة على الخضوع للاستماتة ظلت محفوظة: بمجرد إزالة شبكة الأمان BCL-xL، كان بالإمكان تفعيل برنامج الموت الداخلي، بغض النظر عن المسار الجيني الذي اتبعه الورم للهروب من السيتوكسيماب.
ماذا يعني هذا للمرضى
بالنسبة للأشخاص الذين يتوقف سرطان القولون والمستقيم لديهم عن الاستجابة للسيتوكسيماب، تقدم هذه الدراسة تفاؤلًا حذرًا. فهي تشير إلى أنه حتى بعد أن تصبح الأورام مقاومة للعلاج الموجه ضد EGFR، تظل العديد من خلايا السرطان مهيأة للموت إذا حُجب بروتين البقاء الرئيسي BCL-xL. بينما قد تسبب مثبطات BCL-xL آثارًا جانبية، لا سيما على الصفائح الدموية، يشير العمل إلى استراتيجيات للجمع بين الأدوية وضبط الجرعات قد تحد من السمية مع استغلال نقطة ضعف مشتركة للأورام الصعبة العلاج. في المستقبل قد تشكل الأدوية التي تضعف BCL-xL العمود الفقري لعلاجات خط ثاني جديدة لسرطان القولون والمستقيم المقاوم للسيتوكسيماب، بأقل اعتماد على المشهد الطفري المتغير للورم.
الاستشهاد: Asmanidou, S., Thiel, J., Ekstrom, T.L. et al. BCL-xL as a therapeutic target in cetuximab-refractory colorectal cancer. Cell Death Dis 17, 187 (2026). https://doi.org/10.1038/s41419-026-08434-5
الكلمات المفتاحية: سرطان القولون والمستقيم, مقاومة الدواء, سيتوكسيماب, مثبط BCL-xL, الاستماتة