Clear Sky Science · ar
LAP2α يدفع تكوّن أورام الثدي من خلال التخفيف من إجهاد النسخ
لماذا هذا مهم لسرطان الثدي
تنمو أورام الثدي جزئياً لأن خلايا السرطان تجد طرقاً للبقاء على قيد الحياة تحت ضغوط مستمرة أثناء نسخ حمضها النووي. تكشف هذه الدراسة كيف يساعد بروتين أقل شهرة يُدعى LAP2α خلايا سرطان الثدي على حماية حمضها النووي أثناء النسخ، مما يشجّع نمو الورم ويجعل السرطانات أصعب في المعالجة. فهم هذا النظام الداعم الخفي يقترح طرقاً جديدة لإضعاف الأورام وتحسين فعالية الأدوية الحالية.
مساعد خفي داخل نوى خلايا الورم
في كل مرة تنقسم فيها الخلية، يجب أن تنسخ حمضها النووي بدقة. في خلايا السرطان، تكون هذه العملية تحت ضغط أكبر: إشارات النمو محبوسة في وضع التشغيل، وآلات النسخ تعمل بأقصى طاقتها. يعرف هذا الضغط باسم إجهاد النسخ، وهو يترك مناطق من الحمض النووي أحادية السلسلة يجب تغطيتها وتثبيتها بسرعة بواسطة مجموعة بروتينية تسمى RPA. وجد المؤلفون سابقاً أن LAP2α، وهو بروتين مرتبط بهيكل النووي الداخلي، يمكن أن يرتبط بـRPA ويساعده على الوصول إلى الحمض النووي المتضرر. في العمل الحالي، تساءلوا عمّا إذا كان هذا التعاون بين LAP2α وRPA يغذي فعلاً تطور أورام الثدي ويؤثر في استجابة الأورام للعلاج.
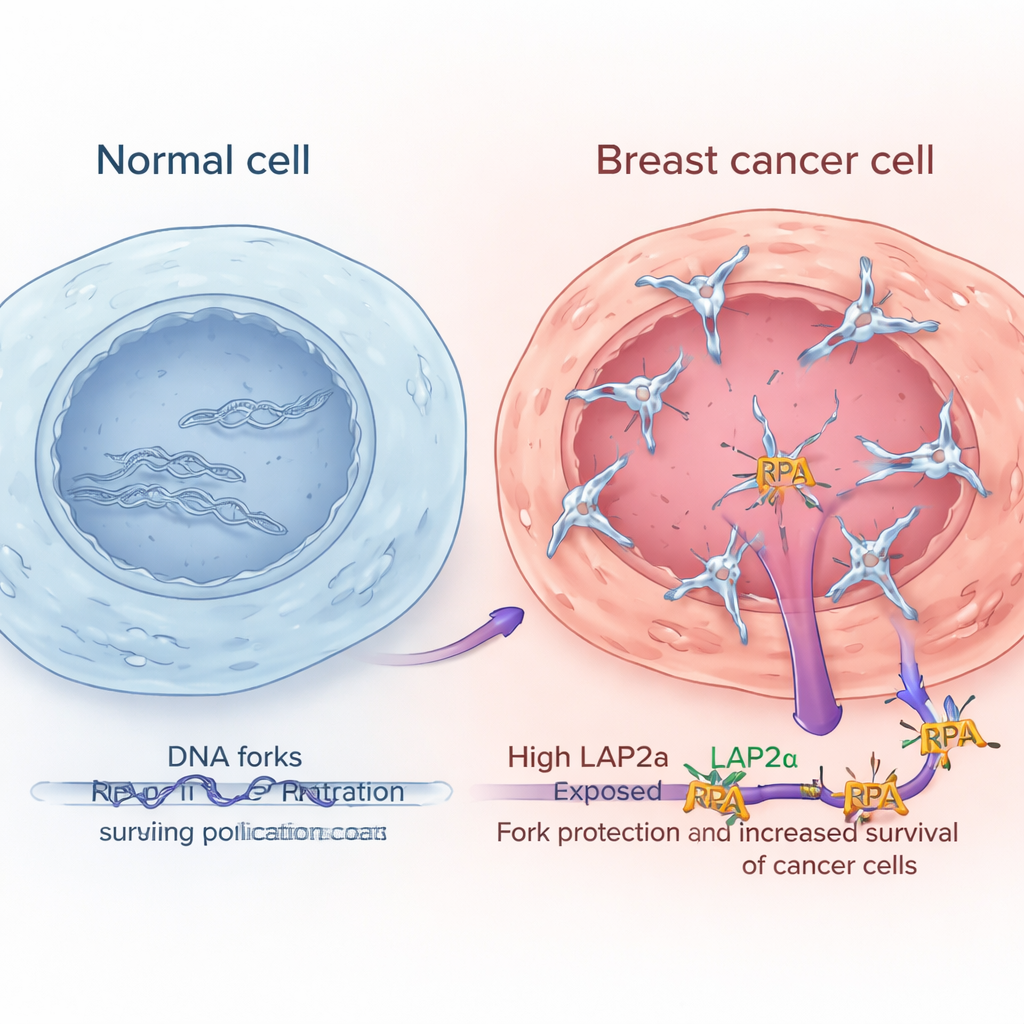
مستويات عالية من LAP2α تميّز الأورام الأكثر عدوانية في الثدي
من خلال تحليل مجموعات بيانات تعبير جيني عامة كبيرة وفحص عينات الأورام تحت المجهر، أظهر الباحثون أن LAP2α يكون دوماً أعلى في نسيج سرطان الثدي مقارنةً بالنسيج الطبيعي المجاور. ترتفع مستوياته مع درجة الورم، مما يعني أن السرطانات الأكثر شذوذاً وعدوانية تميل إلى امتلاك LAP2α أكثر. ظهر هذا النمط عبر عدة أنواع رئيسية من سرطان الثدي، بما في ذلك الأورام الإيجابية لمستقبلات الهرمونات، والأورام الغنية بـHER2، والأورام ثلاثية السلبية. والأهم للمرضى، أن أولئك الذين كانت أورامهم تمتلك مستويات عالية من LAP2α مالوا لأن تكون لديهم بقاء أسوأ. بالمقابل، لم تُظهر مكونات RPA الأساسية تغيّرات مماثلة أو ارتباطات واضحة بالنتيجة، مما يوحي بأن الوظيفة المعززة لـLAP2α، وليس فقط كمية أكبر من RPA، هي ما يساعد خلايا السرطان على التعامل بشكل أفضل مع إجهاد النسخ.
إيقاف LAP2α يبطئ الأورام ويكشف نقاط ضعف
للتقدم ما وراء الارتباطات، استخدم الفريق نماذج فأرية لسرطان الثدي يمكن فيها إزالة LAP2α انتقائياً. بعد تشكّل أورام الثدي، أدى الحذف الجيني لـLAP2α إلى بطء نمو الأورام وإطالة عمر الحيوانات. خلايا الورم الخالية من LAP2α انقسمت أقل وحملت علامات أكثر على تلف الحمض النووي، كما ظهر بزيادة تلوين مؤشرات انقسام الحمض النووي وتقليل تغطية RPA للحمض النووي. عندما نُقلت هذه الخلايا الورمية الناقصة لـLAP2α إلى فئران جديدة، شكّلت مجدداً أوراماً أصغر وأظهرت حساسية متزايدة للعلاج الكيميائي المسبب للضرر في الحمض النووي، بما في ذلك دواء البلاتين سيسبلاتين ومثبط PARP. أكدت تجارب مماثلة في خطوط خلايا سرطان الثدي البشرية أن تقليل LAP2α جعل الخلايا أكثر عرضة لعدة أدوية جينية السمية، بينما إعادة LAP2α الطبيعي — وليس شكل طافح لا يستطيع الارتباط بـRPA — أعادت حماية الحمض النووي ومقاومة الدواء.
كيف يساعد LAP2α في حماية خيوط الحمض النووي الهشة
لتفكيك الآلية، أعاد الباحثون خطوات ارتباط الحمض النووي في تجارب أنبوبية. مزجوا RPA المنقى، والحمض النووي أحادي السلسلة، وإما LAP2α الطبيعي أو صيغة غير قادرة على التفاعل مع RPA. وجدوا أن LAP2α يزيد مباشرة من كفاءة تغطية RPA للحمض النووي أحادي السلسلة ويساعد RPA على شد وتثبيت هذه المناطق الهشة، وهو يعمل أشبه بمساعد تحميل أو شيفرون. عند وجود الحمض النووي، كان RPA يميل إلى مغادرة LAP2α والالتزام تماماً بربط السلسلة المفردة، مما يدل على أن LAP2α ليس جزءاً من الغطاء الواقي النهائي بل يسلم RPA إلى الحمض النووي. بدون تفاعل فعال بين LAP2α وRPA، انهارت مزيد من شوكات النسخ، تراكمت كسور الحمض النووي، وكانت خلايا السرطان أكثر عرضة للموت، لا سيما عند تحفيز ضرر إضافي بالعلاج الكيميائي.
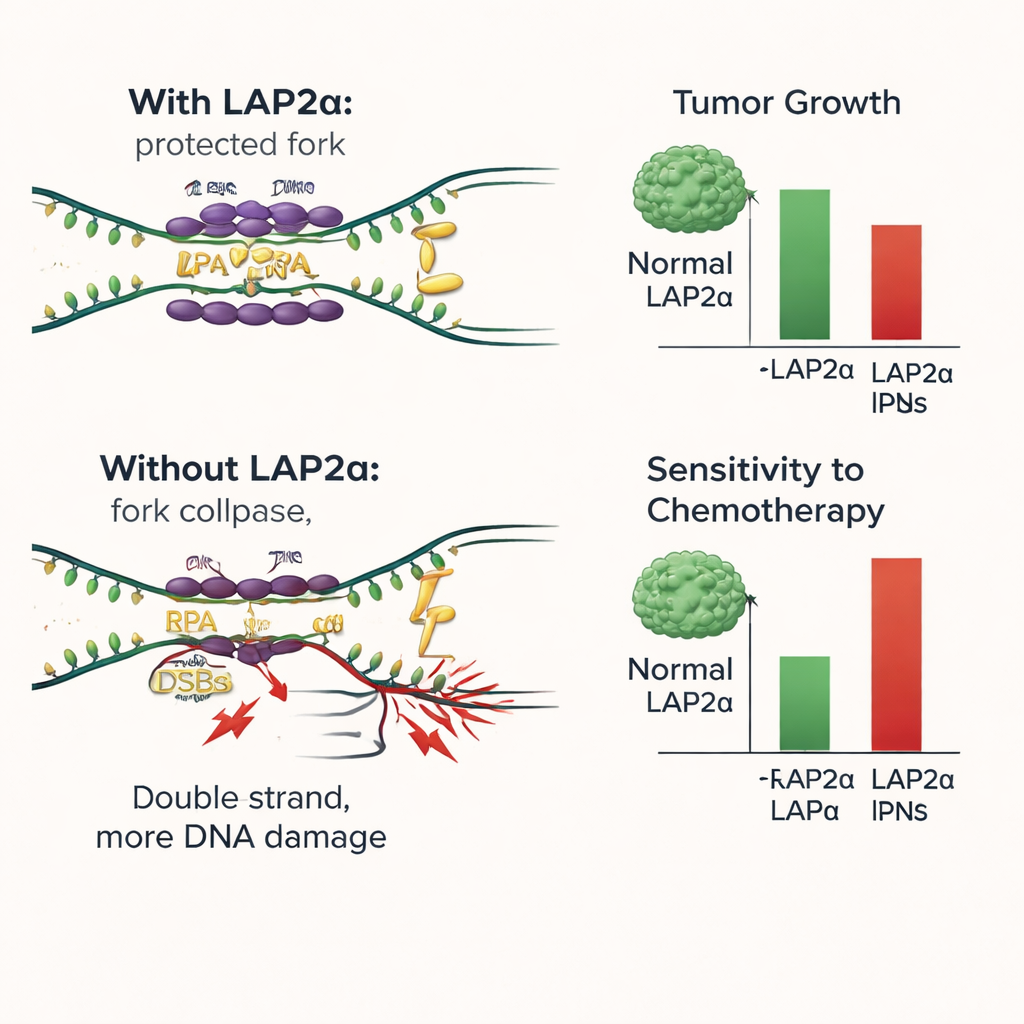
ماذا يعني هذا لعلاج سرطان الثدي في المستقبل
بعبارة بسيطة، تظهر هذه الدراسة أن LAP2α يعمل كمساعد خلف الكواليس يساعد خلايا سرطان الثدي على تحمل ضغط نسخ حمضها النووي. من خلال تحميل RPA بكفاءة على الحمض النووي المعرض للخطر، يقلل LAP2α الضرر ويدعم استمرار نمو الورم. يؤدي إزالة أو تعطيل LAP2α إلى قلب الموازين: يتراكم تلف الحمض النووي، تتوقف الخلايا عن الانقسام، وتصبح الأدوية التقليدية التي تستهدف الحمض النووي أكثر فاعلية. تشير هذه النتائج إلى أن LAP2α يمكن أن يُستخدم كعلامة تنبؤية لسوء النذير وكهدف علاجي جديد. قد تجعل الأدوية التي تعيق LAP2α أو قبضته على RPA العلاجات الحالية مثل عوامل البلاتين ومثبطات PARP أكثر فعالية، خصوصاً في الأورام التي تعتمد بشدة على هذا النظام الموازن للضغط.
الاستشهاد: Ma, Y., Qin, Y., Bao, P. et al. LAP2α drives breast tumorigenesis by mitigating replication stress. Cell Death Dis 17, 201 (2026). https://doi.org/10.1038/s41419-026-08433-6
الكلمات المفتاحية: سرطان الثدي, إجهاد تكرار الحمض النووي, LAP2 alpha, بروتين النسخ A, حساسية العلاج الكيميائي