Clear Sky Science · ar
استهداف تخليق الغليسروفوسفوليبيد يتغلب على المقاومة الكيميائية الناتجة عن فقدان SLFN11 في ساركومة إيونغ
لماذا هذا البحث مهم لسرطان الأطفال
ساركومة إيونغ هي سرطان نادر لكنه عدواني يصيب الأطفال والمراهقين بشكل أساسي. يستجيب كثير من المرضى كيماوياً في البداية بشكل جيد، ولكن بالنسبة لأولئك الذين تعود لديهم الأورام، غالباً ما تفشل العلاجات الحالية. يطرح هذا البحث سؤالاً ملحاً: عندما تصبح خلايا ساركومة إيونغ مقاومة للعلاج الكيميائي، ما التغييرات الداخلية التي تساعدها على البقاء — وهل يمكن تحويل تلك التغييرات إلى نقاط ضعف جديدة يمكن للأطباء استهدافها؟
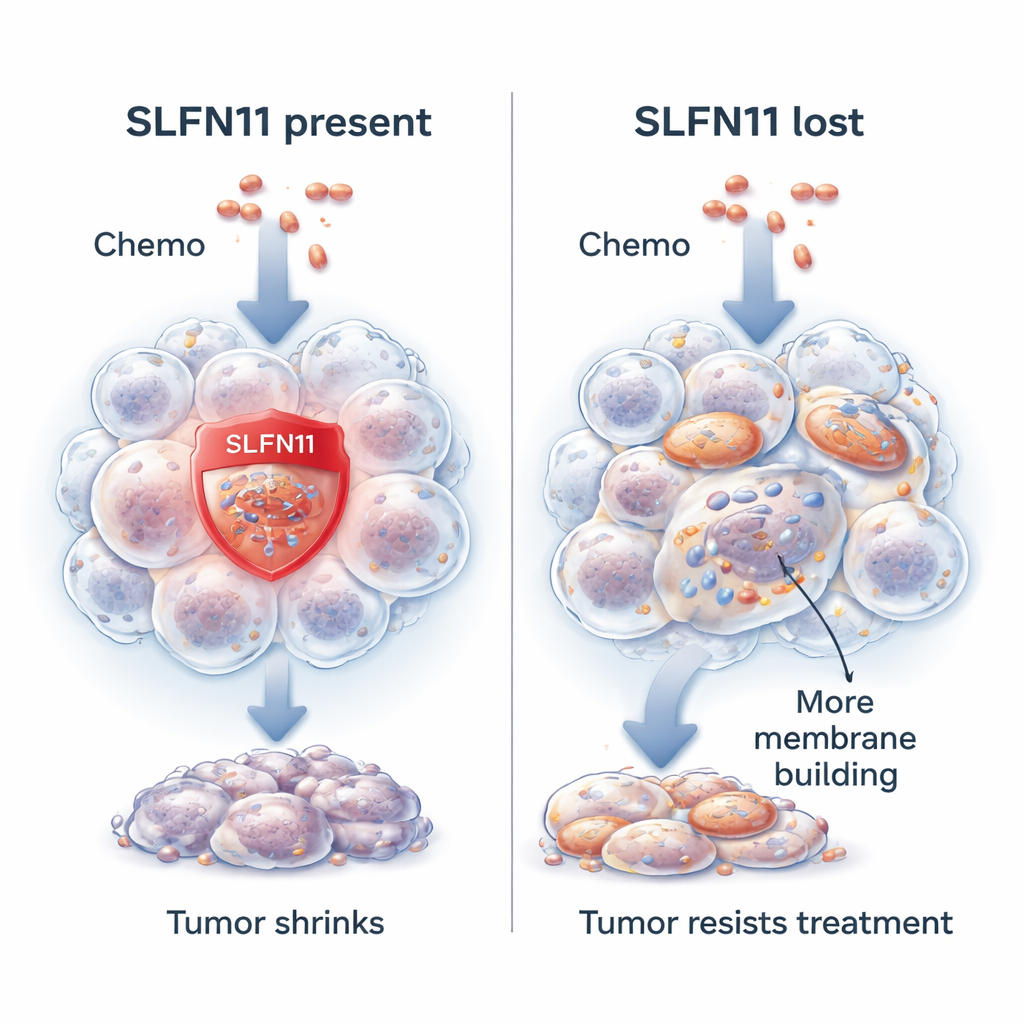
جين يجعل خلايا السرطان أسهل للقتل
يركز الباحثون على جين يُدعى SLFN11. في العديد من أورام ساركومة إيونغ، يكون SLFN11 نشطاً بدرجة عالية ويجعل خلايا السرطان أكثر حساسية للعقاقير التي تضر بالحمض النووي، وهو المخطط الوراثي للخلايا. عند إعطاء هذه الأدوية، يساعد SLFN11 على تعطيل إصلاح الحمض النووي ويدفع الخلية السرطانية نحو الموت. يميل المرضى الذين تحتوي أورامهم على مستويات أعلى من SLFN11 إلى العيش لفترة أطول والاستجابة للعلاج بشكل أفضل. ومع ذلك، فإن نحو واحد من كل عشرة أورام إما يبدأ بقليل أو بدون SLFN11 أو يفقده خلال مسار العلاج. عندما يحدث ذلك، يصبح نفس العلاج الكيميائي أقل فعالية بكثير، ومع ذلك تظل خلايا السرطان قادرة تماماً على النمو.
كيف تعيد خلايا السرطان توصيل استخدام الوقود والدهون
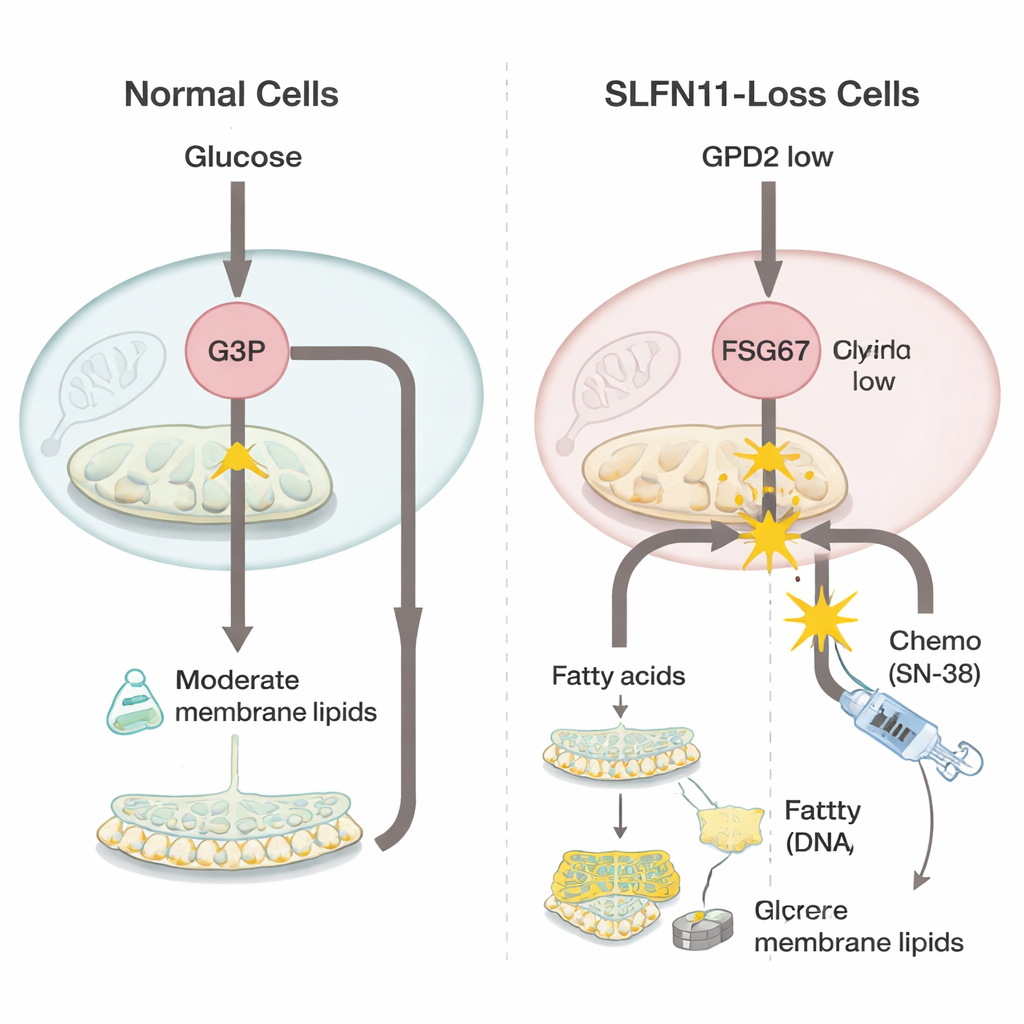
لفهم ما يتغير عند فقدان SLFN11، قارن الفريق خلايا ساركومة إيونغ التي لديها هذا الجين وتلك التي تفتقده باستخدام أدوات «أوميكس» قوية تقيس آلاف الجينات والجزيئات الصغيرة دفعة واحدة. اكتشفوا أن الخلايا التي تفتقر إلى SLFN11 تخفض نشاط إنزيم في الميتوكوندريا يُدعى GPD2، وهو الذي يساعد عادة على حرق جزيء يُسمى غليسيرول‑3‑فوسفات كجزء من إنتاج الطاقة. عندما يقل GPD2، يتراكم غليسيرول‑3‑فوسفات. وبدلاً من أن يضيع، يُحول هذا البناء الإضافي إلى صنع المزيد من الجزيئات الدهنية التي تشكل أغشية الخلايا، وهي مجموعة تعرف بالغليسروفوسفوليبيدات. كما أظهرت الخلايا دلائل على صنع دهون أكثر عدم تشبع ومرونة، مما قد يساعد الأورام سريعة النمو على التكيف مع الضغوط.
تحويل خدعة البقاء إلى نقطة ضعف
لأن هذه الخلايا الناقصة لـ SLFN11 تعتمد أكثر على بناء الأغشية، اختبر العلماء ما إذا كان حجب هذه العملية يمكن أن يعيد حساسية العلاج الكيميائي. استخدموا مركباً يسمى FSG67، الذي يمنع خطوة أساسية في إنتاج الغليسروفوسفوليبيدات. بمفرده، أصبح الدواء القياسي المسبب لضرر الحمض النووي SN‑38 أقل فاعلية كثيراً في الخلايا الناقصة لـ SLFN11، ما يعكس المشكلة السريرية للمقاومة. لكن عندما تم الجمع بين SN‑38 وFSG67، تعرضت الخلايا المقاومة سابقاً لضربة أقوى، وعملت الدواءان معاً بشكل أفضل مما كان متوقعاً من تأثير كل منهما على حدة. بالمقابل، في الخلايا التي لا تزال تحتوي على SLFN11 وكانت شديدة الحساسية أصلاً لـ SN‑38، لم يضف FSG67 فائدة كبيرة وقد يكون حتى مضراً قليلاً. وهذا النمط يشير إلى أن الاعتماد الجديد على إنتاج الدهون والأغشية محدد للحالة المقاومة والمنخفضة SLFN11.
علامة محتملة غير باضعة للأورام الصعبة العلاج
سأل الباحثون بعد ذلك ما إذا كان يمكن اكتشاف هذا إعادة توصيل الاستقلاب في الأورام الفعلية وليس فقط في الخلايا المزرعية. نَمَوا أورام ساركومة إيونغ في فئران، مع أو بدون SLFN11، واستخدموا الرنين المغناطيسي النووي (NMR) لفحص التركيب الكيميائي لمستخلصات الأورام. أظهرت الأورام التي تفتقر إلى SLFN11 نسبة أعلى من جزيئين يحتويان على الكولين مرتبطين بدوران الغشاء: الفوسفوكولين والغليسيروفوسفوكولين. وقد رُبطت نسبة عالية من الفوسفوكولين إلى الغليسيروفوسفوكولين في سرطانات أخرى بسلوك أكثر عدوانية واستجابة علاجية أسوأ. ولأن إشارات الكولين يمكن قياسها باستخدام تقنيات تصوير متقدمة، قد يخدم هذا التحول يوماً ما كعلامة غير باضعة للإشارة إلى أورام ساركومة إيونغ التي تبنت هذا النمط المقاوم المبني على تصنيع الأغشية.
ما الذي قد يعنيه هذا للعلاجات المستقبلية
بشكل عام، تُظهر الدراسة أنه عندما تفقد خلايا ساركومة إيونغ SLFN11 وتصبح أقل حساسية للعلاجات المسببة لضرر الحمض النووي، فإنها تعوض ذلك عبر إعادة توصيل استقلابها نحو صنع المزيد من الدهون الغشائية. هذا التحول لا يساعد الخلايا على النجاة فحسب؛ بل يخلق أيضاً كعب أخيل جديد. إن حجب إنتاج الغليسروفوسفوليبيدات بدواء مثل FSG67 يمكن أن يعيد جزئياً قدرة العلاج الكيميائي على القتل في هذه الخلايا المقاومة. وبينما لم يصبح FSG67 بحد ذاته عقاراً سريرياً بعد، تشير هذه النتائج إلى استراتيجية قد يطابق من خلالها الأطباء يوماً ما أورام المرضى بحسب حالة SLFN11 والملامح الاستقلابية، ثم يزاوجون العلاجات المسببة لضرر الحمض النووي مع مثبطات محددة لصنع الدهون والأغشية لتجاوز المقاومة.
الاستشهاد: Chakraborty, K., Burman, R., Satheesh, S. et al. Targeting glycerophospholipid biosynthesis overcomes chemoresistance driven by SLFN11 loss in Ewing sarcoma. Cell Death Dis 17, 190 (2026). https://doi.org/10.1038/s41419-026-08432-7
الكلمات المفتاحية: ساركومة إيونغ, المقاومة الكيميائية, SLFN11, استقلاب السرطان, تخليق الدهون