Clear Sky Science · ar
استهداف IGFBP2 الإكسوسومية الناتجة عن نقص الأكسجة يتغلب على تهرب المناعة المتوسط بـCD47 في الورم الأرومي الدبقي
لماذا قد يسبب تجويع الأورام من الأكسجين نتائج عكسية
لطالما علم الأطباء أن الورم الأرومي الدبقي، وهو سرطان قاتل في الدماغ، ينمو غالباً في مناطق تعاني من نقص الأكسجة. تجعل هذه الجيوب منخفضة الأكسجين العلاج أكثر صعوبة. تكشف هذه الدراسة كيف يساعد انخفاض الأكسجين خلايا السرطان على الاختفاء من جهاز المناعة، وتقترح مزيج علاجياً جديداً قد يجعلها أكثر عرضة لهجوم الجسم.
ورم دماغي قاتل يتملص من دفاعاتنا
الورم الأرومي الدبقي هو أكثر أورام الدماغ شيوعاً وعدوانية لدى البالغين، وغالباً ما تُقاس فترة البقاء فيها بالأشهر. وعلى الرغم من تسلل خلايا مناعية إلى هذه الأورام، فإن خلايا السرطان كثيراً ما تهرب من التدمير. أحد مسارات الهروب الرئيسية هو بروتين سطحي يُدعى CD47، يُعرف أحياناً بإشارة «لا تأكلني»، الذي يخبر الخلايا المناعية المجاورة مثل الضامة بعدم ابتلاع وتدمير خلية الورم. تُجرب أدوية تمنع CD47 بالفعل، لكن النتائج في الأورام الصلبة مثل الورم الأرومي الدبقي كانت متباينة، ما يوحي بوجود عوامل أخرى في بيئة الورم قد تقوّض فعالية هذه العلاجات.
مناطق نقص الأكسجة وحزم صغيرة من السرطان
باستخدام تسلسل RNA للخلية الواحدة، خريطة الباحثون آلاف الخلايا من مناطق مختلفة من عينات الورم الأرومي الدبقي، مقارنِينَ نواة الورم منخفضة الأكسجين بحافته الخارجية. وجدوا نوعاً فرعياً شديد العدوانية في النواة منخفضة الأكسجة، يُدعى خلايا GBM الشبيهة باللحمة (mesenchymal-like)، والتي عبّرت بقوة عن CD47 وبروتين اسمه IGFBP2. في الوقت نفسه، اكتشفوا أن هذه الخلايا النواة أفرزت أعداداً كبيرة من الحويصلات النانوية المعروفة بالإكسوسومات، التي حملت IGFBP2 على سطحها. وبما أن الإكسوسومات يمكنها الانتقال عبر الدماغ وحتى إلى مجرى الدم، فهي قادرة على نشر الإشارات بعيداً عن مواضع إنتاجها. 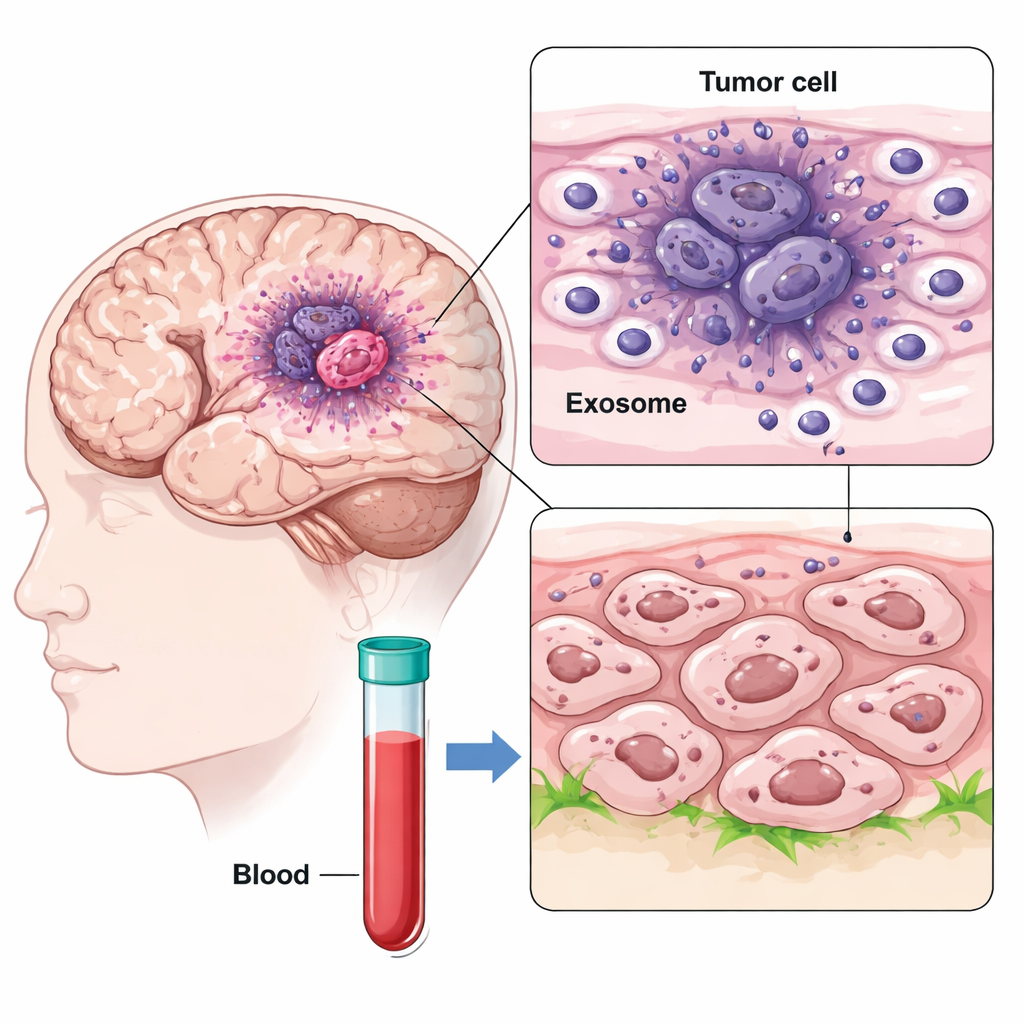
كيف يعزز بروتين مرافق إشارة «لا تأكلني»
ثم تعمق الفريق في وظيفة IGFBP2. أظهروا أنه تحت نقص الأكسجة، يعمل بروتين حساس لنقص الأكسجة يُدعى HIF-2α على تشغيل جين IGFBP2 في خلايا الورم. يرتبط IGFBP2 بعد ذلك بمستقبلات محددة تُدعى التكاملات (integrins) على سطح الإكسوسومات، مما يزيّن غشائها الخارجي. عندما تندمج هذه الإكسوسومات المغلفة بـIGFBP2 مع خلايا ورمية أخرى، تُفعّل سلسلة إشارات داخل الخلية تشمل بروتينات معروفة باسم FAK وSTAT3. تؤدي هذه الشلالة في النهاية إلى زيادة كمية CD47 على سطح خلية الورم، معزِّزةً رسالة «لا تأكلني» للضامات ومُعمّقةً حماية خلايا السرطان من الهجوم المناعي. 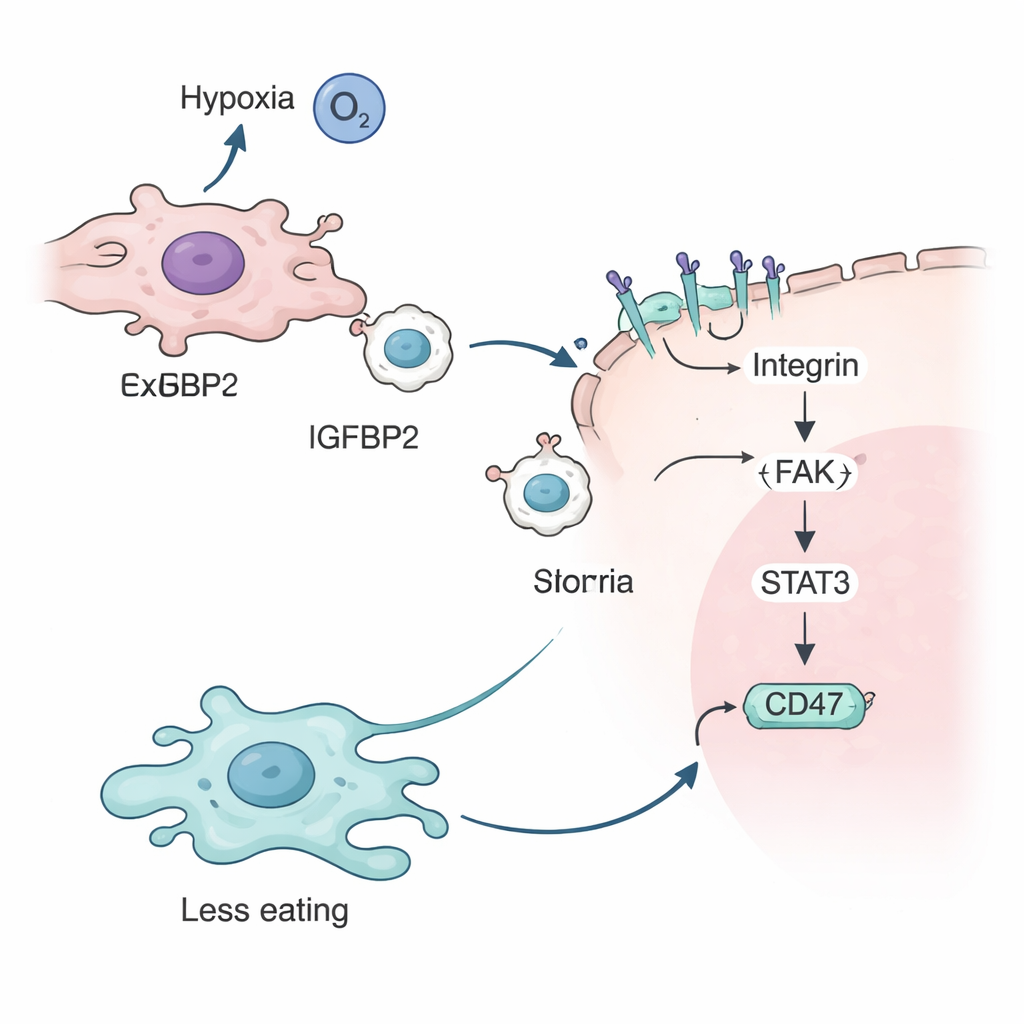
أدلة من عينات مرضى ونماذج حيوانية
لربط هذه النتائج المختبرية بالمرض الحقيقي، فحص الباحثون نسيج الورم والدم من أشخاص مصابين بالغليوما. وجدوا أن مستويات IGFBP2 كانت أعلى في كلٍ من الأورام والإكسوسومات الدموية لدى المرضى ذوي المرض المتقدم، ما يوحي بأن الإكسوسومات الموجبة لـIGFBP2 يمكن أن تكون علامة دمويّة على درجة الورم. في نماذج الفئران، جعل خفض IGFBP2 في خلايا الورم الأرومي الدبقي هذه الخلايا أكثر عرضة لابتلاع الضامات، وأبطأ نمو الورم، وطوّل البقاء. وبالمقابل، أدى إضافة إكسوسومات غنية بـIGFBP2 إلى زيادة مستويات CD47، وتقليل الأكل المناعي، وتسريع تقدم الورم.
ضربة علاجية واعدة مزدوجة
أخيراً، اختبر الفريق ما إذا كان حجب IGFBP2 يمكن أن يجعل علاج استهداف CD47 أكثر فاعلية. في فئران مصابة بأورام دماغية، أدى العلاج بأجسام مضادة ضد كل من IGFBP2 وCD47 إلى نشاط أقوى للضامات، وأورام أصغر، وبقاء أطول مقارنة بكل علاج بمفرده. عن طريق قطع إشارة IGFBP2 المدفوعة بنقص الأكسجة وحجب إشارة «لا تأكلني» بواسطة CD47 مباشرة، هاجم هذا العلاج المزدوج تمويه الورم المناعي من اتجاهين. بالنسبة للمرضى، تشير هذه النتائج إلى أن قياس IGFBP2 في الإكسوسومات الدموية قد يساعد في تحديد من هم أكثر احتمالاً للاستفادة من علاج مناعي قائم على CD47، وأن دمج مثبطات IGFBP2 وCD47 قد يكون استراتيجية أقوى ضد الورم الأرومي الدبقي من أي دواء بمفرده.
الاستشهاد: Qi, Y., Zhao, R., Zhang, X. et al. Targeting hypoxic exosomal IGFBP2 overcomes CD47-mediated immune evasion in glioblastoma. Cell Death Dis 17, 192 (2026). https://doi.org/10.1038/s41419-026-08430-9
الكلمات المفتاحية: الورم الأرومي الدبقي, الإكسوسومات, تهرب مناعي, CD47, نقص الأكسجة