Clear Sky Science · ar
HSPA5 يعزز استقرار YAP/TAZ بشكل مستقل عن مسار هيبو ويحفز التحول من الحالة العصبية إلى الميزنشيمالية في الورم الدماغي الأرومي
لماذا تهمّ هذه الدراسة لسرطان الدماغ
الورم الأرومي الدبقي هو واحد من أخطر سرطانات الدماغ، ويرجع ذلك جزئياً إلى أن العديد من الأورام تتحول مع الوقت إلى حالة أكثر صلابة ومقاومة للعلاج. تكشف هذه الدراسة كيف يساعد بروتين شائع في استجابة الإجهاد، HSPA5، على دفع ذلك التحول ويحافظ على جزيئات تعزز الورم أطول مما ينبغي. فهم هذه «الحيلة البقائية» يفتح سبلًا جديدة لجعل الورم الأرومي الدبقي أقل عدوانية وأكثر استجابة للعلاجات المتاحة.
ورم يغيّر شخصيته
يعترف الأطباء والعلماء اليوم أن الورم الأرومي الدبقي ليس مرضًا واحدًا بل مزيجًا من الأنماط الجزيئية. هناك نوعان رئيسيان: شكل «عصبي المنشأ» (proneural) الذي يكون أقل عدوانية إلى حد ما، وشكل «ميزنشيمي» الذي يكون أكثر تغلغلاً ومقاومة للعلاج ومترابطًا بانتكاس مبكر. يمكن للأورام أن تتطور من الحالة العصبية المنشأ إلى الحالة الميزنشيمالية، وهي عملية يسميها المؤلفون التحول من العصبي المنشأ إلى الميزنشيمي (PMT). سعى الفريق لمعرفة أي بروتينات استجابة للإجهاد قد تدفع الأورام على هذا المسار الخطر.
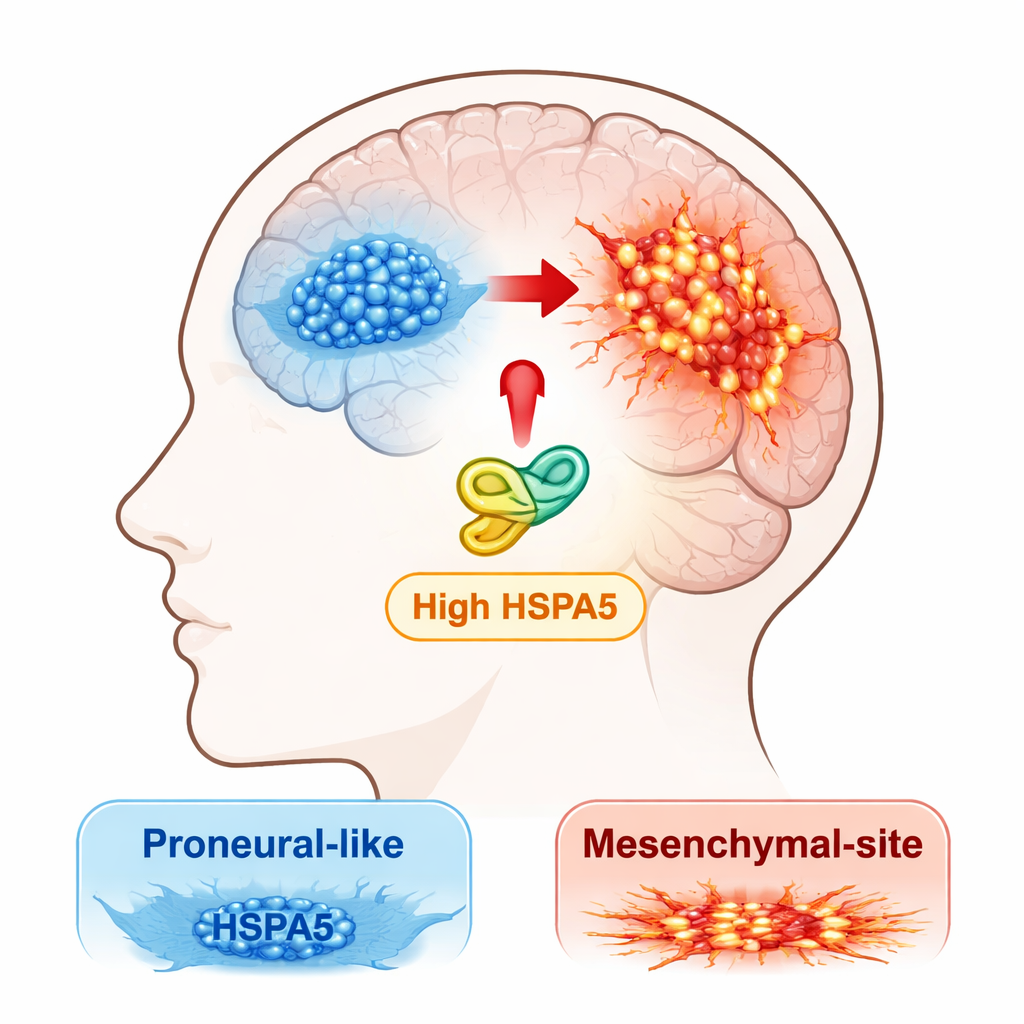
بروتين مساعد للإجهاد تحت الأضواء
بدأ الباحثون بمسح مجموعات بيانات سرطانية عامة كبيرة وعينات مرضاهم الخاصة بحثًا عن أعضاء عائلة HSP70، وهي مجموعة من بروتينات «المرافق» التي تساعد البروتينات الأخرى على الطي والبقاء تحت الإجهاد. برز أحد هذه المرافق، HSPA5. كانت نشاطاته أعلى في النوع الميزنشيمي من الورم الأرومي الدبقي ومرتفعة بشكل ملحوظ في الأورام مقارنة بنسيج الدماغ الطبيعي. وارتبطت مستويات أعلى من HSPA5 في أورام المرضى ببقاء إجمالي أسوأ، مما يبرز دوره المحتمل كسائق للمرض العدواني بدلاً من كونه مجرد مرافقة سلبية.
إجبار الخلايا على أن تصبح أكثر عدوانية
لاستكشاف وظيفة HSPA5 داخل خلايا الورم، زرع الفريق خلايا ورم أرومي دبقي أولية مأخوذة مباشرة من المرضى وفصلها إلى مجموعات تشبه الحالة العصبية المنشأ ومجموعات تشبه الحالة الميزنشيمالية. عندما أجبروا الخلايا العصبية المنشأ على إنتاج HSPA5 إضافي، بدأت تلك الخلايا تتصرف أشبه بالخلايا الميزنشيمالية: انقسمت بسرعة أكبر، وهاجرت وغزت بسهولة أكبر، وشغّلت علامات ميزنشيمالية نموذجية مثل CD44 و c‑MET، بينما خفّضت علامات عصبية المنشأ مثل SOX2 و OLIG2. والعكس كان صحيحًا أيضًا — خفض مستويات HSPA5 في الخلايا الميزنشيمالية قلّل من نموها وغزوها ودفعها جزئيًا نحو ملف أقل عدوانية.
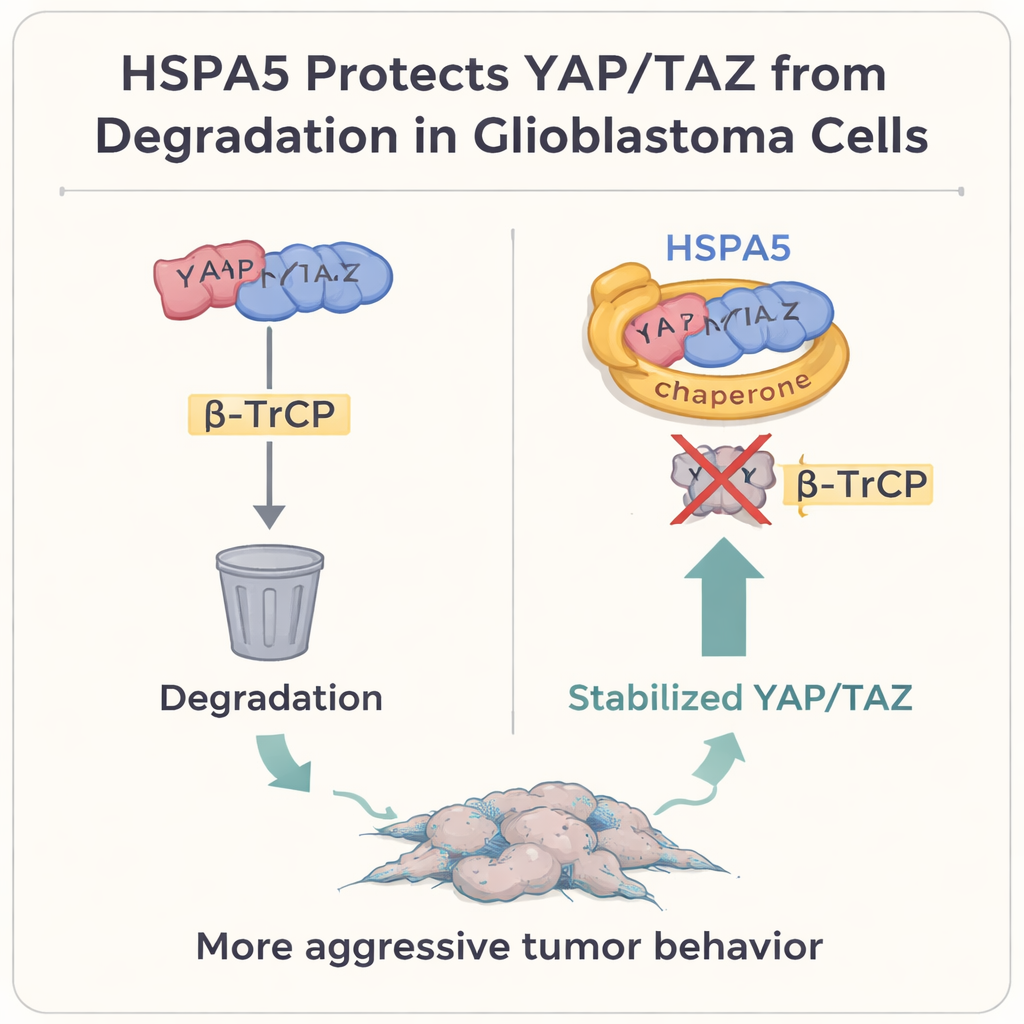
حماية مفاتيح النمو من سلة مهملات الخلية
بالتعمق أكثر، ركز المؤلفون على منظِّمين قويين للنمو، YAP و TAZ، اللذين يقفان في قلب مسار الإشارات هيبو. في العديد من الأورام الصلبة، بما في ذلك الورم الأرومي الدبقي، تعمل هذه البروتينات كمفاتيح رئيسية تعزز نمو الخلايا والمرونة والحالة الميزنشيمالية. عادةً، عندما تريد الخلايا كبح هذا البرنامج، فإنها تميّز YAP و TAZ للتدمير عبر بروتين يُدعى β‑TrCP، الذي يصحبهما إلى «سلة المهملات» الخلوية، البروتيازوم. تُظهر الدراسة أن HSPA5 يرتبط فعليًا بـ YAP و TAZ، مستخدمًا مجال ارتباطه بالركائز كقفاز واقٍ. وبذلك يمنع ارتباط β‑TrCP، ويمنع وسم YAP/TAZ باليوبايتين وتدميرهما، ويسمح بتكدسهما في النواة حيث يُشغّلان الجينات الميزنشيمالية، بما في ذلك CD44 و c‑MET نفسها.
من الأطباق والفئران إلى أورام المرضى
أكد الفريق هذه الآلية بعدة طرق. أدى حجب HSPA5 إلى اختفاء بروتينات YAP و TAZ بسرعة أكبر، ما لم يُثبط البروتيازوم كيميائيًا، وزاد من إشارات «وسم النفاية» عليها. أعاد تنشيط YAP و TAZ انتعاش النمو والغزو الذي فقد عند تقليل HSPA5، بينما قضى إسكات YAP/TAZ على التأثيرات المروِّجة للورم الناتجة عن فرط تعبير HSPA5. في نماذج الفئران التي زرعت فيها خلايا ورم أرومي دبقي بشرية في الدماغ، نمت الأورام ذات مستويات HSPA5 العالية أكبر وقتلت الحيوانات أسرع؛ إن خفض HSPA5، أو مقاطعة دعمه لـ YAP/TAZ، أبطأ النمو ومدد البقاء. أخيرًا، في عينات بشرية مطابقة مأخوذة من نفس المرضى قبل وبعد الانتكاس، أظهرت الأورام المنتكسة والأكثر ميزنشيمالية مستويات أعلى من HSPA5 و YAP و TAZ وعلامات ميزنشيمالية مقارنة بالأورام الأصلية الشبيهة بالعصبية المنشأ.
ماذا يعني هذا لعلاج سرطان الدماغ في المستقبل
بعبارات بسيطة، تشير هذه الدراسة إلى أن خلايا الورم الأرومي الدبقي تستغل مساعدًا في استجابة الإجهاد، HSPA5، لدرء مفاتيح النمو الحيوية (YAP و TAZ) عن التحلل. تساعد هذه الحماية الأورام على التحول إلى هوية أكثر عدوانية ومقاومة للعلاج والحفاظ عليها. ونظرًا لوجود مثبطات جزيئية صغيرة لـ HSPA5 بالفعل واعتمادية خلايا الورم المحتملة على هذا المرافق أكثر من الخلايا الطبيعية، فإن محور HSPA5–YAP/TAZ يقدم هدفًا واعدًا جديدًا. قد تجعل العلاجات التي تضعف هذا الدرع الواقي خلايا الورم الأرومي الدبقي أقل قابلية للتكيّف، وأقل تغلغلاً، وأكثر عرضة للعلاجات القياسية مثل الكيمياء الإشعاعية والعلاج الإشعاعي.
الاستشهاد: Gui, S., Yu, W., Song, Z. et al. HSPA5 promotes YAP/TAZ stability independently of the Hippo pathway and induces proneural-to-mesenchymal transition in glioblastoma. Cell Death Dis 17, 208 (2026). https://doi.org/10.1038/s41419-026-08428-3
الكلمات المفتاحية: ورم أرومي دبقي, HSPA5, YAP/TAZ, مرونة الورم, التحول الميزنشيمي