Clear Sky Science · ar
فقدان MLKL يعيق تطور أم الدم الأبهرية البطنية من خلال تقليل نخر الخلايا العضلية الملساء
لماذا يهم هذا قلبك وشرايينك
أم الدم الأبهرية البطنية هي انتفاخات صامتة في الشريان الرئيسي بالجسم قد تتمزق فجأة وتسبب وفاة. اليوم، الحماية الحقيقية الوحيدة هي الجراحة عندما يصبح الوعاء كبيرًا بشكل خطير بالفعل. تدرس هذه الدراسة زاوية مختلفة تمامًا: بدلاً من انتظار فشل الشريان، هل يمكننا حماية جدار الوعاء عن طريق إيقاف نوع محدد ومثير للالتهاب بشدة من موت الخلايا في طبقة العضلات؟
عندما يضعف شريان رئيسي بهدوء
يحمل الشريان الأبهر البطني الدم من القلب إلى أسفل الجسم. لدى بعض الأشخاص، يتمدد جدارَه ببطء ويتشكل أم دم، غالبًا دون أعراض حتى يصبح كبيرًا أو يتمزق. يعرف العلماء أن خلايا العضلات الملساء في جدار الوعاء تموت وأن الالتهاب المزمن يقوّض الأنسجة الداعمة، لكن نوع موت الخلايا الدقيق المتورط ظل غير واضح. يركّز المؤلفون على عملية تسمى نِكروبتوز — شكل "فوضوي" من الموت الخلوي المبرمج يقوده بروتين يسمى MLKL الذي يفتح الخلايا ويفرش محتوياتها، مما يثير الالتهاب.
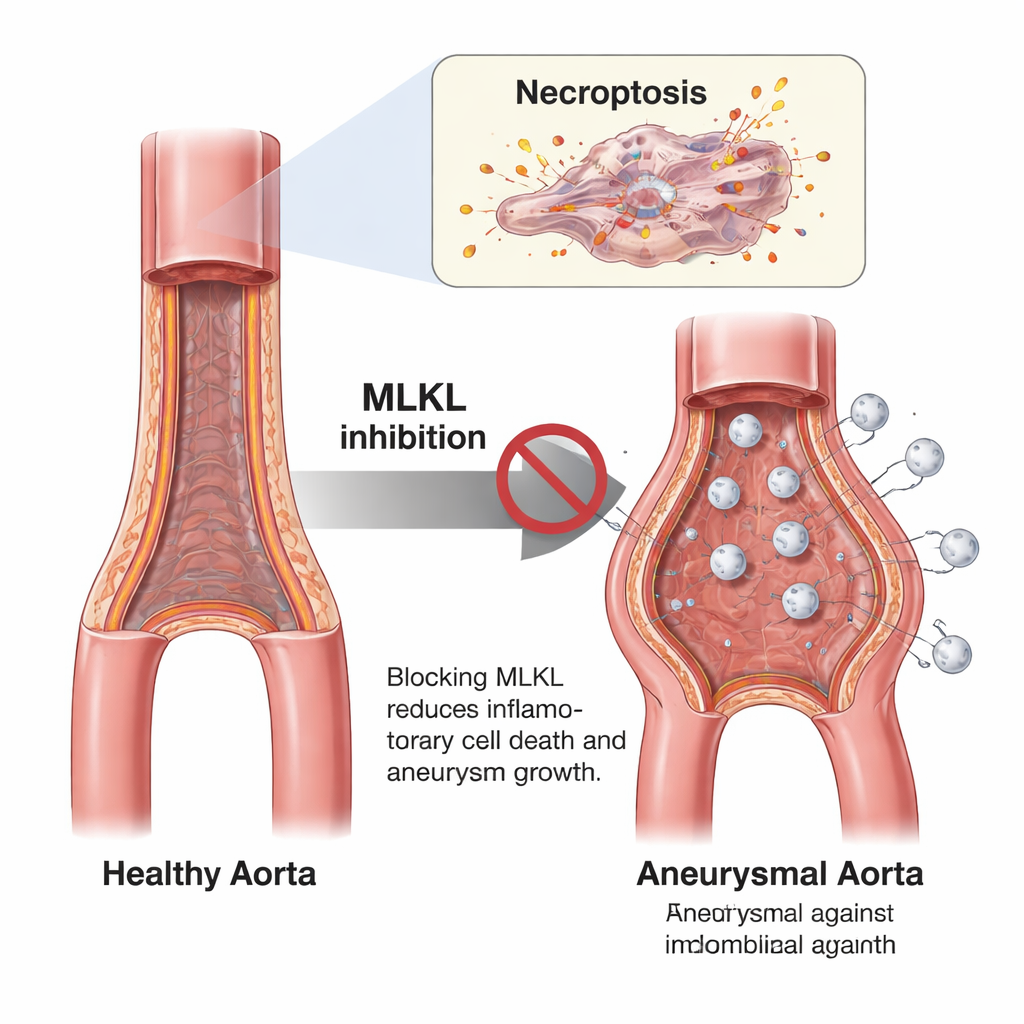
حجب مفتاح الموت يحمي الأبهر في الفئران
لاختبار مدى أهمية النِكروبتوز، استخدمت المجموعة فئرانًا ذات تغييرات وراثية تعطل هذا المسار: بعضها افتقد MLKL تمامًا، وبعضها حمل نسخة متحولة من MLKL لا يمكن تنشيطها، وآخرون حملوا نسخة من بروتين أعلى في السلسلة تُدعى RIPK1 لا تستطيع إطلاق إشاراتها المعتادة. ثم أحدثوا تلفًا شبيهًا بالأم الدم في الجزء السفلي من الأبهر باستخدام محلول الإيلاستاز الذي يضعف جدار الوعاء. مقارنةً بالفئران الطبيعية، طورت الفئران غير القادرة على تنفيذ النِكروبتوز أم دم أصغر بكثير، حافظت على شكل أبهر أقرب للطبيعي في الموجات فوق الصوتية، وأظهرت ضررًا أقل للكولاجين والألياف المرنة — «الحديد والأشرطة المطاطية» التي تمنح الشرايين القوة والمرونة.
خلايا التهابية أقل تغزو جدار الوعاء
كشفت صور المجهر سبب تحسن حالة الفئران المحمية. في الحيوانات الطبيعية، امتلأ الأبهر المصاب بسرعة بالعدلات والبلاعم — خلايا الدم البيضاء الخط الأمامي التي تُطلق إنزيمات وأكسدهات، مما يفاقم تدهور الجدار. في الفئران التي تفتقر إلى MLKL الوظيفي، دخل عدد أقل بكثير من هذه الخلايا جدار الأبهر، رغم أن أعدادها في مجرى الدم لم تتغير. وفي الوقت نفسه، تم الحفاظ على طبقة الخلايا العضلية الملساء بشكل أفضل. أكدت ملفات نشاط الجينات في الأبهر هذه الصورة: في الفئران العادية، شغّلت الجينات المرتبطة بالالتهاب وتجند الخلايا المناعية وتفكك الخثرة بشكل قوي، بينما كانت هذه البرامج الالتهابية والمرتبطة بتحلل الفبرين مخففة بشكل ملحوظ في الحيوانات التي تعاني نقصًا في النِكروبتوز.
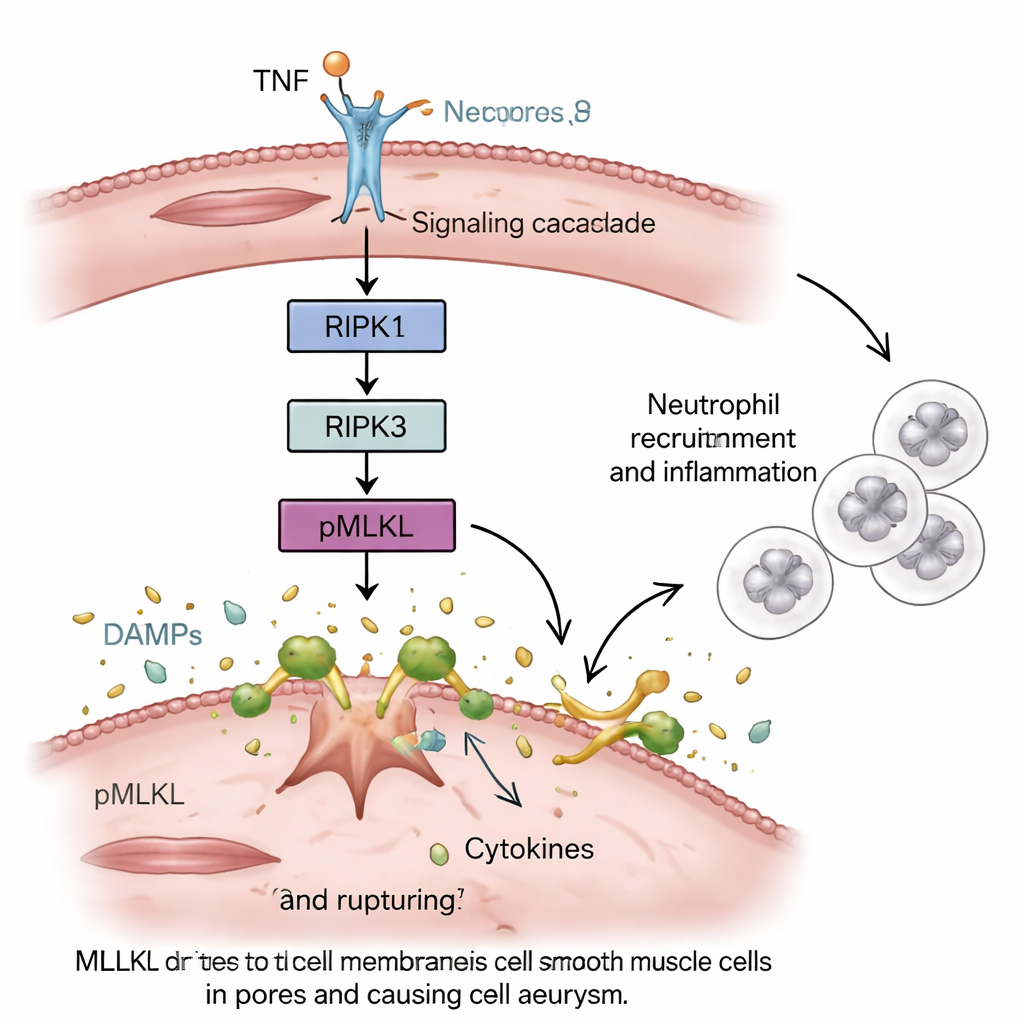
تحولت الخلايا العضلية الملساء من حامية إلى محفزة
بعد ذلك، سأل الباحثون أين يكون النِكروبتوز ذا أهمية قصوى. من خلال تبادل نخاع العظم بين الفئران العادية والمتحولة، تمكنوا من فصل تأثيرات خلايا الدم عن تلك في جدار الوعاء. حدثت أوضح حماية عندما كانت خلايا العضلات الملساء الأبهرية، وليس الخلايا المناعية، تفتقر إلى MLKL. في تجارب زراعة الخلايا مع خلايا عضلات ملساء بشرية وفأرية، أدى إجبار النِكروبتوز المدفوع بـ MLKL إلى تمزق الخلايا وإفراز إشارات خطر وجزيئات التهابية. هذه الإفرازات جذبت ونشّطت بقوة خلايا شبيهة بالعدلات، التي هاجرت بعد ذلك نحو الخلايا العضلية المحتضرة. عندما أضيف مركب يثبّط MLKL، قلّ كل من موت الخلايا العضلية الملساء والتنشيط الناتج للعدلات.
طريق محتمل جديد لإيقاف نمو الأم الدم
بجمع هذه النتائج، تشير الدراسة إلى أنه عندما تموت خلايا العضلات الملساء في الأبهر بالنِكروبتوز، فهي لا تختفي ببساطة؛ بل تستدعي بنشاط الخلايا المناعية وتشعل دورة من الالتهاب وتفكك الأنسجة التي تدفع نمو الأم الدم. يؤدي إزالة أو تعطيل MLKL في الفئران إلى مقاطعة هذه الدورة، محافظًا على جدار الوعاء ومحدودًا لتكوّن الأم الدم. بالنسبة للمرضى، يفتح ذلك احتمال أن تدخلات دوائية مستقبلية تستهدف MLKL قد تبطئ أو تمنع الأم الدم الأبهرية البطنية، مقدّمة بديلاً طبيًا لـ«المراقبة اليقظة» والجراحة في المراحل المتأخرة. بينما هذه العلاجات غير متاحة بعد، يرسم هذا العمل هدفًا جزيئيًا ملموسًا لحماية أحد أهم أوعية الدم في الجسم.
الاستشهاد: Nemade, H., Mehrkens, D., Lottermoser, H.S. et al. Loss of MLKL impairs abdominal aortic aneurysm development by attenuating smooth muscle cell necroptosis. Cell Death Dis 17, 217 (2026). https://doi.org/10.1038/s41419-026-08427-4
الكلمات المفتاحية: أم الدم الأبهرية البطنية, نخر الخلايا المبرمج (نِكروبتوز), الخلايا العضلية الملساء, تثبيط MLKL, التهاب الأوعية الدموية