Clear Sky Science · ar
يحفّز الحمض النووي الميتوكوندري محور NLRP3-IL-1β في الخلايا الميكروغلية عبر الارتباط بـ NLRP3، مما يؤدي إلى تنكس عصبي في نماذج مرض باركنسون
لماذا هذا مهم لمرض باركنسون
يشتهر مرض باركنسون بالارتعاش وبطء الحركة، لكن تحت هذه الأعراض تدور معركة معقدة داخل الدماغ. يكشف هذا البحث كيف أن شظايا صغيرة من المادة الوراثية المأخوذة من ميتوكوندريا تالفة في خلايا المناعة الدماغية يمكن أن تشعل التهابًا يقضي تدريجيًا على الخلايا العصبية المنتجة للدوبامين اللازمة لحركة سلسة. فهم هذا التسلسل يفتح أهدافًا دوائية جديدة ومحددة قد تبطئ أو تمنع التلف الشبيه بمرض باركنسون.
خلايا المناعة الدماغية ومحطات الطاقة تحت الضغط
يحتوي الدماغ ليس فقط على العصبونات، بل أيضًا على الخلايا الميكروغلية، وهي خلايا المناعة المقيمة فيه. في مرض باركنسون، تصبح هذه الخلايا الميكروغلية غالبًا مفرطة النشاط، مطلقة جزيئات سامة وإشارات التهابية تضر بالخلايا العصبية المجاورة. ركز المؤلفون على الميتوكوندريا، «محطات الطاقة» في الخلايا، التي تحمل حمضًا نوويًا خاصًا بها. عندما تتعرض الميتوكوندريا لإصابة—بسبب السموم أو الشيخوخة أو ضغوط أخرى—قد يتأكسد حمضها النووي، وهو شكل من أشكال التلف الكيميائي الناتج عن أنواع الأكسجين التفاعلية. وبما أن حمض الميتوكوندريا النووي يشبه حمض البكتيريا، يمكن للشظايا المتضررة أن تعمل كإشارات إنذار داخل الدماغ، منبهة جهاز المناعة ومحتملة الدفع نحو التهاب مزمن.
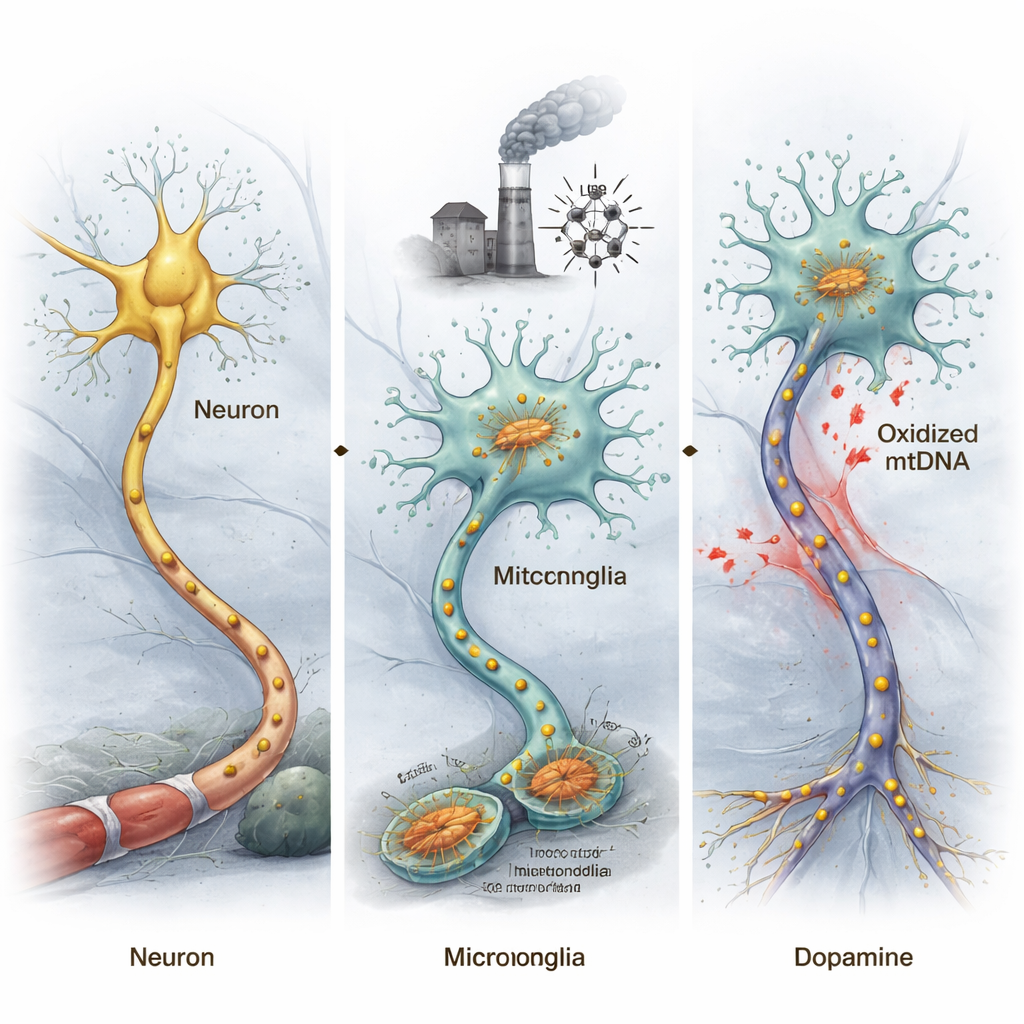
يمكن للحمض النووي الميتوكوندري المتأكسد أن يدفع الفئران نحو مرض شبيه بباركنسون
لاختبار ما إذا كان حمض الميتوكوندريا المؤكسد (ox-mtDNA) قادرًا فعليًا على إحداث تغييرات شبيهة بباركنسون، استخلص الباحثون ox-mtDNA من خلايا ميكروغلية متوترة وحقنوه مباشرة في منطقة دماغية تحتوي عادة خلايا منتجة للدوبامين مهمة للحركة. أظهرت الفئران المعرضة لهذا الحمض النووي المتأكسد انخفاضًا في الحركة في اختبارات السلوك وفقدانًا لهذه الخلايا المنتجة للدوبامين، بما يعكس سمات أساسية لمرض باركنسون. من خلال فصل الخلايا العصبية والميكروغلية من المساحة المتوسطة في الدماغ وتحليل نشاط الجينات فيها، وجد الفريق أن الجينات المرتبطة بمرض باركنسون أصبحت أكثر اضطرابًا في الخلايا العصبية، بينما تنشطت جينات مرتبطة بالالتهاب بقوة في الخلايا الميكروغلية.
مفتاح إنذاري جزيئي داخل الميكروغليا
ركزت الدراسة على مركب بروتيني في الميكروغليا يُدعى NLRP3، وهو جزء من مجموعة أكبر تُعرف بالإنفلاماسوم. عند تشغيله، يساعد NLRP3 على تفعيل الكاسباز-1، إنزيم يقص الجزيء الالتهابي IL-1β إلى شكله النشط والضار. في الفئران وفي الخلايا المستزرعة، أدى الجمع بين إشارة تمهيدية التهابية (LPS، مكوّن بكتيري) وسم يشبه المبيدات الحشرية (روتينون) إلى إطلاق الميتوكوندريا في الميكروغليا لحمضها النووي المتأكسد إلى سيتوبلازم الخلية. تزامن هذا الإصدار مع تنشيط أقوى لـ NLRP3، ومزيد من كاسباز-1 المقطوع (النشط)، وارتفاع مستويات IL-1β. الوسط الثقافي المأخوذ من هذه الميكروغليا المفرطة النشاط كان سامًا مباشرة للخلايا المشابهة للدوبامين المزروعة في طبق، مما خفض بقائها ومستوى علامة رئيسية لها، التيروسين هيدروكسيلاز.
الارتباط المباشر: كيف يقلب الحمض النووي المؤكسد مفتاح NLRP3
علاوة على الارتباط البسيط، أظهر المؤلفون أن ox-mtDNA ليس حاضرًا أثناء الالتهاب فحسب—بل يبدو أنه يرتبط جسديًا بـ NLRP3 ويشغّله. عندما منعوا إفراز حمض الميتوكوندريا النووي بعقار، انخفض تنشيط كاسباز-1 وIL-1β. وبالعكس، أدى توصيل حمض الميتوكوندريا المؤكسد مباشرة إلى الميكروغليا إلى تعزيز كبير في إشارة NLRP3، أكثر من حمض الميتوكوندريا غير المؤكسد. باستخدام تجارب سحب حيوية كيميائية، اكتشفوا mtDNA غنيًا بعلامات التلف التأكسدي ملتصقًا بـ NLRP3. وأظهرت النمذجة الحاسوبية وكيمياء البروتين أن ox-mtDNA يرتبط بقسم موجب الشحنة ومرن في NLRP3 (منطقة «غير منظمة ذاتيًا» تمتد عند الأحماض الأمينية 180–187). عندما أزيل هذا المقطع الحاسم من NLRP3، انخفضت قدرته على ربط ox-mtDNA وتنشيط كاسباز-1 بشكل كبير.
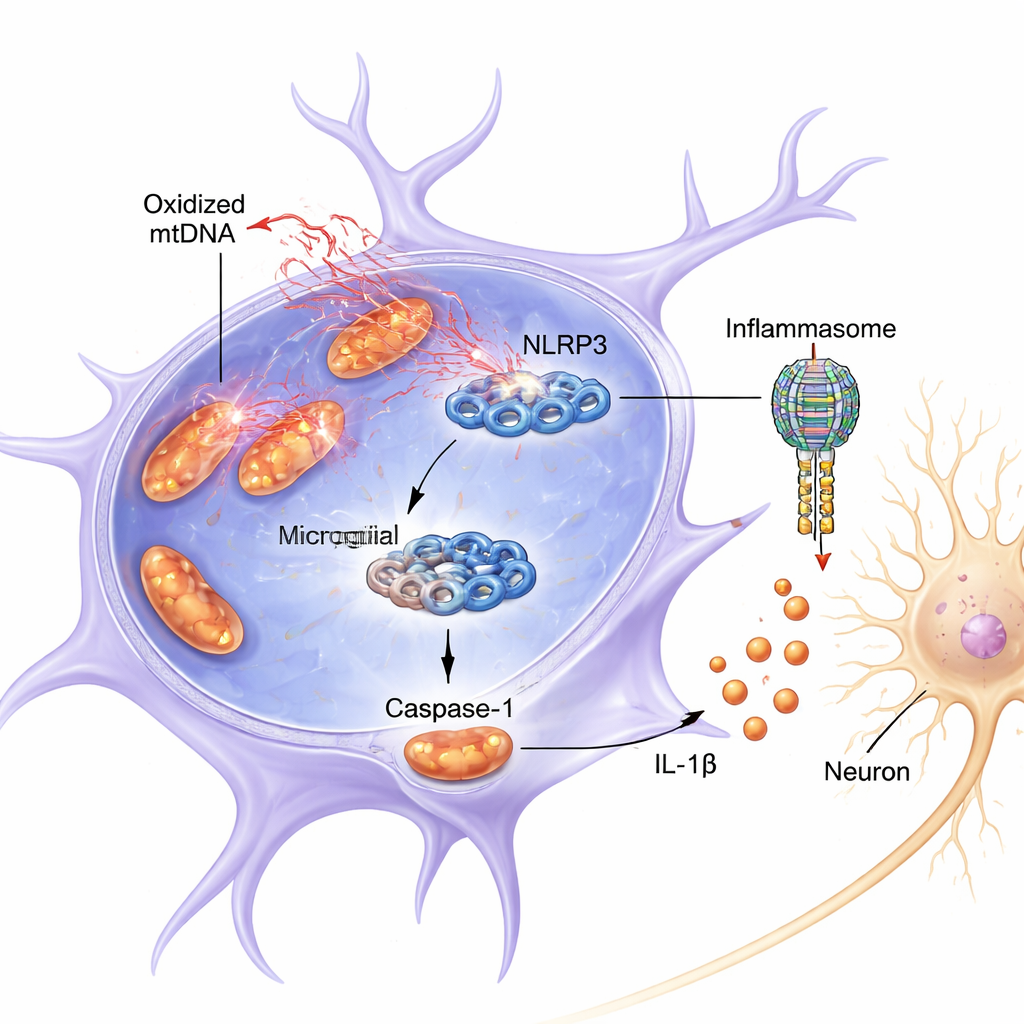
إطفاء الإنفلاماسوم يحفظ الخلايا العصبية
سأل الباحثون بعد ذلك ما إذا كان التدخل في NLRP3 يمكن أن يحمي الخلايا العصبية. في الميكروغليا المستزرعة، أدت الخفض الجيني لـ NLRP3 إلى تقليل حاد في تنشيط كاسباز-1 وIL-1β بعد معالجة بـ LPS وروتينون، وكان الوسط المكيف من هذه الخلايا أقل سمية بكثير للخلايا الشبيهة بالدوبامين. في الفئران، خفّض مثبط انتقائي لـ NLRP3 (MCC950) تنشيط الميكروغليا، وحفظ خلايا الدوبامين، وخفض البروتينات المرتبطة بالإنفلاماسوم في نماذج نُشطت إما بواسطة LPS مع روتينون أو بواسطة حقن mtDNA. معًا، تُظهر هذه التجارب أن سلسلة ox-mtDNA–NLRP3–IL-1β ليست مرتبطة بالتلف فحسب؛ بل هي مطلوبة لمعظم الفقدان العصبي الملحوظ.
ما يعنيه هذا لعلاجات باركنسون المستقبلية
للغير متخصصين، الرسالة الأساسية هي أن الحمض النووي الميتوكوندري التالف المتسرب من خلايا المناعة الدماغية يمكنه الالتحام مباشرة بمفتاح إنذار داخلي (NLRP3)، مسببًا موجة من الالتهاب التي تضر خلايا الدوبامين وتقود إلى مرض شبيه بباركنسون في النماذج. وبما أن هذا التفاعل يعتمد على مقطع قصير ومحدد من بروتين NLRP3 وعلى الطبيعة المؤكسدة لحمض الميتوكوندريا النووي، فإنه يوفر أهدافًا دوائية دقيقة. قد تُبرد العلاجات التي تمنع تلف أو هروب حمض الميتوكوندريا النووي، أو تمنع ارتباطه بـ NLRP3، أو تثبط NLRP3 نفسه، هذا التدفق الالتهابي وتبطئ تقدم مرض باركنسون.
الاستشهاد: Gan, Q., Fu, X., Zhou, T. et al. Mitochondrial DNA drives NLRP3-IL-1β axis activation in microglia by binding to NLRP3, leading to neurodegeneration in Parkinson’s disease models. Cell Death Dis 17, 213 (2026). https://doi.org/10.1038/s41419-026-08424-7
الكلمات المفتاحية: مرض باركنسون, الخلايا الميكروغلية, الحمض النووي الميتوكوندري, الإنفلاماسوم NLRP3, الالتهاب العصبي