Clear Sky Science · ar
لاكتلة SLC26A3 في بيئة الورم الحمضية تعزز التقدم الخبيث لسرطان القولون والمستقيم
لماذا تهم حمضية الورم
يظل سرطان القولون والمستقيم أحد أكثر السرطانات فتكا على مستوى العالم، جزئياً لأن الأورام غالباً ما تعود أو تنتشر أو تتوقف عن الاستجابة للأدوية. تستكشف هذه الدراسة سبباً مُهمَلاً جزئياً وراء هذا السلوك: بيئة الأورام الحمضية الغنية بحمض اللاكتيك. من خلال كشف كيفية تسبب هذه البيئة القاسية في زعزعة استقرار بروتين غشائي حمائي يُدعى SLC26A3، يكشف المؤلفون سلسلة أحداث جديدة تساعد خلايا السرطان على اكتساب صفات أكثر شبهاً بالخلايا الجذعية، وتصبح أكثر غزوًا ومقاومة للأدوية — ما يقدّم أفكاراً علاجية جديدة.
حي قاسٍ حول خلايا السرطان
تستهلك الأورام سريعة النمو كميات كبيرة من السكر والأكسجين، مطلقة حمض اللاكتيك وأيونات الهيدروجين التي تجعل البيئة المحيطة بها حمضية. باستخدام مجموعات بيانات مرضى واسعة وعينات نسيجية، تُظهر الباحثون أن هذه الحالة الحمضية، التي يتتبعها بروتين علامة يُدعى CA9، ترتبط بأورام القولون والمستقيم العدوانية. في السرطانات الأكثر تقدماً، تكون مستويات CA9 مرتفعة، بينما تكون مستويات SLC26A3 منخفضة باستمرار. عادةً ما يتوضع SLC26A3 على سطح خلايا القولون ويسهم في توازن الأملاح والبيكربونات، مما يساعد بدوره على ضبط الحموضة. في عينات الأورام وخطوط الخلايا وتحليل الخلايا المفردة، يجد الفريق أنه عندما ترتفع الحمضية، تنخفض مستويات SLC26A3 — لا سيما في الخلايا الخبيثة الشبيهة بالخلايا الجذعية. 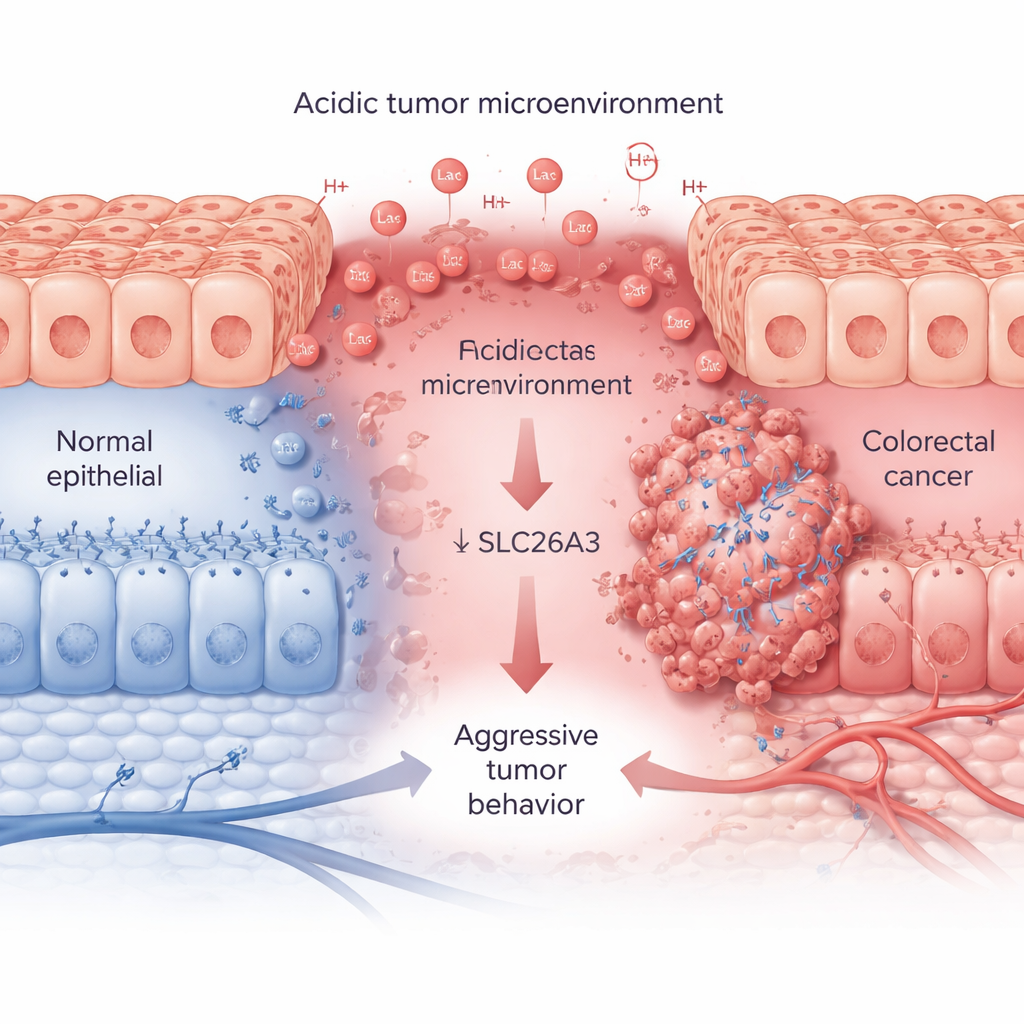
كيف يعلّم حمض اللاكتيك هدفاً للتدمير
ثم يتساءل المؤلفون لماذا ينخفض SLC26A3 في الأورام الحمضية. يركزون على اللاكتلة، وهي علامة كيميائية اكتشفت حديثاً تتكون من حمض اللاكتيك ويمكن إضافتها إلى البروتينات. عندما تتعرض خلايا سرطان القولون والمستقيم لحمض اللاكتيك أو تُنمى في ظروف حمضية، يصبح SLC26A3 مشبعاً باللاكتلة. يحدد التحليل البروتيني التفصيلي موضعاً أساسياً واحداً، وهو الحمض الأميني المسمى K536، حيث تُضاف هذه العلامة. تجعل اللاكتلة عند K536 SLC26A3 أقل استقراراً: يصبح البروتين أكثر عرضة لأن يُعلّم باليوبيكويتين، إشارة خلوية لـ"تخلص من هذا"، ويُرسل إلى آلية إعادة التدوير داخل الخلية. حجب الإنزيم p300، الذي يساعد على إضافة علامات اللاكتلة، يحمي جزئياً SLC26A3 من التحلل. نتيجة لذلك، تهيئ الحمضية واللاكتات حلقة تغذية راجعة ضارة — المزيد من اللاكتات يؤدي إلى المزيد من اللاكتلة، مما يقلل SLC26A3، ويُخلّ بتوازن درجة الحموضة ويعزز بيئة مجهرية أكثر حمضية.
إطفاء فرامل التميز الجذعي وانتشار السرطان
مع استنفاد SLC26A3، تتصرف خلايا السرطان بشكل أكثر عدوانية. في الثقافة الخلوية، تعبر خلايا سرطان القولون والمستقيم الشبيهة بالخلايا الجذعية بطبيعتها عن مستويات أقل من SLC26A3 مقارنة بنظرائها غير الشبيهة بالجذع. عندما يخفض الباحثون عمداً مستويات SLC26A3، تُكوّن الخلايا الورمية مزيداً من الكرات (علامة على التميز الجذعي)، وتتجدد بكفاءة أعلى، وتغزو عبر أغشية صناعية، وتهاجر بسرعة أكبر عبر جروح القشط. كما تصبح أقل حساسية لأدوية العلاج الكيميائي الشائعة مثل أوكساليبلاتين و5‑فلورويوراسيل. على العكس من ذلك، يؤدي تعزيز SLC26A3 إلى خفض علامات التميز الجذعي وإبطاء الغزو والهجرة — لكن هذه الفائدة تقل عندما يُضاف لاكتات إضافي، مؤكدةً كيف يمكن للحمضية أن تتغلب على التأثير الوقائي.
رابط خفي بالتحكم في الجينات
فضلاً عن دوره في تنظيم الحموضة، يعمل SLC26A3 أيضاً كهيكل يرتبط ببروتينين ناقلين للـRNA، هما HuR وCUGBP1. تتحكم هذه البروتينات في مدة بقاء العديد من الرناّات الرسولية التي ترمز لبروتينات ذات صلة بالسرطان. عندما يتوفر SLC26A3 بكثرة، فإنه يحجز بعض HuR وCUGBP1، مما يحد من مدى قدرتهما على تثبيت أو إضعاف بعض الرسائل المرتبطة بالسرطان. عندما يفقد SLC26A3 نتيجة اللاكتلة والتحلل، يصبح HuR وCUGBP1 أحراراً في الارتباط بالرناّات المرساليات المسرطنة التي تعزز التميز الجذعي، والانتقال الطلائي-اللحمي (EMT)، والغزو، والبقاء. تُظهر التجارب أن HuR يساعد على تثبيت رناّات مرسال لعلامات التميز الجذعي وبروتينات وصل الخلايا، بينما يمكن أن يعارض CUGBP1 HuR لبعض الأهداف، مما يقلل من تكامل الوصلات ويشجع EMT — وكلاهما يفضي إلى انتشار الورم.
إعادة موازنة البيئة لمحاربة السرطان
لاختبار ما إذا كان يمكن تحويل هذه الرؤى إلى استراتيجيات علاجية، يستخدم الباحثون نماذج فأرية لسرطان القولون والمستقيم. تحييد حمضية الورم بمحلول بيكربونات الصوديوم، حجب نقل اللاكتات بمثبط MCT1، أو زيادة التعبير عن SLC26A3 كلها تبطئ نمو الورم. إن الجمع بين استعادة SLC26A3 والعلاج الكيميائي يقلص الأورام أكثر. في بيانات المرضى، ترتبط مستويات SLC26A3 الأعلى ببقاء أفضل، وانخفاض الانتكاس، وقلة النقائل، واستجابة أفضل للعلاج الكيميائي، مما يشير إلى أن هذا البروتين قد يكون علامة حيوية وهدفاً علاجياً محتملاً. 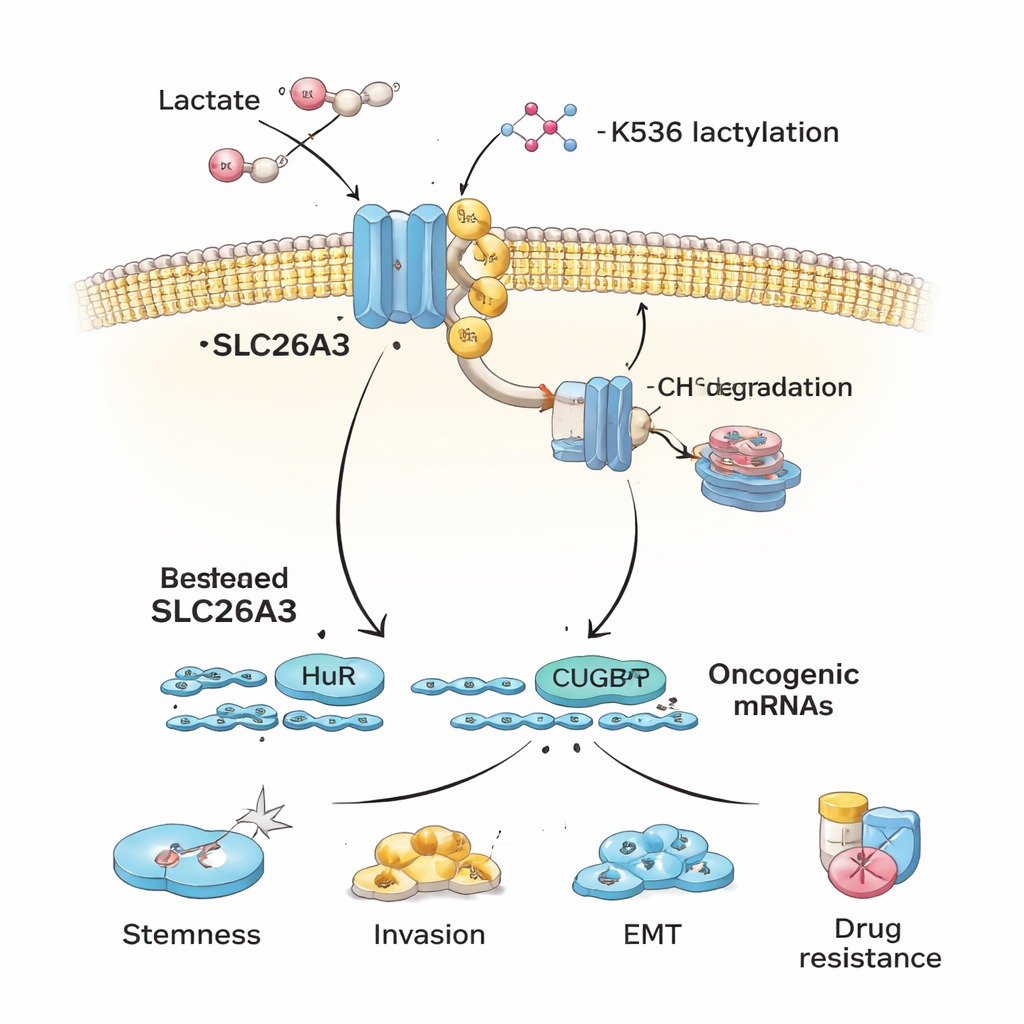
ماذا يعني هذا للمرضى
بعبارات بسيطة، تُظهر هذه الدراسة أن أورام القولون والمستقيم تزدهر في حمام حمضي غني بحمض اللاكتيك يعلّم كيميائياً ويدمر حاجز حماية يُدعى SLC26A3. بمجرد زوال هذا الحارس، تتبنى خلايا السرطان بسهولة أكبر صفات شبيهة بالخلايا الجذعية، وتنتشر، وتقاوم العلاج، بمساعدة منظِّمي الرناّات الأقوياء داخل الخلية. من خلال عزل حمضية الورم، حجب معالجة اللاكتات، أو استعادة SLC26A3، قد يكون من الممكن إضعاف حلقة التغذية الراجعة الخبيثة هذه وجعل العلاجات القياسية أكثر فعالية. بينما تحتاج مثل هذه المقاربات لمزيد من الاختبارات السريرية المتأنية، فإنها تفتح زاوية واعدة حول كيفية إدارة البيئة الكيميائية للورم للمساعدة في السيطرة على سرطان القولون والمستقيم.
الاستشهاد: Chen, C., Cai, D., Liu, X. et al. Lactylation of SLC26A3 in the acidic tumor microenvironment promotes malignant progression of colorectal carcinoma. Cell Death Dis 17, 164 (2026). https://doi.org/10.1038/s41419-026-08422-9
الكلمات المفتاحية: سرطان القولون والمستقيم, البيئة المجهرية للورم, اللاكتلة, خلايا السرطان الجذعية, مقاومة العلاج الكيميائي