Clear Sky Science · ar
استهداف GNG4 يثبط تقدم الورم ويستعيد حساسية الإنسالوتاميد في سرطان البروستاتا عن طريق قمع الالتهام الذاتي
لماذا تهمّ هذه الدراسة
بالنسبة للعديد من الرجال المصابين بسرطان البروستاتا المتقدم، تعمل أدوية حاصرة للهرمونات قوية مثل الإنسالوتاميد جيدًا في البداية لكنها تفقد فعاليتها تدريجيًا. تكشف هذه الدراسة عن حيلة بقاء خفية تستخدمها خلايا الورم وتشير إلى بروتين محدد يُدعى GNG4 يساعد الأورام على الاستمرار في النمو والتغلب على العلاج. قد يؤدي فهم هذه الآلية إلى علاجات مركبة تجعل الأدوية الحالية أكثر فعالية ولمدة أطول.
مفتاح بروتيني ظاهر للعيان
تعتمد خلايا سرطان البروستاتا بشكل كبير على الهرمونات الذكرية، لذا يهدف العلاج القياسي للمرض المتقدم إلى قطع هذه الإشارات. ومع ذلك تصبح معظم الأورام في النهاية «مقاومة للاستئصال الهرموني» وتبدأ في النمو من جديد. بحث المؤلفون عن جينات كانت أكثر نشاطًا بكثير في نسيج الورم مقارنة بالنسيج البروستاتا الطبيعي المجاور من نفس المرضى. من بين عدة مرشحين، برز GNG4: عندما قلّلوا مستوياته في خلايا سرطان البروستاتا انخفض نمو الخلايا بشكل حاد. أكدت تحليلات مئات عينات المرضى أن GNG4 أعلى في سرطانات البروستاتا الأولية منه في النسيج الطبيعي ويزداد بشكل خاص في الأورام الأكثر عدوانية وذات الدرجة الأعلى.
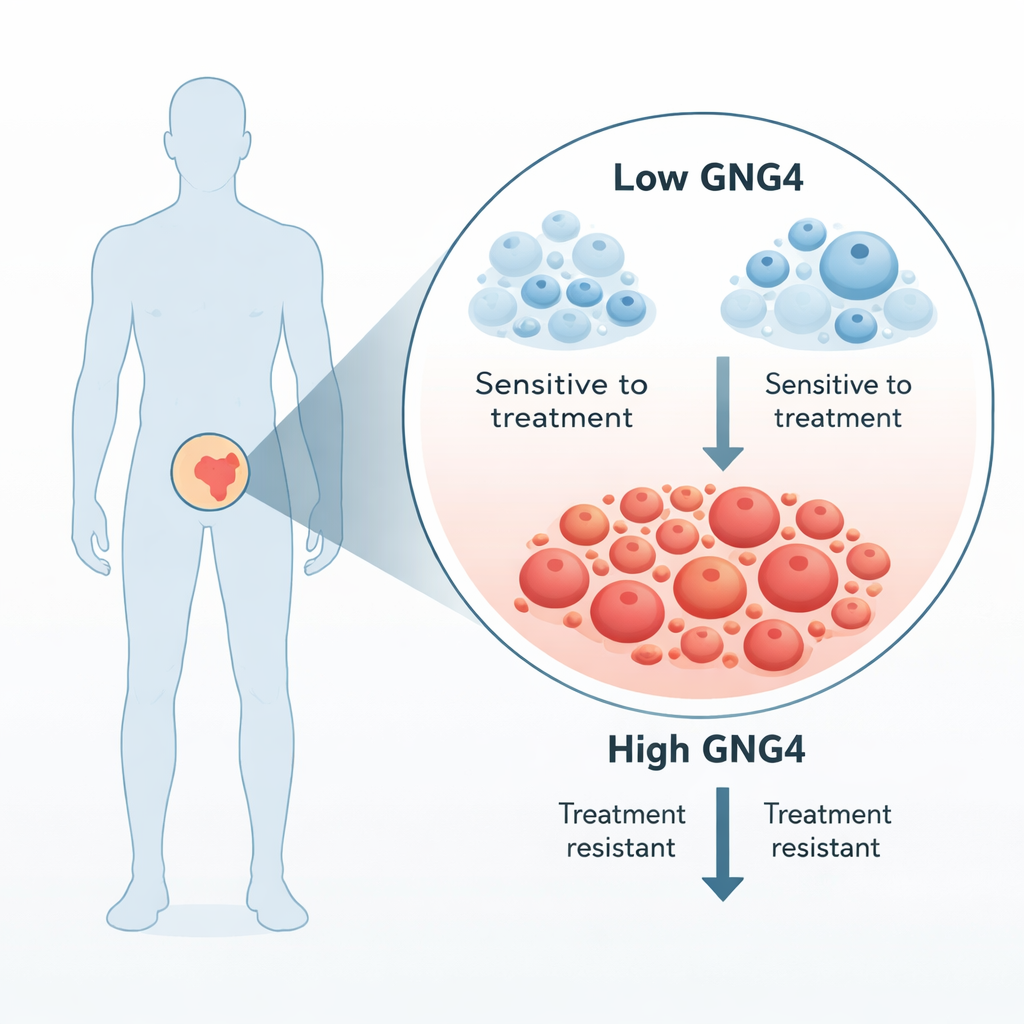
كيف يساعد GNG4 الأورام على الازدهار
ينتمي GNG4 إلى عائلة إشارات أكبر تعرف ببروتينات G، والتي تقع في غشاء الخلية وتنقل الإشارات من الخارج إلى داخل الخلية. أظهرت المجموعة أن خفض GNG4 في خطوط خلايا سرطان البروستاتا أبطأ انقسام الخلايا، ودفع الخلايا للتوقف في طور تفتيش من دورة الخلية، وزاد من موت الخلايا المبرمج. قلّلت هذه التغيرات أيضًا من قدرة الخلايا السرطانية على الهجرة وإغلاق الجروح في تجارب المختبر، ونمت الأورام المتشكلة من خلايا ناقصة GNG4 بشكل أبطأ في الفئران. مجتمعة تشير هذه النتائج إلى أن GNG4 يعمل كدواسة تسارع لنمو وانتشار سرطان البروستاتا.
الالتهام الذاتي: مخزن طوارئ خلية السرطان
ركز الباحثون بعد ذلك على عملية تسمى الالتهام الذاتي، التي تكسر فيها الخلايا مكوناتها وتعيد تدويرها لتنجو من الضغوط، مثل الجوع أو العلاج الدوائي. في العديد من السرطانات المتقدمة، يعمل الالتهام الذاتي كمخزن طوارئ يساعد خلايا الورم على التكيّف مع الظروف الصعبة. في هذه الدراسة، أظهرت خلايا سرطان البروستاتا ذات النشاط العالي لـ GNG4 مزيدًا من علامات الالتهام الذاتي النشط، بينما كانت الخلايا التي تم فيها خفض GNG4 تحتوي على هياكل إعادة التدوير أقل ومستويات أدنى من علامات الالتهام الذاتي الرئيسية. عندما زاد إنتاج GNG4، تحمّلت الخلايا الإنسالوتاميد أفضل وخضعت لموت خلوي أقل. إيقاف الالتهام الذاتي بمثبط كيميائي أزال الكثير من هذا الحماية، مما يشير إلى أن GNG4 يساعد الأورام على تحمل العلاج إلى حد كبير عن طريق تعزيز هذا النظام التدويري.
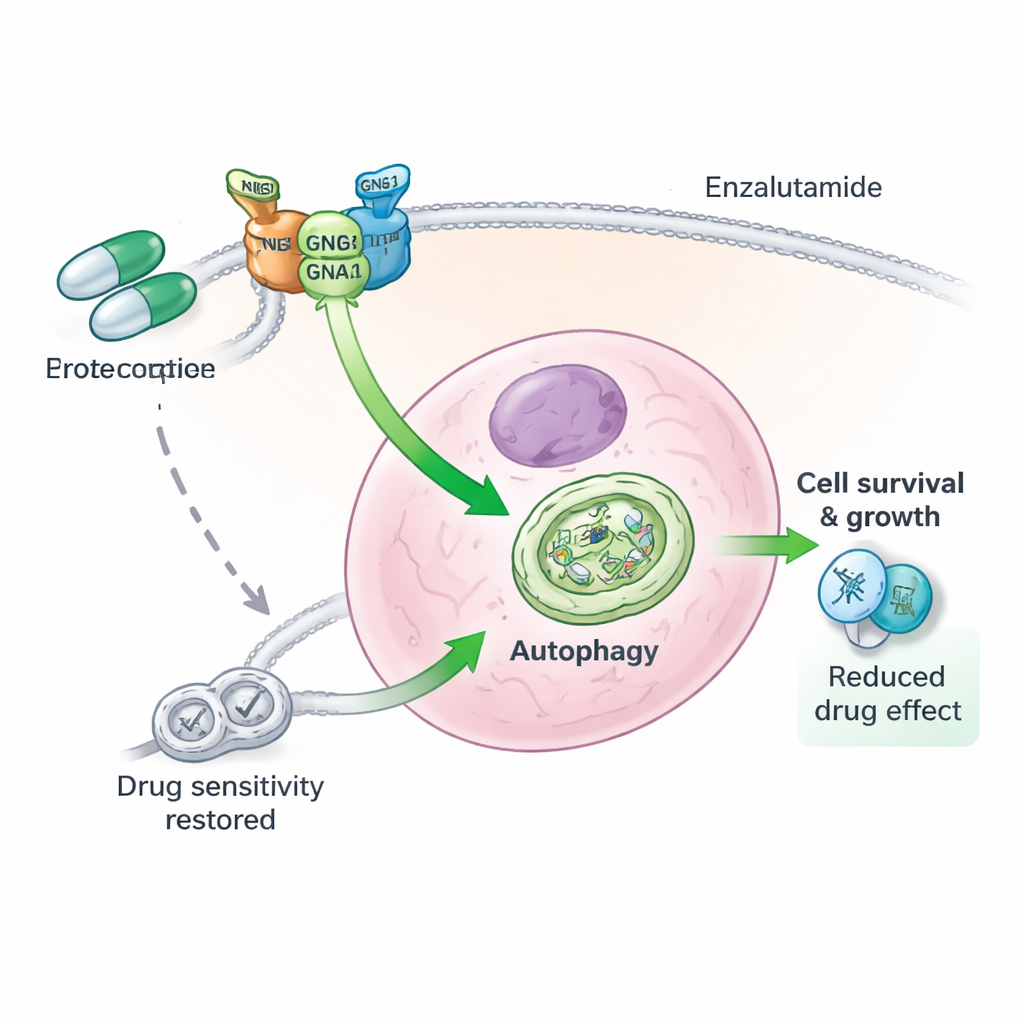
فريق بروتيني ثلاثي وراء مقاومة الدواء
بتعمق أكثر، اكتشف المؤلفون أن GNG4 لا يعمل بمفرده. يرتبط فعليًا بمكوّن آخر من بروتينات G، وهو GNB1، ليُثبّت بروتينًا ثالثًا هو GNAI3. معًا تُشكّل هذه الوحدات الثلاث مركبًا وظيفيًا يعزّز الالتهام الذاتي داخل خلايا سرطان البروستاتا. عندما قلّلوا GNG4، وُسم بروتين GNAI3 بشكل أسرع للتدمير وتفكك بواسطة آليات التخلص من الفضلات داخل الخلية، مما أوقف إشارة الالتهام الذاتي. إلغاء GNAI3 نفسه ألغى مزايا النمو والبقاء التي يوفرها GNG4 الزائد، سواء في الخلايا المستزرعة أو في أورام الفئران. بعبارة أخرى، يقود GNG4 الخباثة ومقاومة الضغط إلى حد كبير عبر محور GNG4–GNB1–GNAI3 هذا.
جعل الأدوية الحالية أكثر فعالية
أخيرًا، سأل الفريق ماذا يحدث عندما يُدمج استهداف GNG4 مع الإنسالوتاميد، الدواء الرائد لسرطان البروستاتا المتقدم. في المختبر، جعل خفض GNG4 الخلايا السرطانية أكثر حساسية للإنسالوتاميد بشكل ملحوظ وقلّل من قدرتها على تشكيل مستعمرات بعد العلاج. في الفئران، انكمشت الأورام منخفضة GNG4 أكثر عند إعطاء الإنسالوتاميد مقارنة بالأورام ذات مستويات GNG4 الطبيعية، دون سمية إضافية واضحة. إنتاج نتائج مماثلة عن طريق حجب الالتهام الذاتي مباشرة. تشير هذه النتائج إلى أن تعطيل الالتهام الذاتي المدفوع بـ GNG4 يمكن أن يسلب خلايا الورم آلية تكيف حيوية، مما يسمح للعلاجات الحاصرة للهرمونات الحالية بتوجيه ضربة أقوى وأكثر دوامًا.
ماذا يعني هذا للمرضى
لغير المتخصصين، الرسالة الرئيسية أن بعض سرطانات البروستاتا تنجو من العلاج عن طريق تشغيل نظام داخلي لإعادة التدوير يعمل كمولد احتياطي. تحدد هذه الدراسة GNG4 كمفتاح رئيسي يشغّل هذا النظام، ويعمل مع بروتينات شريكة لحماية خلايا السرطان من الإنسالوتاميد. من خلال إيقاف هذا المفتاح — إما باستهداف GNG4 مباشرة أو بخفض الالتهام الذاتي بأمان — قد تتمكن العلاجات المستقبلية من إبطاء نمو الورم واستعادة حساسية الدواء لدى الرجال الذين أصبحت سرطاناتهم صعبة العلاج.
الاستشهاد: Chen, L., Zhang, J., Hu, Y. et al. Targeting GNG4 inhibits tumor progression and restores enzalutamide sensitivity in prostate cancer by suppressing autophagy. Cell Death Dis 17, 160 (2026). https://doi.org/10.1038/s41419-026-08421-w
الكلمات المفتاحية: سرطان البروستاتا, مقاومة الأدوية, الالتهام الذاتي, بروتينات G, الإنسالوتاميد