Clear Sky Science · ar
تنسيق DNA-PKcs لشيخوخة الخلايا الناتجة عن نضوب CTLA-4 في خلايا السرطان
تحويل مفتاح نمو السرطان إلى إشارة توقف
تركز أدوية السرطان المناعية غالبًا على جزيء يُدعى CTLA-4 الموجود على خلايا الجهاز المناعي لمساعدة الجسم على مهاجمة الأورام. تكشف هذه الدراسة منعطفًا مفاجئًا: يوجد CTLA-4 أيضًا داخل خلايا السرطان نفسها ويمكن أن يعمل كمساعد نمو خفي. عندما أزال الباحثون هذا الـ CTLA-4 الداخلي عمدًا من خلايا الميلانوما، توقفت خلايا السرطان عن التكاثر ودخلت في حالة «تقاعد» طويلة الأمد تُعرف بالشيخوخة الخلوية. يوفر فهم هذا الدور غير المتوقع طرقًا جديدة لإبطاء أو حتى تقليص الأورام من خلال استهداف CTLA-4 داخل خلايا السرطان، وليس فقط على خلايا الجهاز المناعي.
عندما تختار الخلايا التقاعد بدل النمو الجامح
تنقسم الخلايا عادةً، تصلح نفسها، وعندما تتعرض لضرر لا يُصلح إما أن تموت أو تدخل في الشيخوخة، وهي توقف دائم لنموها. تميل الخلايا المسنة لأن تكبر حجمًا، وتتغير في الشكل، وتنتج علامات مميزة يمكن للباحثين كشفها في المختبر. وجد الباحثون أنه عندما خفضوا مستوى CTLA-4 داخل خلايا الميلانوما لدى الفأر والإنسان، أصبحت الخلايا أكبر، وانخفض نموها بشدة، وارتفعت إشارات الشيخوخة الكلاسيكية، بما في ذلك إنزيمات يمكن كشفها بصبغات خاصة وبروتينات مثل p16 وp21 اللذين يوقفان دورة الخلية. لوحِظت هذه التغيرات سواء عند كبت CTLA-4 مؤقتًا أو عند حذفه نهائيًا باستخدام أدوات تحرير الجينات.
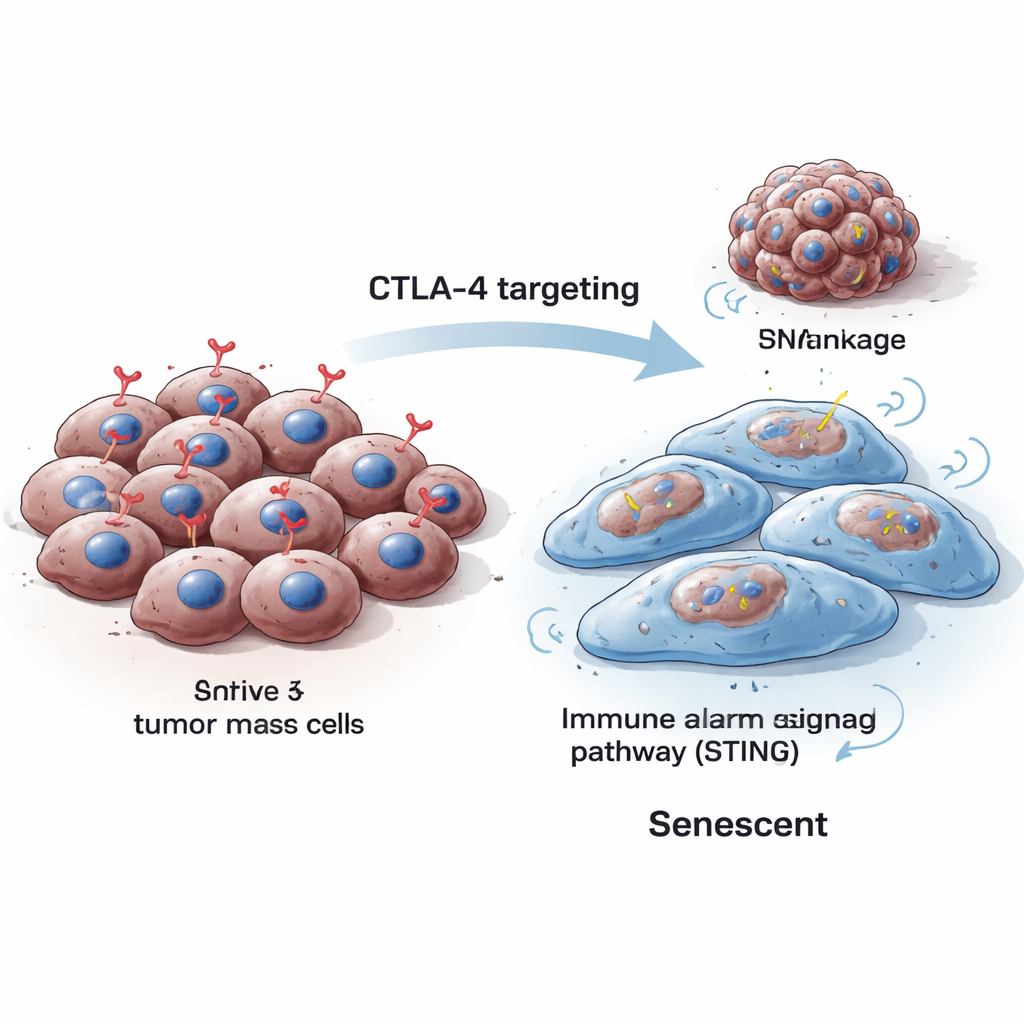
تشقق المخطط الجيني يقود إلى توقف
لفهم سبب دفع فقدان CTLA-4 خلايا السرطان إلى الشيخوخة، نظر الفريق في كيفية تعامل هذه الخلايا مع حمضها النووي أثناء الانقسام. اكتشفوا أن نضوب CTLA-4 خفض مستويات Aurora B، وهو بروتين يساعد على فصل الكروموسومات بسلاسة عند انقسام الخلايا. عندما انخفض Aurora B، طورت الخلايا عدم استقرار جيني: ظهرت أجسام دقيقة تحتوي على DNA تُدعى النوى الصغرى، وزادت علامات تلف الحمض النووي. يُعرف أن هذا النوع من الضغط على الحمض النووي يدفع الخلايا نحو الشيخوخة بدل النمو غير المنضبط. ومن المهم أن إعادة Aurora B قللت من هذه النوى الصغرى، مما يربط فقدان CTLA-4 مباشرة بسوء معالجة الكروموسومات وتلف الحمض النووي.
ضرر الحمض النووي يشغل شبكة إنذار داخلية
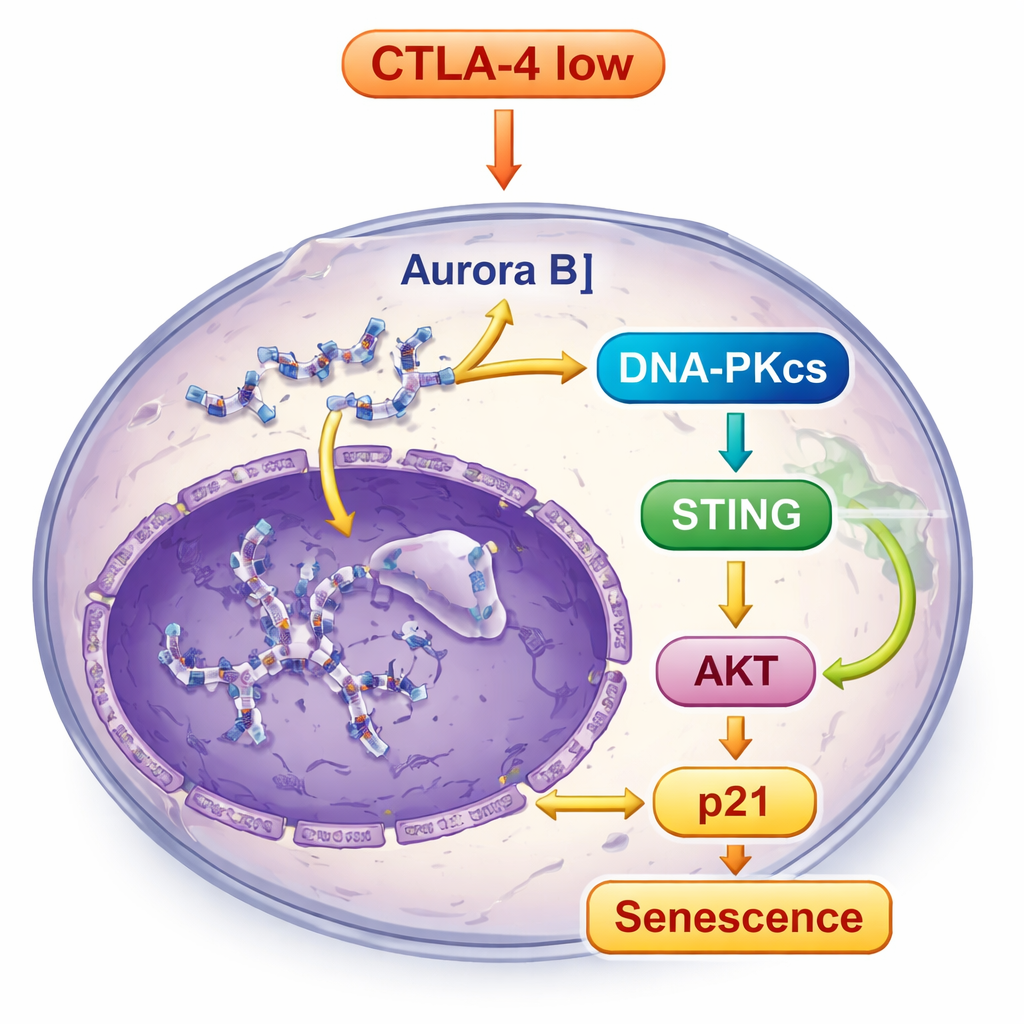
لم يغب الحمض النووي المكسور والغير في موضعه في الخلايا المنقوصة من CTLA-4 عن الانتباه. فقد فعّل مستقبل تلف الحمض النووي DNA-PKcs، والذي بدوره أطلق مسار STING، وهو نظام إنذار داخلي يستجيب لوجود DNA طليق داخل الخلايا. بمجرد تنشيط STING، أرسل إشارات إلى جزيئات أسفل السلسلة، بما في ذلك TBK1 وIRF3، كما عزز مسار ضبط النمو الآخر المهم، مسار AKT. بدلاً من تعزيز النمو، أدت هذه الإشارات المجمعة في نهاية المطاف إلى زيادة p21، الموقِّف القوي لدورة الخلية، ما يعزز حالة الشيخوخة. عندما حجب الباحثون DNA-PKcs، تقلص تنشيط STING وسمات الشيخوخة بشكل كبير، مما يظهر أن DNA-PKcs يقع في قلب هذا التسلسل الإشعاري.
من مزارع الخلايا إلى أورام في حيوانات حية
لا تحكي أطباق المختبر القصة كاملة، لذا اختبر الباحثون ما إذا كان فقدان CTLA-4 سيؤثر على أورام حقيقية في الفئران. زرعوا خلايا ميلانوما مع أو بدون CTLA-4 في جانبي نفس الحيوان. نمت الأورام الخالية من CTLA-4 بشكل أبطأ، ووزنت أقل، وكان حجمها أصغر من نظرائها المحتوية على CTLA-4. أظهرت هذه الأورام التي تفتقد CTLA-4 أيضًا تلوينًا أقوى لعلامات الشيخوخة ومستويات أعلى من تلف الحمض النووي وتنشيط مسار STING. دعمت تحليلات بيانات مرضى السرطان من قواعد بيانات عامة واسعة الصلة: عبر عدة أنواع من السرطان، كان تعبير CTLA-4 يميل لأن يكون عكسيًا لعوامل مثل DNA-PKcs ومكونات إصلاح الحمض النووي الأخرى، مما يرد صدى النتائج المخبرية في الأمراض البشرية.
ماذا يعني هذا لعلاجات السرطان المستقبلية
بشكل عام، تُظهر الدراسة أن CTLA-4 داخل خلايا السرطان يساعدها في الحفاظ على الاستقرار الجيني ومواصلة الانقسام. عند إزالة CTLA-4، تصبح الكروموسومات غير مستقرة، تتراكم شُقوق الحمض النووي، ويؤدي مسار الإنذار الداخلي—المتمركز حول DNA-PKcs وSTING—إلى دفع الخلايا نحو توقف نمو دائم. بالنسبة للقارئ العام، يعني هذا أن إيقاف CTLA-4 في خلايا الورم يدفع السرطان بعيدًا عن السلوك السريع والخطير نحو حالة «تقاعد» أكثر أمانًا. وتشير هذه الرؤى إلى أن العلاجات المستقبلية للسرطان قد تُصمم ليس فقط لتحرير الجهاز المناعي عن طريق حجب CTLA-4 على الخلايا المناعية، بل أيضًا لتعطيل الأورام مباشرة عن طريق استهداف CTLA-4 داخل خلايا السرطان واستغلال الشيخوخة كفرملة مدمجة لنمو السرطان.
الاستشهاد: Lee, JJ., Rhee, W.J., Kim, S.Y. et al. DNA-PKcs orchestrates CTLA-4 depletion-induced senescence in cancer cells. Cell Death Dis 17, 204 (2026). https://doi.org/10.1038/s41419-026-08419-4
الكلمات المفتاحية: الشيخوخة الخلوية, ميلانوما, CTLA-4, ضرر الحمض النووي, مسار STING