Clear Sky Science · ar
تنقّل TET2 بين السيتوبلازم والنواة: فرملة داخلية لتقدّم سرطان القولون والمستقيم
كيف تحمل الخلايا السرطانية فراملها الخاصة
يعد سرطان القولون والمستقيم من أكثر السرطانات شيوعًا على مستوى العالم، وغالبًا ما يتحول إلى مرض قاتل عندما تتعلم الخلايا الورمية الغزو إلى الأنسجة المجاورة والانتشار إلى أعضاء أخرى. تكشف هذه الدراسة أن الكثير من هذه الخلايا السرطانية تحمل «نظام فرملة» داخليًا — بروتينًا يُدعى TET2 — يمكنه إبطاء تقدمها عندما ينتقل إلى نواة الخلية. فهم كيف تتشغّل وتُوقَف هذه الفرملة المدمجة قد يفتح سبلًا جديدة لكبح نمو الأورام بدلاً من محاولة قتل الخلايا السرطانية فقط.
مراقبة تحرّك بروتين رئيسي داخل الخلايا الورمية
ركّز الباحثون على بروتين TET2، وهو بروتين يساعد في التحكم في تشغيل الجينات أو إيقافها عن طريق إزالة علامات كيميائية معينة من الحمض النووي. في عينات أنسجة مأخوذة من مئات مرضى سرطان القولون والمستقيم، تتبّع الباحثون موضع وجود TET2 داخل الخلايا الورمية. وجدوا أربعة أنماط رئيسية: وجوده بصورة أساسية في النواة، أو بصورة أساسية في السيتوبلازم، أو تحيّز قوي نحو أحدهما. كان المرضى الذين تحتوي أورامهم على مزيد من TET2 في النواة يميلون للعيش لفترة أطول، بينما الذين احتفظت أورامهم بـTET2 في السيتوبلازم كانوا أسوأ حالًا. ومع تقدّم السرطان إلى مراحل سريرية متأخرة، أصبح وجود TET2 النووي أقل شيوعًا، ما يوحي بأن فقدان هذا الحماية النووية يعد جزءًا من كيفية تحول الأورام إلى أكثر عدوانية.
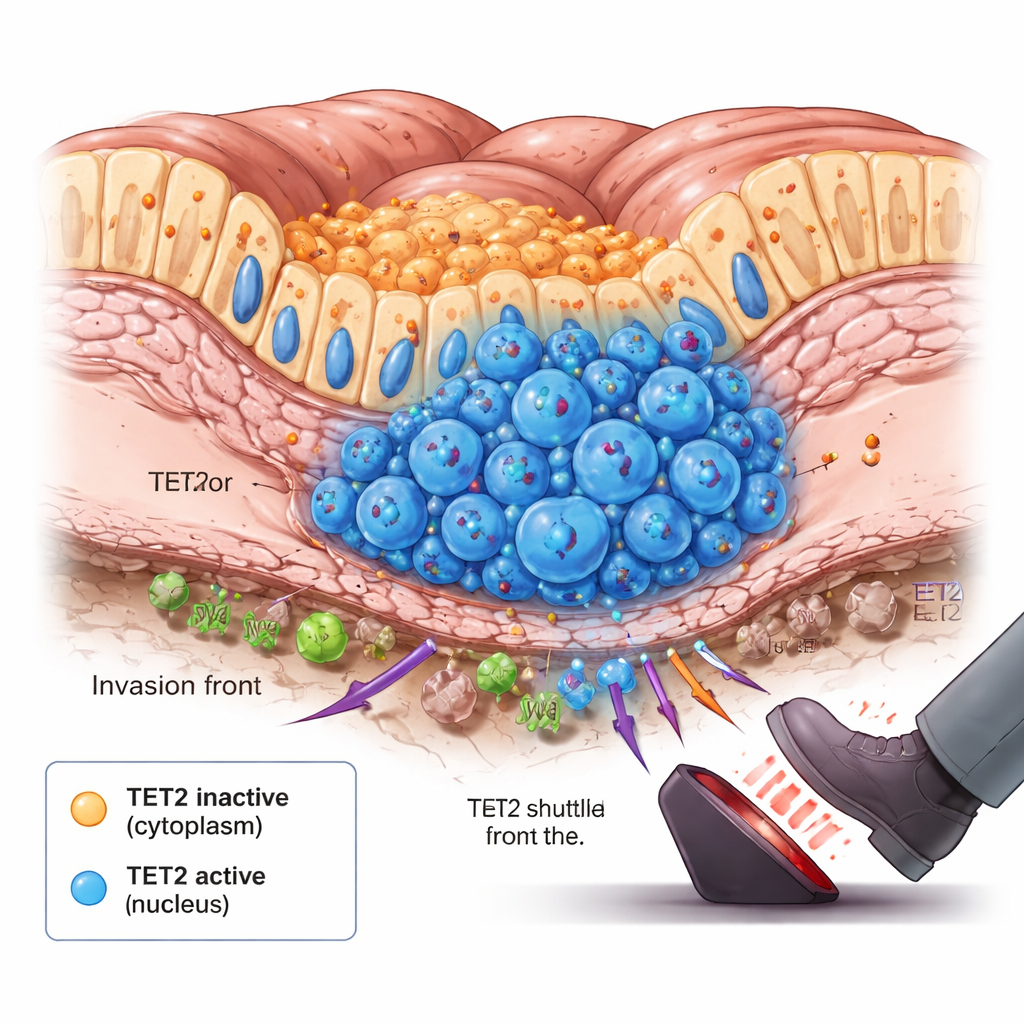
الخط الأمامي للورم ولحظة التحول
بتعمق أكبر، لاحظ الفريق أمرًا مفاجئًا: في الأورام التي كانت على وشك أن تبدأ بالانتشار، كان هناك ارتفاع طفيف في عدد الخلايا التي انتقل فيها TET2 إلى النواة. كانت هذه الخلايا تتجمع عند قاعدة بطانة الأمعاء، وهي الجبهة الغازية حيث تدفع الخلايا السرطانية لأول مرة نحو الأنسجة الأعمق. أظهرت تجارب على الحيوانات ونماذج ثقافات خلوية طويلة الأمد تحاكي نمو الورم نمطًا مشابهًا عبر الزمن. في المراحل المبكرة، ظل TET2 في السيتوبلازم وكان إلى حد كبير غير نشط. مع نمو الأورام ونفاد الأكسجين والمغذيات في المناطق الداخلية، أدت إشارات داخل الخلايا إلى دفع TET2 إلى النواة في مجموعات فرعية محددة. وبمجرد وجوده هناك، بدأ TET2 بإزالة علامات ميثلة الحمض النووي وإبطاء نمو الورم، فعمل كفرملة طارئة عندما اجتاز السرطان عتبة خطيرة.
عندما تُشغّل إشارات «انطلق» أيضًا الفرامل
تعتمد أورام القولون والمستقيم كثيرًا على برنامجين قويين يحفزان النمو: عملية تغيير الشكل المعروفة بالانتقال الظهاري–اللحمي (EMT)، التي تساعد الخلايا على أن تصبح أكثر حركة وغزوًا، ومسار إشارة WNT الذي يعزز النمو والبقاء. عادة ما تُعتبر هذه المسارات ضارة بحتًا في السرطان. ومع ذلك، تُظهر هذه الدراسة أنه عندما تشتغل EMT وWNT بقوة، فإنهما يساعدان أيضًا في دفع TET2 إلى النواة. باستخدام أدوية وأدوات جينية في ثقافات خلوية، أظهر العلماء أن تشغيل EMT أو WNT جعل مزيدًا من الخلايا تنقل TET2 إلى نواتها، بينما أدى حجب هذه المسارات إلى العكس. وبمجرد وجوده في النواة، قلّل TET2 النشط من تعبير الجينات المرتبطة بـEMT وWNT، مما خفّض هجرة الخلايا وأبطأ التكاثر. بعبارة أخرى، الإشارات نفسها التي تساعد الأورام على النمو توقظ أيضًا قوة معاكسة داخلية.
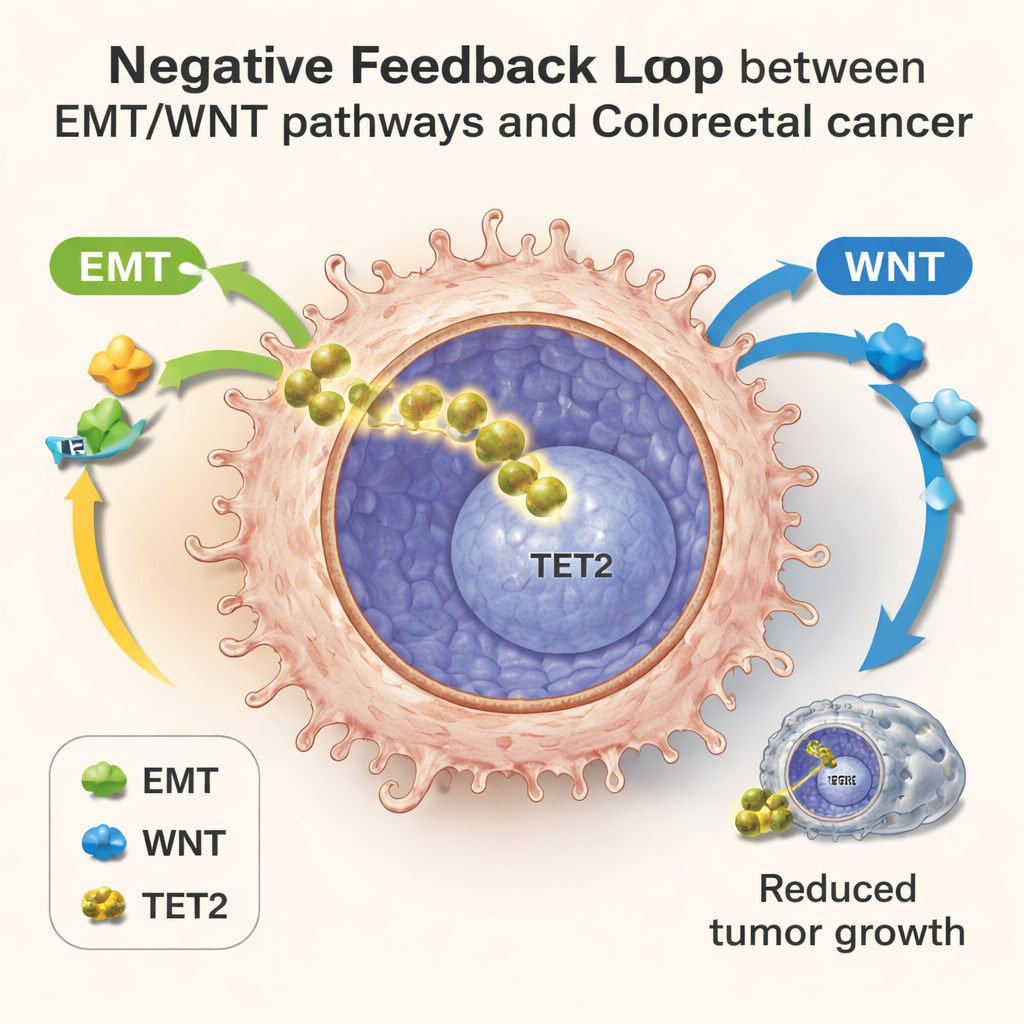
الخلايا المفردة تكشف حلقة تغذية مرتدة خفية
لفكّ تمزّق القوى هذا بتفصيل أكبر، استخدم الفريق تسلسل RNA على مستوى الخلية المفردة، الذي يقرأ أي الجينات نشطة في آلاف الخلايا الفردية في وقت واحد. في المستعمرات المزروعة مختبريًا، وفي أورام الفئران، وفي عينات من مرضى سرطان القولون والمستقيم، رأوا الخلايا منتشرة على طول خط زمني لتقدّم المرض. أظهرت الخلايا المبكرة استخدامًا طاقويًا طبيعيًا ونشاطًا ضعيفًا لـEMT/WNT؛ وأظهرت الخلايا المتأخرة إعادة برمجة أيضية، وإشارات قوية لـEMT/WNT، ثم ارتفاعًا في جينات أهداف TET2. في هذه المراحل المتأخرة، كانت الخلايا ذات نشاط أعلى لـTET2 تُظهر مستويات أقل من الجينات المرتبطة بالغزو وكانت مرتبطة بنتائج أفضل للمرضى، حتى بين الأورام التي بدأت بالفعل بالانتشار. يدعم هذا النمط فكرة حلقة تغذية راجعة سلبية: الإجهاد الأيضي وتنشيط EMT/WNT يدفعان TET2 إلى النواة، وTET2 النووي بدوره يقيّد تلك البرامج العدوانية نفسها.
ما الذي يعنيه هذا لعلاجات السرطان المستقبلية
بالنسبة لغير المتخصصين، تكمن الرسالة الأساسية في أن تقدّم سرطان القولون والمستقيم ليس مفتاح تشغيل/إيقاف بسيطًا بين سلوك جيد وسيئ. بل هناك آلية أمان مدمجة ومتأخرة: عندما تصبح الخلايا الورمية أكثر غزوًا، فإنها تنشّط أيضًا TET2 في نواتها، مما يحدّها جزئيًا. مع مرور الوقت، تفلت العديد من الأورام من هذه السيطرة عن طريق فقدان TET2 النووي أو التغلب على تأثيراته. من خلال إيجاد طرق لإبقاء TET2 في النواة أو تعزيز نشاطه — ربما بالجمع مع أدوية تعدّل EMT أو WNT — قد يتمكن الأطباء من تقوية هذه الفرملة الطبيعية وإبطاء انتشار السرطان. بدلًا من قصر الاستراتيجية على مهاجمة الخلايا من الخارج، قد تعمل العلاجات المستقبلية على استعادة وتضخيم نظام السيطرة الداخلي هذا.
الاستشهاد: Li, C., Meng, F., He, J. et al. Cytoplasm-nucleus shuttling of TET2: an intrinsic brake in colorectal cancer progression. Cell Death Dis 17, 163 (2026). https://doi.org/10.1038/s41419-026-08418-5
الكلمات المفتاحية: سرطان القولون والمستقيم, TET2, علم التخلق الوراثي (الإيبيجينيتيكس), الانتقال الظهاري‑اللحمي وإشارة WNT, تقدّم السرطان