Clear Sky Science · ar
الإبقاء الشاذ لعامل النسخ التطوري PAX6 يعزز موت الخلايا العصبية عبر إشارات JNK3
لماذا يهم هذا البحث البصر
الزرق هو سبب رئيسي للعمى الدائم، ويرجع ذلك إلى حد كبير إلى موت الخلايا العصبية التي تنقل المعلومات البصرية من العين إلى الدماغ بشكل بطيء. العديد من العلاجات تخفض ضغط العين، لكن قد يفقد الناس البصر حتى عندما يكون الضغط مضبوطًا جيدًا. يطرح هذا البحث سؤالاً أعمق: ما الذي يدفع خلايا الشبكية العصبية إلى اتخاذ قرار الموت عندما تتعرض للإجهاد، وهل يمكننا إيقاف ذلك القرار على مستوى ضبط الجينات داخل نواة الخلية؟
شبكية مرهقة تحت الهجوم
في صلب مرض الزرق والأمراض العينية ذات الصلة يكمن الفقدان البطيء لخلايا العقد الشبكية (RGCs)، وهي الخلايا العصبية المخرجة للعين. هذه الخلايا حساسة لأنواع متعددة من الإجهاد، بما في ذلك مستويات سامة من الناقل العصبي غلوتامات، التي تنشّط مستقبلات NMDA بشكل مفرط وتؤدي إلى حمولة مدمّرة من الكالسيوم. استخدم الباحثون نموذجًا فأريًا راسخًا حيث يُحقَن مقدار صغير من NMDA في العين، مما يسبب إصابة انتقائية لخلايا العقد الشبكية مع ترك طبقات شبكية أخرى إلى حد كبير سليمة. أكدوا أن هذا العلاج لم يغيّر ضغط العين، لكنه سبب علامات نمطية للموت الخلوي المبرمج في خلايا العقد الشبكية، مثل تحرير السيتوكروم ج من الميتوكوندريا وظهور أنوية موجبة في اختبار TUNEL.
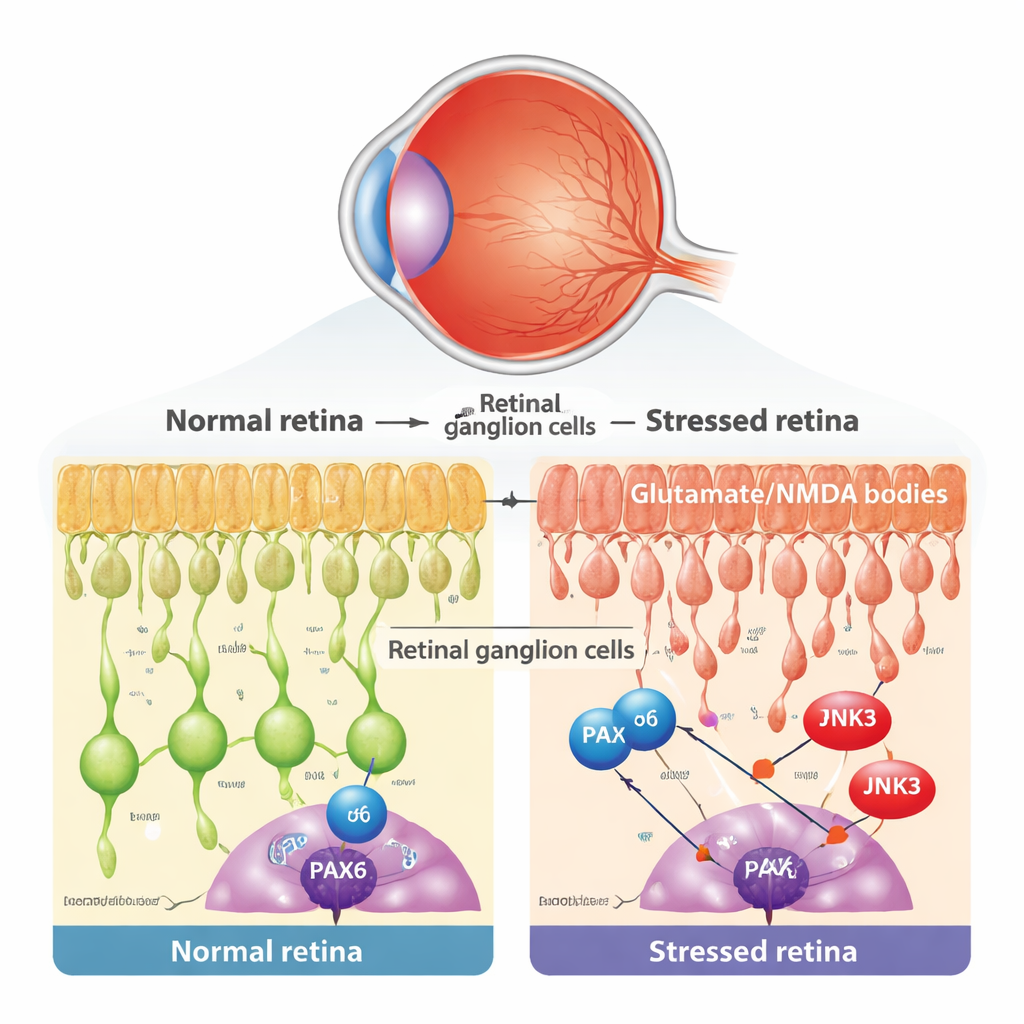
جين تطوري يرفض التقاعد
أثناء التطور المبكر، يعمل منظم الجينات المسمى PAX6 كمهندس رئيسي للعين، موجهًا كيفية تكون الخلايا الشبكية المختلفة وتوصيلها. تقول الحكمة التقليدية إن مثل هذه البرامج التطورية تُغلق إلى حد كبير في البالغين. بإعادة تحليل بيانات نسخ RNA أحادي الخلية من شبكيات كل من الفأر والإنسان، وجد الفريق أن PAX6 محفوظ بقوة وبانتقائية في خلايا العقد الشبكية الناضجة وبعض الخلايا الداخلية. باستخدام التصبغ المجهري، أظهروا أنه في الطبقة التي تقيم فيها خلايا العقد الشبكية، يكون PAX6 موجودًا إلى حد كبير في الخلايا العقدية أكثر منه في الخلايا الأمارينية المجاورة. أثار هذا احتمالًا مثيرًا: في مرض البالغين، قد تُستغل برامج تطورية قديمة وتتحول إلى محرك للانحلال.
من الحارس إلى الجلاد: PAX6 يغير الأدوار
لاختبار ما إذا كان PAX6 يساعد خلايا العقد الشبكية على البقاء أم الموت تحت الإجهاد، استخدم العلماء نهجًا شبيهًا بالعلاج الجيني. نقلوا ناقلًا فيروسيًا يحمل RNA صغيرًا يثبط PAX6 بشكل محدد في الشبكية، ثم عرضوا العيون لـ NMDA. بالمقارنة مع العيون المعالجة بالتحكم، أظهرت الشبكيات المحرومة من PAX6 عددًا أقل بكثير من خلايا العقد الشبكية المبرمجة للموت وتلفًا ميتوكوندريًا أقل بكثير، ما يشير إلى أن PAX6 مطلوب للموت الخلوي الكامل في هذا النموذج. كشفت تسلسلات RNA على مستوى الجينوم أن العديد من الجينات المؤيدة للموت، وخصوصًا تلك المشاركة في تلف الميتوكوندريا وتنشيط الكاسبازات، تم تحفيزها بشدة بواسطة NMDA في الفئران العادية لكن تقلص تحفيزها عندما تم إسكات PAX6. بعبارة أخرى، يساعد PAX6 في تشغيل شبكة من الجينات التي تدفع خلايا العقد الشبكية إلى الحافة.
كيناز الإجهاد الذي يقلب مفتاح PAX6
كيف يُفعّل الإجهاد PAX6 دون زيادة كميته؟ ركز الفريق على JNK3، وهو إنزيم مستجيب للإجهاد يوجد أساسًا في الخلايا العصبية. تحت إصابة NMDA، انتقل JNK3 إلى نواة خلايا العقد الشبكية وارتبط ماديًا بـ PAX6. أظهرت تجارب بيوكيميائية «في أنبوب الاختبار» باستخدام بروتينات مُنَقَّية أن JNK3 قادر مباشرة على إضافة شارات الفوسفات إلى PAX6، وكانت هذه التفاعلات محجوبة بمثبط JNK. في الفئران التي تفتقر إلى جين Jnk3، لم يعد NMDA ينتج نفس نمط فسفرة PAX6. كشفت خرائط الكروماتين (ChIP-seq) وتجارب ربط الحمض النووي المستهدفة أن PAX6 المفسفر، مع JNK3، يصبح تحت الإجهاد أكثر ارتباطًا بمناطق التحكم في جينات رئيسية مؤيدة للموت مثل Bax وGadd45a، مما يعزز نشاطها. عندما تم إسكات PAX6 أو حذف JNK3 وراثيًا، تقلص هذا الارتباط وتنشيط الجينات المؤيدة للموت بشكل حاد.
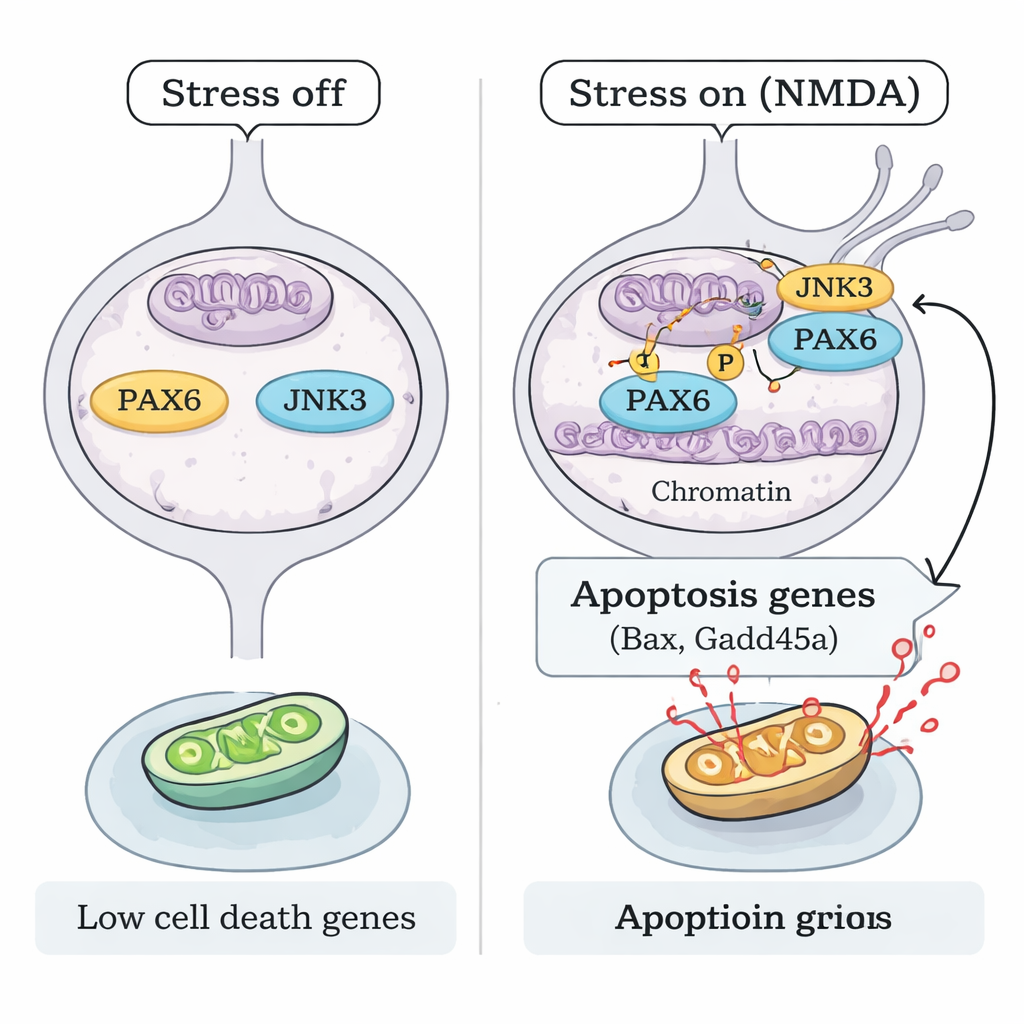
إيقاف برنامج الموت لحماية البصر
أخيرًا، تساءل الباحثون عما إذا كان حظر محور JNK3–PAX6 كافيًا لحماية الخلايا الحرجة للرؤية. في كل من فئران إسكات PAX6 والفئران الناقصة لـ JNK3، تم الحفاظ على خلايا العقد الشبكية بشكل كبير بعد التعرض لـ NMDA، مع عدد أقل من الخلايا الميتة وبنية شبكية أكثر صحة. يشير هذا إلى نموذج آلي واضح: تحت الإجهاد الناجم عن التحفيز المفرط، يقوم JNK3 بفوسفرة PAX6 المعبر عنه باستمرار، محولًا إياه من باني تطوري إلى منشط قوي لبرنامج جيني للموت في خلايا العقد الشبكية البالغة. إن مقاطعة ذلك الرابط — عن طريق إسكات PAX6 أو تعطيل JNK3 — تبقي العديد من هذه الخلايا العصبية على قيد الحياة. للمرضى، يقترح هذا العمل أن علاجات الزرق المستقبلية قد تتجاوز خفض ضغط العين وتستهدف مباشرة مفاتيح الجينات التي تقرر ما إذا كانت خلايا الشبكية العصبية تعيش أم تموت.
الاستشهاد: Kim, JY., An, MJ., Kim, J. et al. Aberrant maintenance of developmental transcription factor PAX6 promotes neuronal cell death via JNK3 signaling. Cell Death Dis 17, 161 (2026). https://doi.org/10.1038/s41419-026-08417-6
الكلمات المفتاحية: الزرق, خلايا العقد الشبكية, PAX6, JNK3, الانحلال العصبي