Clear Sky Science · ar
استهداف ENO1 يعيد برمجة استقطاب البلاعم لتحفيز المناعة المضادة للأورام ويحسّن التأثير العلاجي للعلاج الإشعاعي
تحويل دروع الورم إلى أهداف
لا ينجو السرطان غالبًا بمجرد النمو السريع فحسب، بل من خلال تعطيل دفاعات الجسم بهدوء. تستكشف هذه الدراسة جزيئًا خفيًا على خلايا السرطان، يُدعى ENO1، يساعد الأورام على التهرب من الجهاز المناعي والمقاومة للعلاج الإشعاعي. من خلال تطوير جسم مضاد جديد يستهدف ENO1، يُظهر الباحثون إمكانية تجفيف الأورام من المواد الكيميائية الواقية، وإيقاظ خلايا المناعة، وتحسين فعالية الإشعاع في نماذج سرطان القولون والثدي الثلاثي السلبي. 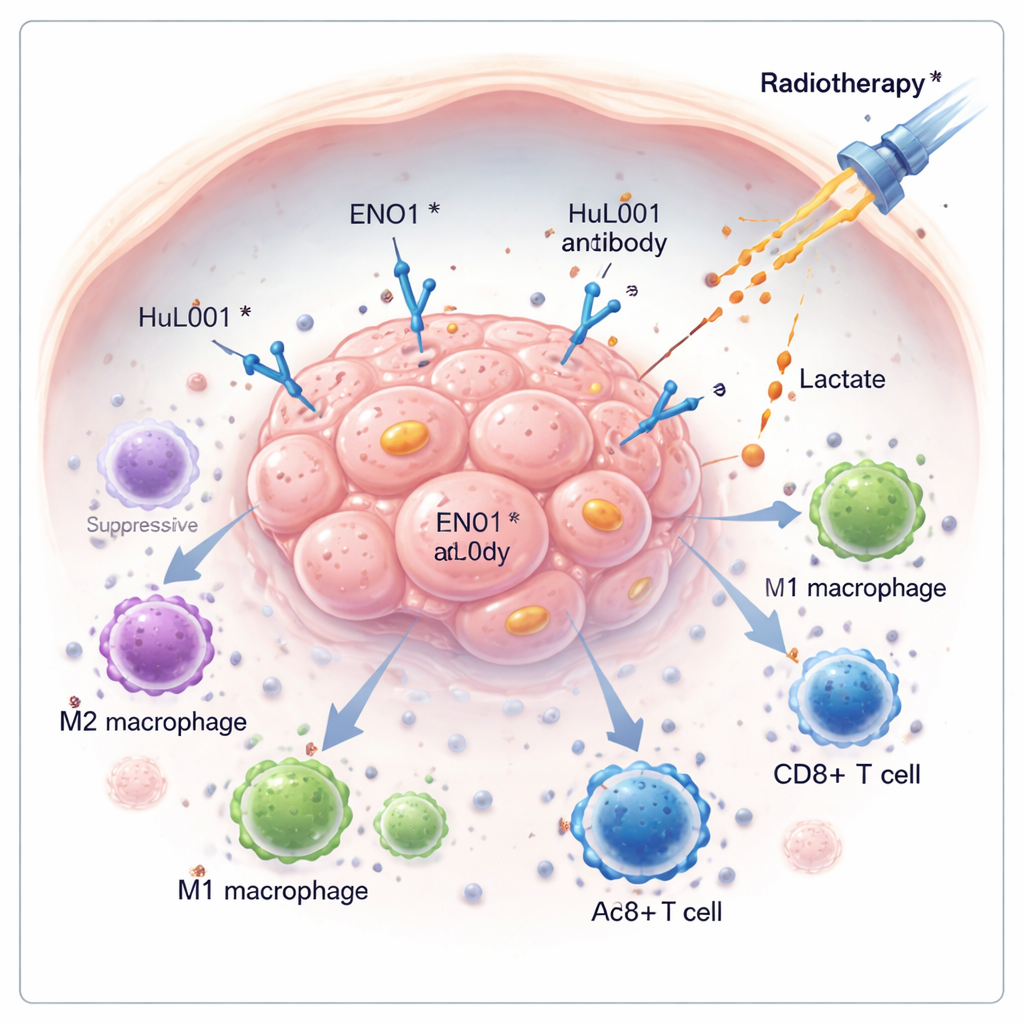
حيلة أيضية تكتم المناعة
تعيد العديد من الأورام برمجة كيفية استخدام الطاقة، فتكسر السكر بطريقة تولد كميات كبيرة من حمض اللاكتيك حتى عند توفر الأكسجين. يُضخ حمض اللاكتيك هذا خارج خلايا السرطان ويتراكم حول الورم، محولًا المنطقة المحيطة إلى بيئة حمضية قاسية تُضعف الهجوم المناعي. في هذا العمل، يركز المؤلفون على ENO1، وهو إنزيم مشارك في تحلل السكر يمكن أن يظهر أيضًا على سطح خلايا السرطان. عند تواجده على السطح الخلوي، يتعاون ENO1 مع بروتين آخر، ناقل يُدعى MCT4، لمساعدة تصدير اللاكتيت—مما يغذي بيئة تُفضّل نمو الورم وتقمع خلايا المناعة.
كيف يمكن أن ينقلب الدور على العلاج الإشعاعي
صُمم العلاج الإشعاعي لإتلاف حمض نووي الورم وتحفيز استجابات مناعية، لكنه يملك أيضًا تأثيرات جانبية داخل بيئة الورم الميكروية. اكتشف الفريق أن إشارات يقودها جزيء يُسمى TGFβ1، والتي تتعزز بواسطة الإشعاع، تُنَشِّط إنزيمًا (PRMT5) يُعدّل ENO1 كيميائيًا وينقله إلى سطح خلية السرطان. بمجرد تواجده هناك، يتفاعل ENO1 ماديًا مع MCT4 ليُثبّتَه ويعزز تصدير اللاكتيت. وُجدت مستويات أعلى من ENO1 السطحي لدى مرضى بسرطانات القولون والثدي الثلاثي السلبي المتقدمة وكانت مرتبطة بمزيد من النقائل وبانخفاض البقاء، ما يشير إلى أن الإشعاع قد يعزز دون قصد درعًا قمعيًا مناعيًّا مدفوعًا باللاكتيت حول الأورام.
إعادة برمجة خلايا المناعة الصديقة والعدوة
في الهالة الحمضية حول الأورام، تُدفع خلايا المناعة المسماة البلاعم إلى حالة "مُصَلِّحة" (غالبًا ما تُسمى M2) التي تساعد الأورام فعليًا عن طريق كبح الالتهاب والمساهمة في الإصلاح، بدلاً من قتل الخلايا السرطانية. ابتكر الباحثون جسمًا مضادًا مُؤنَّسًا باسم HuL001 يتعرّف على ENO1 على خلايا السرطان البشرية والفأرية على حدّ سواء. في زراعة الخلايا ونماذج الفأر، عطل HuL001 دعم ENO1 لـ MCT4، وخفّض إطلاق اللاكتيت، وحوّل البلاعم بعيدًا عن حالة M2 المحفزة للورم نحو حالة M1، التي تكون أكثر عدائية ضد السرطان وأفضل في بلع الخلايا الورمية. من المهم أن HuL001 لم يقم ببساطة بقتل البلاعم؛ بل أعاد تعليمها مع زيادة مباشرة في موت الخلايا السرطانية.
جعل الإشعاع أكثر فاعلية
عندما جُمِع HuL001 مع العلاج الإشعاعي في نماذج الفأر لسرطان القولون والثدي الثلاثي السلبي، تقلصت الأورام أكثر، ونمت ببطء أكبر بعد العلاج، وفي العديد من الحيوانات اختفت تمامًا. 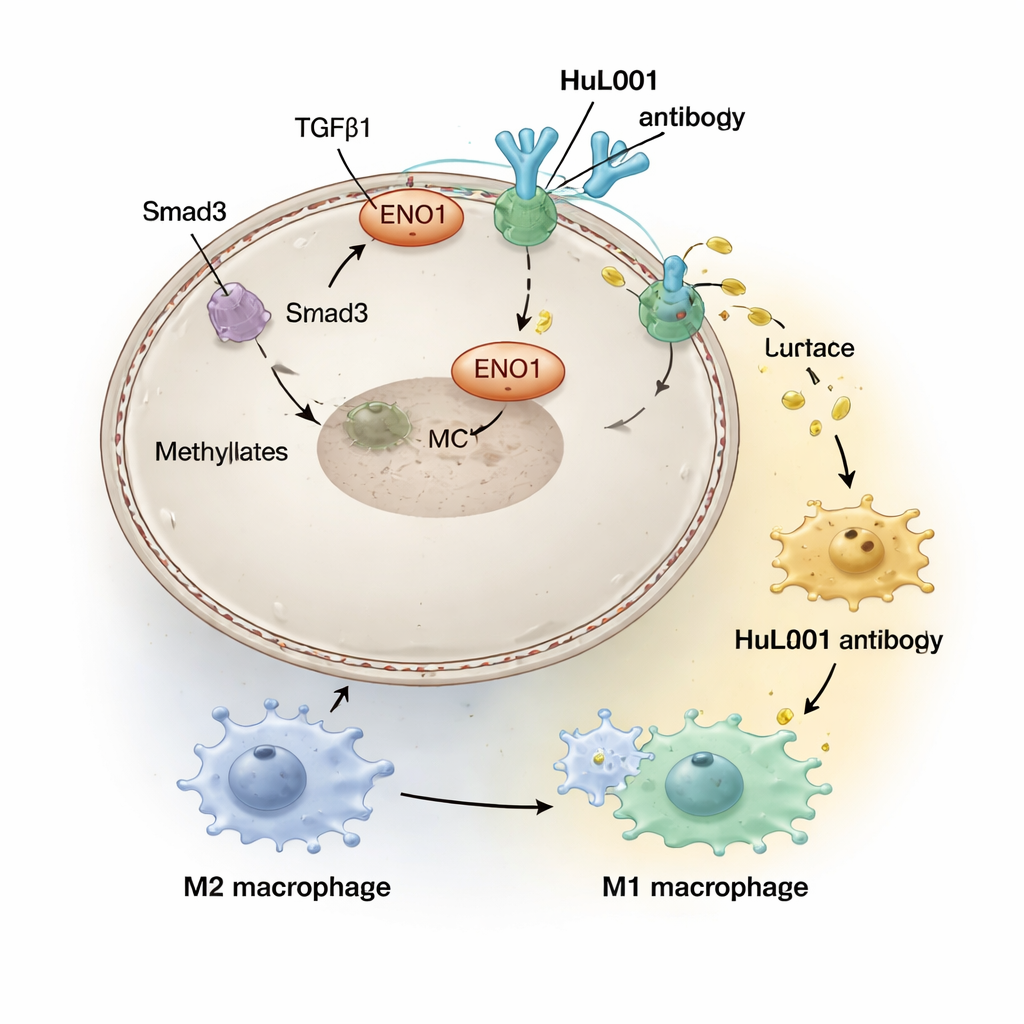
من مسارات معقدة إلى وعد عملي
لغير المتخصصين، رسالة هذه الدراسة أن كيمياء الورم وجيرانه من خلايا المناعة مرتبطان ارتباطًا عميقًا. يقف ENO1 عند مفترق طرق: يساعد الأورام على حرق السكر، وتصدير حمض اللاكتيك، واستدعاء نوع خاطئ من المساعدة المناعية. من خلال حجب ENO1 السطحي بجسم مضاد موجه، تمكن الباحثون من تقليل تراكم اللاكتيت الضار، وقلب البلاعم من مساعدين للورم إلى مقاتلين ضده، وجعل الإشعاع أكثر فعالية في نماذج لأورام يصعب علاجها. وعلى الرغم من أن HuL001 ليس دواءً سريريًا بعد، فإن العمل يشير إلى أن استهداف بوابات الأيض مثل ENO1 قد يصبح وسيلة قوية لتحويل دفاعات الورم ضده وتعزيز العلاجات الحالية مثل العلاج الإشعاعي.
الاستشهاد: Lin, YS., Chang, HY., Hong, WZ. et al. Targeting ENO1 reprograms macrophage polarization to trigger antitumor immunity and improves the therapeutic effect of radiotherapy. Cell Death Dis 17, 194 (2026). https://doi.org/10.1038/s41419-026-08416-7
الكلمات المفتاحية: أيض الورم, استقطاب البلاعم, العلاج الإشعاعي, العلاج المناعي, اللاكتيت