Clear Sky Science · ar
Sec8: منظم إيجابي جديد لـ RIG-I في الدفاع المضاد للفيروسات الريبية
كيف تكتشف خلايانا الفيروسات الماكرة
تحمل العديد من الفيروسات الخطرة، بما في ذلك الإنفلونزا والفيروسات الحيوانية الناشئة، مادتها الوراثية على شكل RNA. تعتمد خلايانا على أنظمة إنذار داخلية لملاحظة هذه الغزاة بسرعة وإطلاق استجابة مضادة للفيروسات. تستكشف هذه الورقة بروتينًا خلوياً قليلاً ما يُعرف باسم Sec8 وتبين أنه يلعب دورًا محوريًا بخفاء في إبقاء أحد مجساتنا الفيروسية الرئيسية، RIG‑I، حيا ونشطًا لفترة تكفي لحمايتنا.
جهاز إنذار خلوي مهدد
يعمل RIG‑I كـ"جهاز إنذار لصوص" جزيئي يجوب داخل الخلايا بحثًا عن قطع من RNA الفيروسي. عندما يكتشف RNA مريبًا، يغير شكله وينشط ويرسل إشارات تؤدي في النهاية إلى إنتاج الإنترفيرونات من النوع الأول — جزيئات تحذير قوية تساعد الخلايا المجاورة على مقاومة العدوى وتنشط الدفاعات المناعية. وبما أن نشاط الإنذار المفرط قد يسبب التهابًا ضارًا أو أمراضًا مناعية ذاتية، تتحكم الخلايا بإحكام في مستويات RIG‑I. يمكن لعدة بروتينات أن تضع علامات على RIG‑I للدمار عن طريق إرفاق سلاسل يوبيكويتين قصيرة، مما يوجهه إلى "المفرمة" الخلوية المسماة البروتيازوم. وحتى الآن، لم يكن واضحًا ما هي العوامل الخلوية الإضافية التي تحمي RIG‑I من التدمير المبكر، خصوصًا أثناء العدوى النشطة بفيروسات RNA.
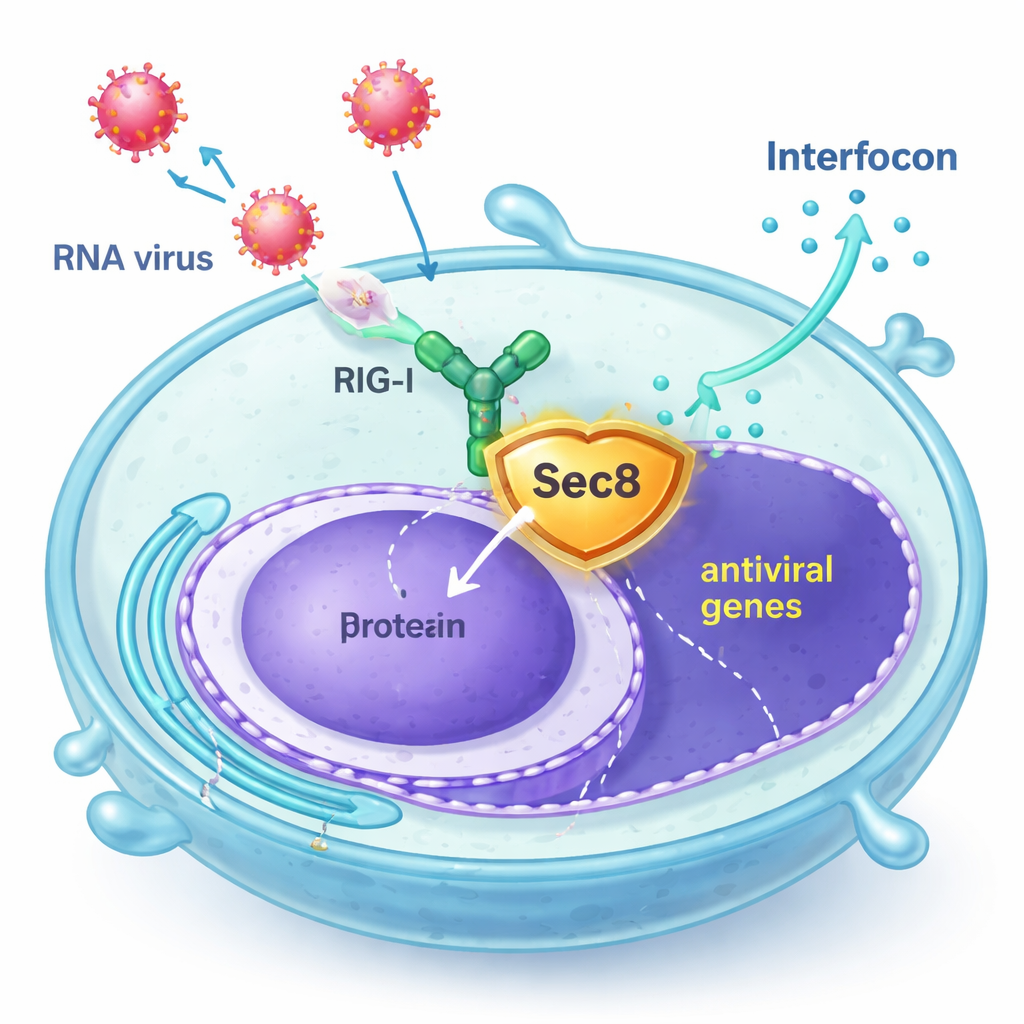
Sec8 يتدخل كحارس شخصي
اكتشف المؤلفون أن Sec8، المعروف أساسًا كجزء من مركب مكون من ثمانية بروتينات يساعد الحويصلات الإفرازية على الاندماج مع سطح الخلية، يعزز فعليًا الإشارة المضادة للفيروسات. في خطوط خلايا بشرية وفي خلايا مناعية أولية من الفئران، أدت زيادة مستويات Sec8 إلى تنشيط أقوى للجينات المرتبطة بالإنترفيرون بعد العدوى بفيروسات RNA مثل فيروس التهاب الفم الحويصلي (VSV) وفيروس سينداي، أو بعد التعرض لـ RNA فيروسي صناعي. وعلى النقيض من ذلك، أدى خفض Sec8 إلى تقليل إنتاج الإنترفيرون والجينات المحفزة بالإنترفيرون، ما جعل الخلايا أقل قدرة على مقاومة تكاثر الفيروس. وتشير هذه النتائج إلى أن Sec8 لا يشارك في الإفراز فحسب، بل يعمل كمنظم إيجابي داخل مسار إنذار المضاد للفيروسات.
إيقاف المفرمة الخلوية
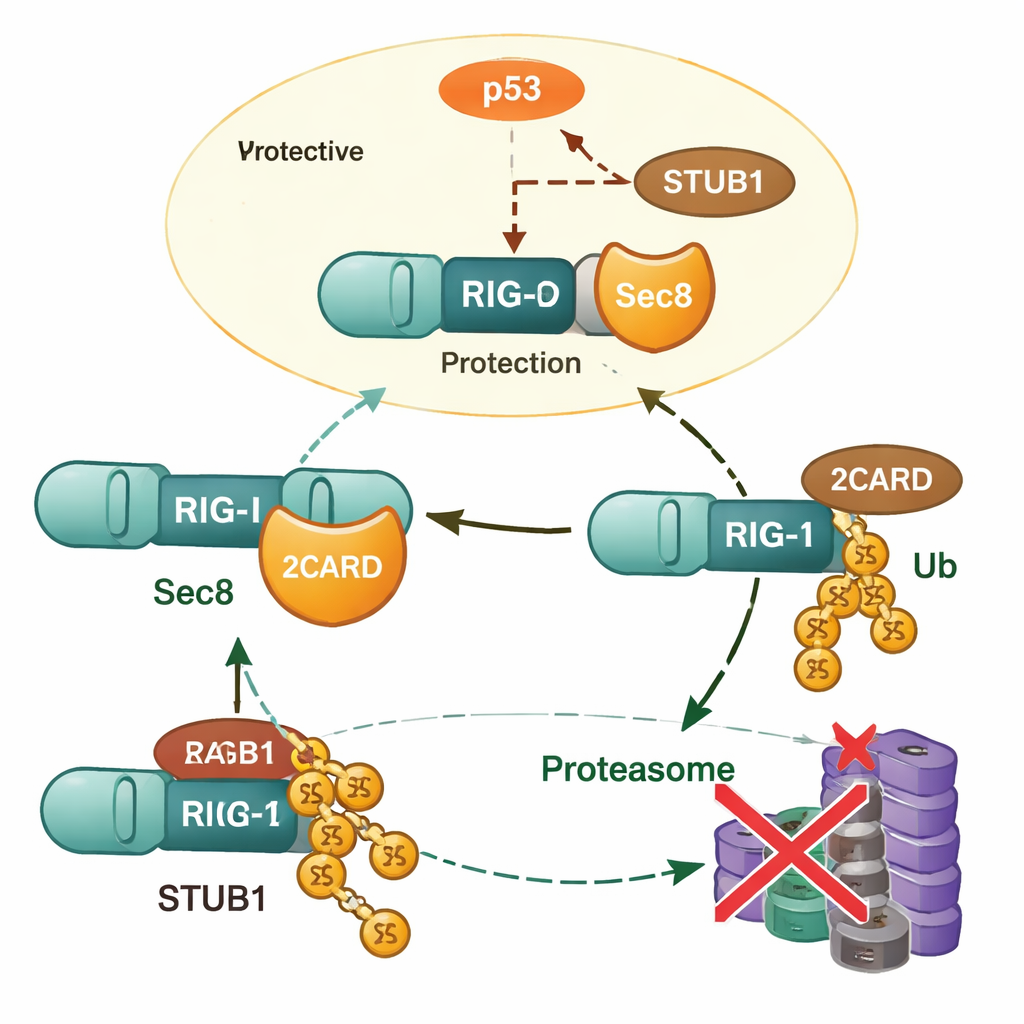
بالغوص أعمق، وجد الباحثون أن Sec8 لا يزيد من تعبير جين RIG‑I؛ بل يمنع تدهور بروتين RIG‑I. عندما أُزيل Sec8، انخفضت مستويات RIG‑I بسرعة أكبر، ويمكن منع هذا الفقدان بعقاقير تعطل البروتيازوم، مما يورط آلية إعادة تدوير البروتينات الخلوية. وحد الفريق بروتينًا آخر، STUB1، كباحث مفتاحي يضع علامة محددة من نوع سلسلة يوبيكويتين مرتبطة بـ K48 على RIG‑I في الحمض الأميني الليزين 190. تضع هذه العلامة RIG‑I على قائمة التدمير. يتداخل Sec8 مع هذه العملية بطريقتين: يتنافس جسديًا مع STUB1 على الارتباط بنفس منطقة تفعيل RIG‑I، ويقلل أيضًا من كمية STUB1 التي تصنعها الخلية في المقام الأول.
Sec8 و p53 والتحكم في الموسِّم بالعلامات
لتفسير كيف يقلل Sec8 إنتاج STUB1، توجه المؤلفون إلى تنظيم الجينات. حددوا امتدادًا قصيرًا من الحمض النووي يعمل كمفتاح تشغيل (مروج) أساسي لجين STUB1 وأظهروا أن بروتين كبح الأورام الشهير p53 يرتبط بهذه المنطقة ويرفع مستويات STUB1. يخمد Sec8 كلاً من كمية p53 وفوسفاتيزاته المنشطة، بحيث لا يستطيع p53 بعد ذلك تحفيز إنتاج STUB1 بفعالية. عندما أُوقف نشاط p53 أو سكّت STUB1، انقلبت الآثار الضارة لفقدان Sec8 على إنتاج الإنترفيرون ونمو الفيروس إلى حد كبير. هذا يضع Sec8 في قمة سلسلة تنظيمية تمتد من p53 إلى STUB1 وأخيرًا إلى استقرار RIG‑I.
من طبق بتري إلى حيوانات حية
اختبر الفريق بعد ذلك أهمية Sec8 في فئران مهندسة لتفتقر إلى جين Sec8 تحديدًا في خلايا مناعية معينة. بعد العدوى بـ VSV، أنتجت هذه الحيوانات إنترفيرونًا أقل، وحملت أعدادًا أكبر من الفيروس في أعضاء مثل الطحال والكبد والرئتين، وأظهرت تلفًا رئويًا أسوأ وفقدان وزن أكبر وبقاء أقل مقارنة بالفئران الضابطة. تؤكد هذه النتائج الحية أن Sec8 ليس لاعبًا ثانويًا بل حاميًا مهمًا ضد عدوى الفيروسات ذات الحمض النووي الريبي في كائن حي كامل.
لماذا هذا مهم للعلاجات المستقبلية
بعبارة بسيطة، تُظهر هذه الدراسة أن Sec8 يعمل كحارس شخصي للمستشعر المضاد للفيروسات RIG‑I. من خلال إبقاء بروتين الموسِّم STUB1 تحت السيطرة وحماية RIG‑I مباشرة من الإرسال إلى المفرمة الخلوية، يسمح Sec8 للخلايا بإطلاق استجابة إنترفيرونية مناسبة الزمان والتحكم بشكل أفضل في الفيروسات الريبية. إن فهم هذا المحور الجديد p53–STUB1–RIG‑I يفتح الباب لاستراتيجيات مضادة للفيروسات في المستقبل تهدف إلى تثبيت RIG‑I أو تقليد أفعال Sec8 الوقائية، مما قد يعزز دفاعاتنا ضد مجموعة واسعة من العدوات الفيروسية القائمة على RNA.
الاستشهاد: Wang, L., Ma, W., Hou, P. et al. Sec8: a novel positive regulator of RIG-I in anti-RNA viral defense. Cell Death Dis 17, 165 (2026). https://doi.org/10.1038/s41419-026-08414-9
الكلمات المفتاحية: المناعة الفطرية, الڤيروسات الريبية, RIG-I, اليوبيكويتين, إشارة الإنترفيرون