Clear Sky Science · ar
ما وراء الأيض: استكشاف الآثار التنظيمية والعلاجية لللاكتيت واللاكتليشن في موت الخلايا المرتبط بالسرطان
لماذا يهم «ناتج نفاية» من السكّر في السرطان
لعقود، وَصِف اللاكتات — المادة التي تسبب احتراق العضلات المتعبة — بأنها نفاية خلوية. تُظهر هذه المراجعة أن اللاكتات في السرطان أبعد ما تكون عن كونها نفاية. فهي تعمل كوقود، وكإشارة كيميائية، وحتى كمفتاح يمكنه أن يقرر ما إذا كانت الخلايا الورمية ستبقى على قيد الحياة أو تموت. فهم هذا الدور المخفي قد يفتح سبلًا جديدة لجعل الخلايا السرطانية تُدمّر ذاتيًا مع الحفاظ على الأنْسجة السليمة.
الطريق المختصر للسكر الذي يعيد برمجة الخلايا السرطانية
الخلايا السرطانية معروفة بـ«شهوتها للسكر». حتى عندما يتوفر الأكسجين بكثرة، تفضّل هذه الخلايا تكسير الجلوكوز بسرعة إلى لاكتات بدلًا من حرقه بالكامل في الميتوكوندريا، وهو تحول يُعرف بتأثير واربورغ. تتيح هذه الاستراتيجية للأورام توليد الطاقة ومكونات البناء بسرعة عالية. ويُضخ سيل اللاكتات الناتج عبر ناقلات خاصة، مشكِّلاً وسطًا حمضيًا وغنيًا بالمغذيات في الميكروبيئة الورمية يدعم النمو ويساعد الأورام على التكيّف مع الضغوط، مثل نقص الأكسجين أو العلاج الكيميائي.
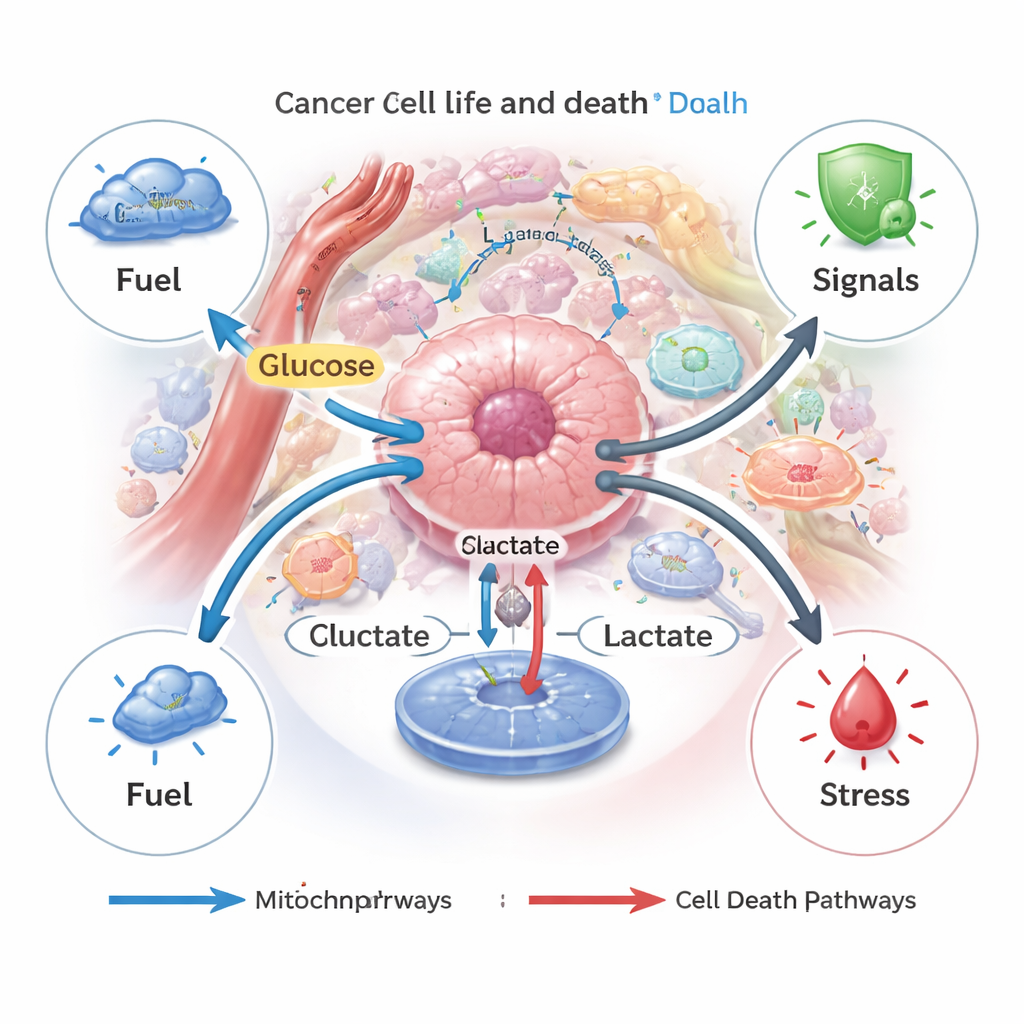
اللاكتات كمقوِّم لأنواع مختلفة من موت الخلايا
الموت الخلوي في أجسامنا عادةً ما يكون مُنظَّمًا بدقة، مما يساعد على إزالة الخلايا التالفة أو الخطرة. غالبًا ما تهرب الخلايا السرطانية من هذه البرامج. يصف المؤلفون كيف أن اللاكتات يمكن أن يعيق أو يحفّز عدة مسارات موت منظم — مثل الاستماتة (انتحار الخلية)، والبلعمة الذاتية (الهضم الذاتي)، والفروبتوزيس (تلف غشائي مدفوع بالحديد)، والبايروبتوزيس (الانفجار الالتهابي)، والكوبروبتوزيس (الانهيار المدفوع بالنحاس). عندما تولّد الخلايا السرطانية أو تستورد كميات معتدلة من اللاكتات، فإنها تميل إلى استخدامها كوقود وإشارة بقاء، مُفَعِّلة مسارات تحميها من العلاج الكيميائي أو نقص المغذيات أو الأدوية الموجهة. لكن عندما يتراكم اللاكتات داخل الخلايا — على سبيل المثال إذا تعطل تصديره — يمكن أن يؤدي الإجهاد الحمضي وإصابة الميتوكوندريا الناتجة إلى قلب الموازين ودفع الخلايا نحو الاستماتة أو الفروبتوزيس.
اللاكتليشن: عندما يكتب اللاكتات على البروتينات
اكتشاف لافت في الآونة الأخيرة هو أن اللاكتات يمكن تحويله إلى علامة كيميائية صغيرة تُرفَق ببقايا الليزين على البروتينات، تعديل يعرف باللاكتليشن. تعمل إنزيمات كـ"كاتبين" و"ممحّيات" لهذه العلامات، مُزيِّنة كلًّا من الهيستونات المرتبطة بالحمض النووي والعديد من البروتينات الأخرى. تُغير هذه العلامات الجينات المشغّلة، وسلوك الإنزيمات، واستقرار المنظّمين الرئيسيين. في السرطان، تضبط اللاكتليشن بدقة التوازن بين البقاء والتدمير الذاتي. يمكن أن تزيد، على سبيل المثال، من البروتينات التي تعوق الاستماتة، وتعزّز إعادة التدوير عبر البلعمة الذاتية، وتحمي الخلايا من الفروبتوزيس عن طريق تشديد ضبط الحديد وتعزيز مضادات الأكسدة، أو تغيّر أشكال موت جديدة مثل الكوبروبتوزيس بتعديل كيفية تعامل الخلايا مع البروتينات الحسّاسة للنحاس.
حوار ثنائي الاتجاه بين الأيض وبرامج الموت
العلاقة ليست أحادية الجانب: مسارات موت الخلايا تُعيد أيضًا تشكيل كيفية استخدام الأورام للسكر وإنتاج اللاكتات. عندما تتضرر الميتوكوندريا خلال المراحل المبكرة من الاستماتة أو الميتوفاجي (الإزالة الانتقائية للميتوكندريا)، غالبًا ما تعود الخلايا إلى التحلل السكري السريع، ما يزيد من إنتاج اللاكتات. قد تخضع الخلايا الداعمة المحيطة، مثل الخلايا الليفية المرتبطة بالسرطان، لإعادة برمجة مشابهة وتصبح مصانع للاكتات تغذي الخلايا الورمية القريبة. أنواع أخرى من الموت، مثل الفروبتوزيس، تميل إلى قمع التحلل السكري ومن ثم خفض مستويات اللاكتات. النتيجة هي حلقة تغذية راجعة ديناميكية يتكيف فيها الأيض وآليات الموت مع بعضهما البعض باستمرار مع تطور الورم واستجابته للعلاج.
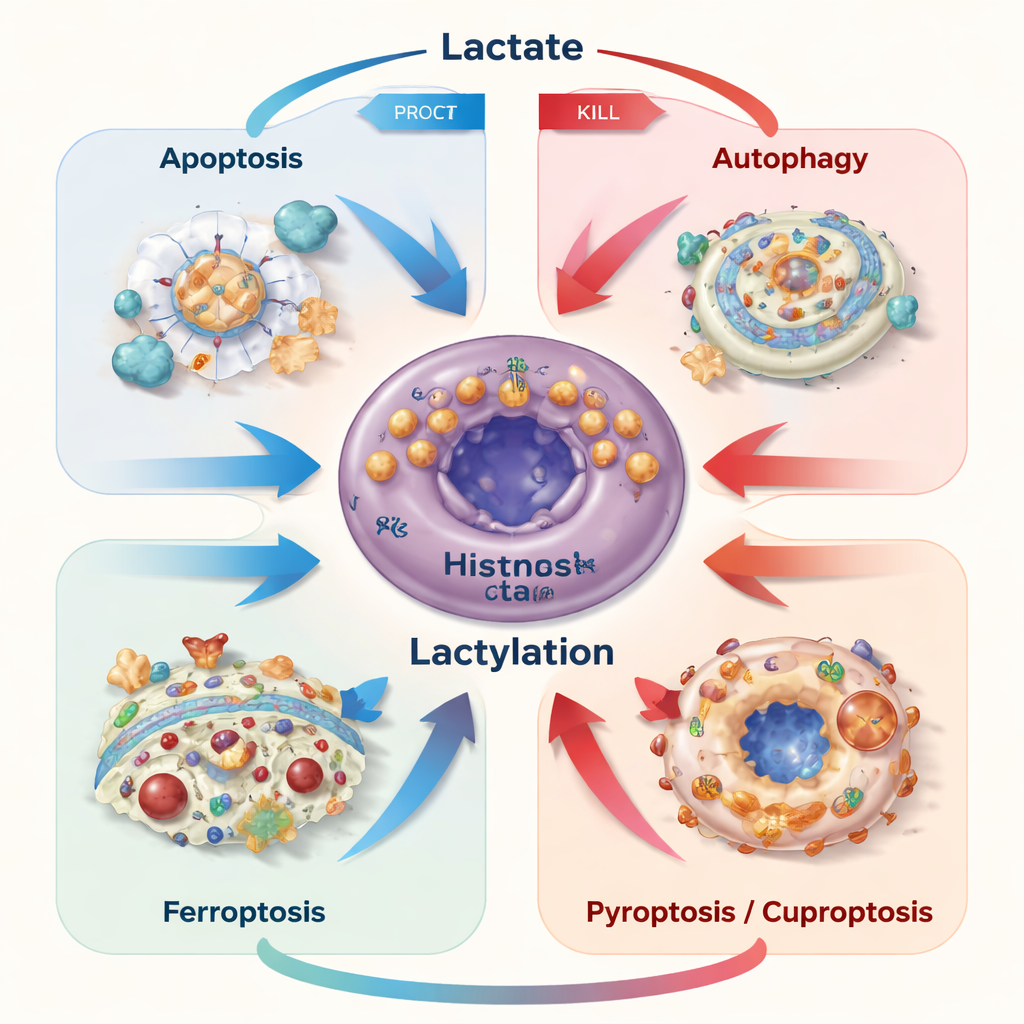
تحويل نقطة ضعف إلى استراتيجية علاجية
بما أن اللاكتات واللاكتليشن يمكن أن يحميَا أو يقتلا الخلايا السرطانية اعتمادًا على السياق، يجادل المؤلفون بأن العلاجات يجب أن تفعل أكثر من مجرد حظر إنتاج اللاكتات. بدلاً من ذلك، قد تعيد العلاجات المستقبلية توجيه تدفقات اللاكتات انتقائيًا، أو تعدّل ناقلاته، أو تستهدف علامات لاكتليشن محددة لكي تُدلي الخلايا السرطانية بدلوها في الانقراض بينما تُعيد تنشيط الخلايا المناعية المضادة للورم التي شُلّت حاليًا بسبب الوسط الحمضي. تظهر أنظمة توصيل الدواء الذكية والنانو‑أدوية التي تستجيب لمستويات اللاكتات أو الحموضة المحلية كوسائل لتطبيق هذه الدقة. ببساطة، رسالة المقال أن ما بدا سابقًا نفاية أيضية هو في الواقع مقوّم تحكّم قوي في مصير الخلايا السرطانية — وتعلّم كيفية تدوير هذا المقوّم بطريقة صحيحة قد يجعل العلاجات الحالية أكثر فعالية بكثير.
الاستشهاد: Chen, C., Lin, A., Zhao, J. et al. Beyond metabolism: exploring the regulatory and therapeutic implications of lactate and lactylation in cancer-regulated cell death. Cell Death Dis 17, 184 (2026). https://doi.org/10.1038/s41419-026-08410-z
الكلمات المفتاحية: اللاكتات, اللاكتليشن, موت الخلية السرطانية, استقلاب الورم, الفروبتوزيس