Clear Sky Science · ar
سياق المناعة الورمية وتجنب المناعة في سرطانات القولون والمستقيم ذات عدم استقرار الميكروساتيلّايت العَرَضيّة والمرتبطة بمتلازمة لينش
لماذا هذا مهم لمرضى السرطان
غيّر العلاج المناعي توقعات الشفاء لكثير من مرضى سرطان القولون والمستقيم، لكن ليس الجميع يستفيد. تطرح هذه الدراسة سؤالاً محوريًا: لماذا تتمكن بعض الأورام التي من الناحية النظرية يجب أن تكون مرئية جيدًا للجهاز المناعي من الإفلات منه؟ من خلال مقارنة نوعين من سرطانات القولون ذات عدم الاستقرار الجيني — المرتبطة بمتلازمة لينش الموروثة وتلك التي تظهر بشكل عَرَضي — يكشف الباحثون اختلافات مهمة في كيفية محاصرة الخلايا المناعية للأورام أو مهاجمتها أو أحيانًا حمايتها.
طريقتان وصول إلى نفس نوع الورم
تحمل سرطانات القولون والمستقيم غير المستقرة في الميكروساتيلّايت (MSI) أعدادًا كبيرة من أخطاء الحمض النووي، ما يؤدي إلى تكوين بروتينات شاذة قد تعمل كـ"أعلام" للجهاز المناعي. قد تنشأ هذه الأورام إما بسبب عيوب موروثة في إصلاح الحمض النووي (متلازمة لينش) أو بسبب تغييرات تحدث في الورم نفسه فقط (سرطانات MSI العَرَضية). على الرغم من أن كلا النوعين يبدوان متشابهين تحت المجهر، فإن البيئة المناعية المحيطة بهما — وربما استجابتهما للعلاج — ليست متماثلة. جمع الفريق 43 حالة من سرطانات القولون والمستقيم ذات MSI من مرضى فنلنديين، شملت حالات مرتبطة بلينش وحالات عَرَضية، وحلّلوها باستخدام تلوين الأنسجة والتسلسل الجينومي الكامل وتسلسل الحمض النووي الريبي لرسم خريطة مفصّلة للخلايا المناعية الحاضرة وكيفية تهرّب الأورام من التدمير.
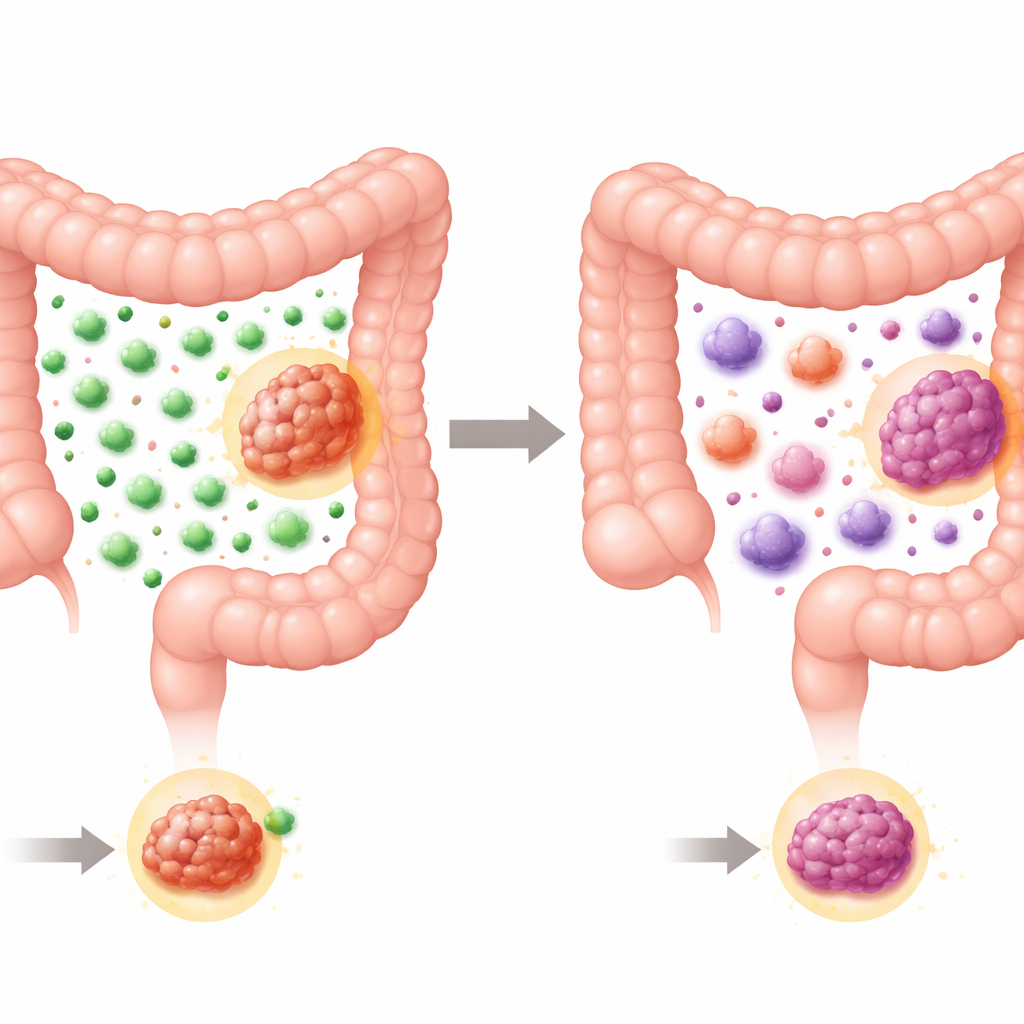
كمية الخلايا المناعية الحاضرة
ركز الباحثون أولًا على الخلايا التائية، القتلة المستهدفة في الجهاز المناعي. قاسوا مقياسًا مناعيًا معتمدًا يجمع كثافة الخلايا التائية الإجمالية والخلايا القاتلة في مركز الورم وحافته الغازية. كما كان متوقعًا، أظهرت أورام MSI عمومًا درجات أعلى من الأورام القولونية المعتادة، ما يعكس قدرتها الأكبر على جذب الخلايا التائية. لكن عند الفحص داخل مجموعة MSI، ظهرت نمطية واضحة: كل ورم مرتبط بمتلازمة لينش كان ذو درجة مناعية عالية، بينما انقسمت أورام MSI العَرَضية تقريبًا إلى نصفين بين درجات عالية ومنخفضة. بعبارة أخرى، تميل أورام MSI الموروثة إلى استدعاء جيوش قوية من الخلايا التائية، بينما تظهر الأورام العَرَضية تباينًا أكبر، وبعضها يبدو «باردًا» بالمقارنة بالنسبة للجهاز المناعي.
الخلايا المساندة الصديقة وغير الصديقة
انتقلت الدراسة بعد ذلك إلى الخلايا النُخاعية — خلايا المناعة الفطرية مثل البلعميات متعدة الأشكال والعدلات التي يمكن أن تساعد الخلايا التائية في محاربة السرطان أو، على نحو متناقض، تحمي الأورام. باستخدام تلوين تعددي يحدد عدة بروتينات في آن واحد، صنّف المؤلفون البلعميات إلى نوعين عامين: خلايا شبيهة بـM1، تدعم الالتهاب وقتل الورم، وخلايا شبيهة بـM2، تميل إلى تهدئة الأنسجة، وإصلاح الجروح، وغالبًا تعزيز الأورام. احتوت كل من أورام MSI المرتبطة بلينش والعَرَضية على عدد كبير من الخلايا النخاعية، لكن الأورام العَرَضية تميّزت بوجود المزيد من البلعميات الشبيهة بـM2، لا سيما في النسيج الداعم عند الحافة الغازية للورم. في تلك المنطقة، فاقت خلايا M2-like حتى عدد خلايا M1-like في الأورام العَرَضية. ضمن مجموعة الأورام العَرَضية، كانت تلك التي لديها درجات عالية من الخلايا التائية تحتوي أيضًا على المزيد من البلعميات الشبيهة بـM1، بينما بقيت مستويات M2-like مرتفعة بغض النظر — مما يوحي أن التوازن بين هذين النوعين من البلعميات قد يحدّد ما إذا كانت الخلايا التائية قادرة على شن هجوم فعّال.
الحيل الجينية وتنوّع الورم
لفهم سبب تهرّب بعض أورام MSI من الجهاز المناعي، فحص الباحثون التغيرات الجينية التي تؤثر على كيفية عرض بروتينات الورم للخلايا المناعية وكيفية تطبيق «الفرامل» على الاستجابة المناعية. كانت طفرات في مكونات رئيسية من آلية عرض المستضدات شائعة في كل من أورام MSI المرتبطة بلينش والعَرَضية، لكن الفروق بين المجموعتين كانت طفيفة. الأكثر لفتًا للانتباه كانت الاختلافات في إشارات «نقاط التفتيش» المناعية. عبّرت الأورام العَرَضية عن مستويات أعلى من PD-L2 وCD40L، وهما جزيئتان يمكن أن تشكّلا سلوك الخلايا المناعية ويجري استكشافهما كأهداف دوائية بالتزامن مع مثبطات نقاط التفتيش الحالية. كما قاس الفريق عدد المستضدات الجديدة المحتملة (النيوأنتيجينات) في كل ورم ومدى تجانس الورم أو تنوعه جينيًا (كلوني مقابل متغاير). بشكل مفاجئ، لم يترجم الحمل الأعلى المتوقع من النيوأنتيجينات إلى كثافة أكبر من الخلايا التائية. بدلًا من ذلك، كانت الأورام الأكثر تنوعًا جينيًا — وخصوصًا أورام MSI العَرَضية — تميل إلى حمل المزيد من النيوأنتيجينات لكن أظهرت أيضًا أنماطًا، مثل انخفاض وجود العدلات، ما يشير إلى أن الجهاز المناعي لم يستغل هذه الأهداف بالكامل.
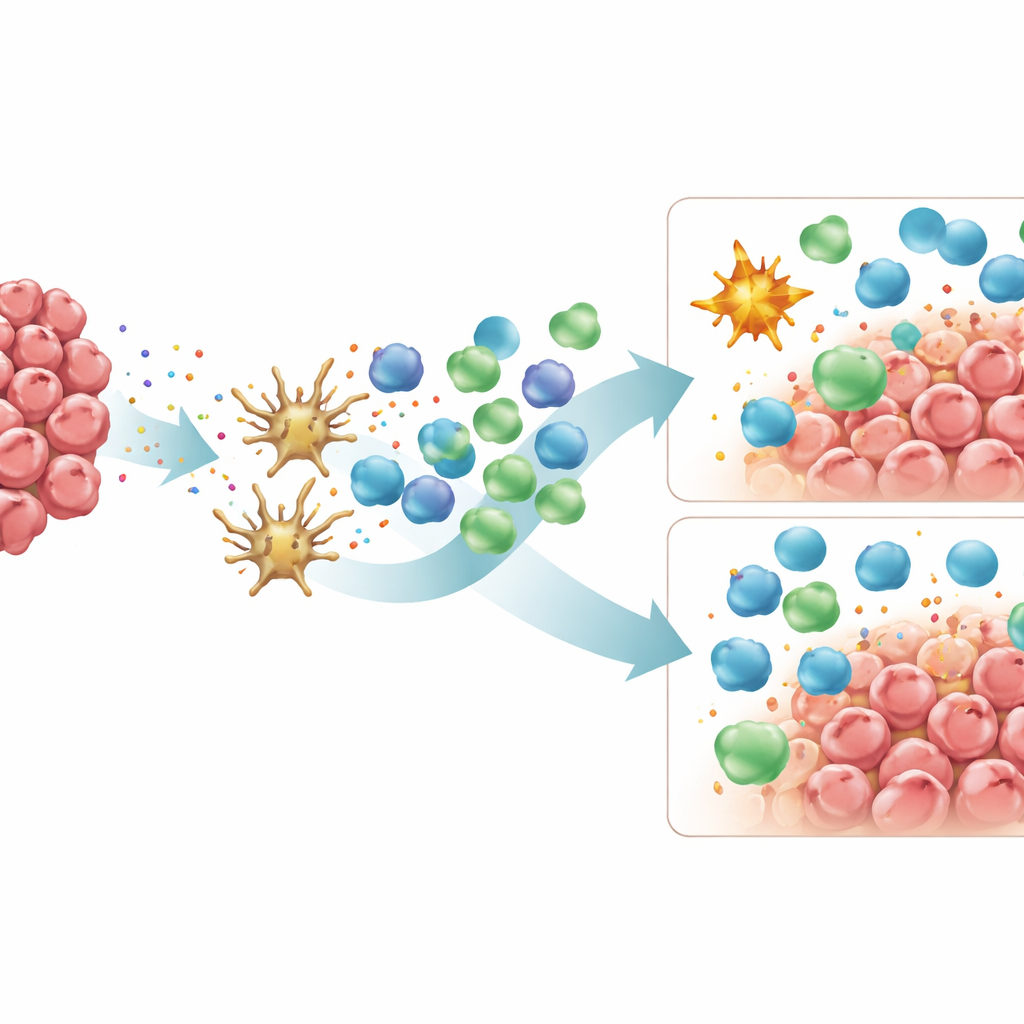
ما يعنيه هذا للعلاجات المستقبلية
بشكل عام، تصوّر الدراسة أورام MSI المرتبطة بلينش كأورام "ساخنة" باستمرار وغنية بالخلايا التائية، في حين تشكّل أورام MSI العَرَضية مجموعة أكثر تنوعًا، بعضها مخترق بشكل قوي والآخر محاط ببلعميات مثبطة للمناعة وتعابير أعلى لبعض جزيئات نقاط التفتيش. في الوقت نفسه، تُظهر الأورام العَرَضية غالبًا تنوعًا جينيًا أعلى وعبئًا ثقيلاً من النيوأنتيجينات الموزعة عبر طفرات فرعية مختلفة للورم — نمط تشير أعمال سابقة إلى أنه قد يضعف فعالية الاستجابات التائية. للمريضين، تساعد هذه النتائج في تفسير سبب عدم استجابة كل أورام MSI لِلْعِلاج المناعي بنفس الدرجة، على الرغم من اشتراكها في معدل طفرات مرتفع. وتشير أيضًا إلى استراتيجيات جديدة، مثل أدوية تعيد برمجة أو تقلّل من البلعميات الشبيهة بـM2 أو علاجات تستهدف نقاط تفتيش إضافية مثل PD-L2 وCD40L، التي قد تكون ذات صلة بشكل خاص بالأورام العَرَضية. من خلال مطابقة أساليب العلاج بشكل أفضل مع المشهد المناعي الفريد لكل ورم، قد يتمكن الأطباء من تحسين وتفصيل نتائج العلاج المناعي في سرطان القولون والمستقيم.
الاستشهاد: Martin, S., Elomaa, H., Väyrynen, J.P. et al. Tumour immune contexture and immune evasion in sporadic and Lynch syndrome-associated microsatellite unstable colorectal cancers. Br J Cancer 134, 1019–1030 (2026). https://doi.org/10.1038/s41416-025-03302-z
الكلمات المفتاحية: سرطان القولون والمستقيم غير المستقر في الميكروساتيلّايت, متلازمة لينش, الميكروبيئة المناعية للورم, البلعميات المرتبطة بالورم, العلاج المناعي للسرطان