Clear Sky Science · ar
البصمات الوظيفية لقصور إعادة التركيب المتماثل في سرطان البروستاتا كما تكشفها تجزئة ctDNA والوصول لعوامل النسخ
لماذا هذا مهم لمرضى السرطان
يمكن أن يستفيد العديد من الرجال المصابين بسرطان البروستاتا المتقدم من أدوية تستغل نقاط الضعف في آليات إصلاح الحمض النووي في أورامهم. ومع ذلك، غالبًا ما يفشل الأطباء اليوم في تحديد من سيستجيب لأن الاختبارات تتطلب عادة خزعات نسيجية صعبة وتركز على عدد محدود من الجينات. تُظهر هذه الدراسة كيف يمكن لتحليل بسيط لعين دم أن يتحول إلى قراءة متعددة الطبقات لهذه القصور في إصلاح الحمض النووي، مما قد يوجه خيارات علاجية أكثر دقة ورفقًا بالمرضى.
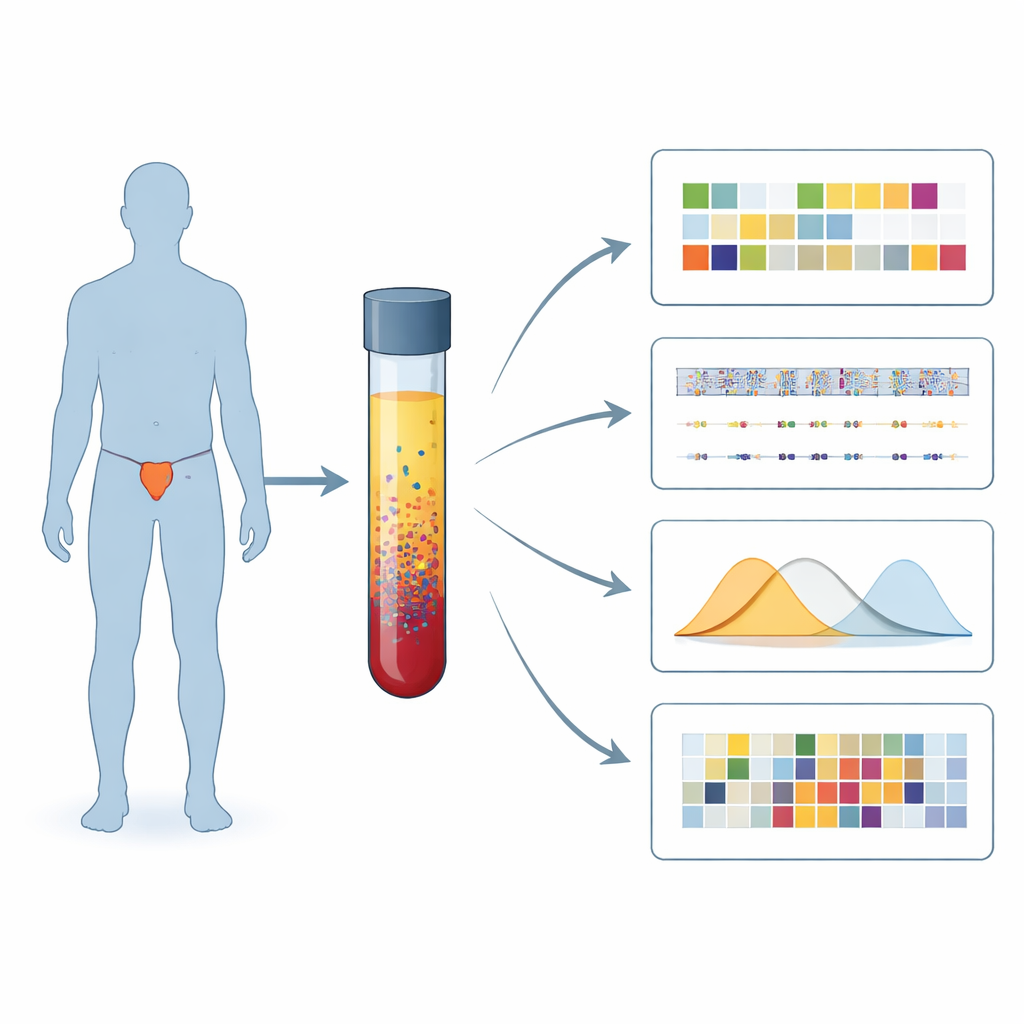
طريقة جديدة لقراءة إشارات السرطان من الدم
ركز الباحثون على مشكلة إصلاح محددة تُسمى قصور إعادة التركيب المتماثل (HRD)، التي تجعل الأورام عرضة بشكل خاص لأدوية مثل مثبطات PARP وبعض أنواع العلاج الكيميائي. بدلاً من الاعتماد على عينات الورم المأخوذة من العظام أو نسيج البروستاتا، حللوا أجزاءً من الحمض النووي الورمي العائمة في مجرى الدم والمعروفة بالحمض النووي الورمي المتداول. من بين 375 رجلاً مصابًا بسرطان البروستاتا النقيلي، اختاروا 106 أفرادًا كانت عينات دمهم تحتوي على ما يكفي من الحمض النووي الورمي للدراسة المتعمقة ثم طبقوا عدة اختبارات تكميلية على نفس عينات البلازما.
النظر إلى ما وراء طفرات الجينات المفردة
أولاً، قاموا بتسلسل لوحة من جينات إصلاح الحمض النووي الرئيسية، بما في ذلك أمثلة معروفة مثل BRCA2 وBRCA1 وPALB2، بالإضافة إلى جينات أخرى تشكل مدى عدوانية أورام البروستاتا. برزت BRCA2 كأكثر جينات الإصلاح تغييرًا وظهرت غالبًا مصاحبة لفقدان حواجز أمان مهمة أخرى مثل PTEN وRB1. لكن الفريق فحص أيضًا تغيُّرات واسعة النطاق في بنية الكروموسومات عبر الجينوم بأكمله، مستخدمين تسلسل الجينوم الكامل منخفض العمق لحساب درجة عدم استقرار جينومي. كانت الأورام التي تحمل جينات BRCA متضررة، أو ذات درجات عالية، تتمتع بجينومات معاد ترتيبها بشكل كبير وكانت مرتبطة ببقاء إجمالي أسوأ، مما يبرز أن التغيرات الهيكلية الكبيرة يمكن أن تكون مفيدة بالمثل مثل الطفرات المحددة.
بصمات فشل الإصلاح في أنماط الطفرات
في مجموعة فرعية من المرضى، تعمق العلماء أكثر من خلال تسلسل جميع المناطق المشفرة للبروتين لقراءة نمط الطفرات المفصل التي تراكمت مع مرور الوقت. تعمل تركيبات معينة من تغييرات القواعد والإدخالات أو الحذف الصغيرة كبصمات لعمليات محدثة لها. وجدوا أن التواقيع الكلاسيكية المرتبطة بـHRD، مثل توقيع يُدعى SBS3 ونمط إدخالات/حذف يُعرف باسم ID6، كانت مثرية في الأورام ذات عيوب جينات الإصلاح وذات عدم استقرار جينومي عالٍ. أشارت تواقيع أخرى إلى مشاكل منفصلة، مثل فشل إصلاح عدم التطابق أو نمط فرعي مميز يقوده CDK12، مما يؤكد أن انهيارات مختلفة في آليات إصلاح الحمض النووي تترك ندوبًا متميزة في الجينوم.
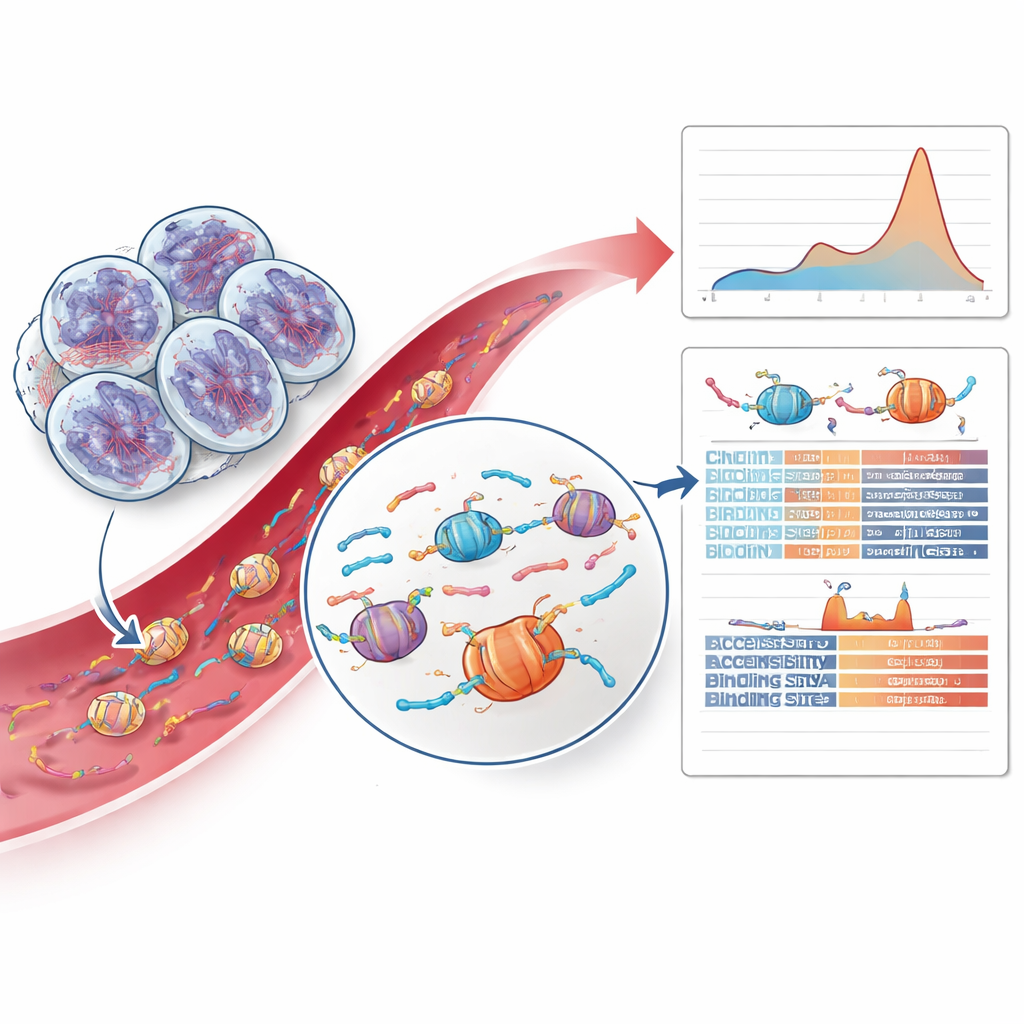
فك شيفرة أنماط شظايا الحمض النووي ودلائل الكروماتين
تجاوز الجزء الأكثر ابتكارًا من العمل الطفرات بالكامل وفحص كيف تم تقطيع شظايا الحمض النووي الورمي. عندما تموت الخلايا، يُقطع حمضها النووي حول حزم بروتينية تُدعى النوكليوسومات، مكوّنًا شظايا ذات أطوال ونهايات مميزة. اكتشف الفريق أن الأورام المصابة بـHRD أظهرت فائضًا نسبيًا في الشظايا الأطول قليلًا المقابلة لوجود نوكليوسومين، وهو تحول لم يظهر في حالات سرطان البروستاتا الأخرى أو في الضوابط الصحية. من خلال تدريب نموذج حذر للتعلم الآلي على أطوال الشظايا وميزات نهايات الشظايا، تمكنوا من تمييز الحالات الإيجابية لـHRD من الدم وحده بدقة واعدة. كما تحققوا من وصولية مناطق مختلفة من الجينوم حول مواقع ربط عوامل النسخ—البروتينات التي تتحكم في نشاط الجينات—ووجدوا أن مواقع ربط بعض عوامل الإصبع الزنّية كانت أقل وصولية في أورام HRD، مما يشير إلى تغييرات أعمق متعلقة بالإصلاح في تنظيم الكروماتين.
ماذا قد يعني هذا للمرضى
تشكل هذه الطبقات من المعلومات معًا—من طفرات جينية محددة وإعادة ترتيب كروموسومات واسعة إلى تحولات دقيقة في حجم شظايا الحمض النووي ووصولية الكروماتين—صورة أكمل لضعف إصلاح الحمض النووي في سرطان البروستاتا. للقراء غير المتخصصين، الرسالة الأساسية هي أن عينة دم محللة بعناية يمكن أن تكشف ليس فقط عما إذا كانت جينة مألوفة مثل BRCA2 مطفرة، بل ما إذا كان الورم يتصرف كما لو أنه يعاني من عيب إصلاح خطير، حتى عندما تبدو الاختبارات الاعتيادية طبيعية. إذا تم التحقق من ذلك في مجموعات أكبر وأكثر تنوعًا من المرضى، فقد تساعد هذه الطريقة المتعددة الوسائط المعتمدة على الدم الأطباء في تحديد من المرجح أن يستفيد من مثبطات PARP أو أدوية البلاتينوم بصورة أكثر موثوقية، ومراقبة التغيرات مع الزمن، وتخصيص العلاج باستخدام اختبار بسيط وقابل للتكرار.
الاستشهاد: Vlachos, G., Moser, T., Lazzeri, I. et al. Functional footprints of homologous recombination deficiency in prostate cancer revealed by ctDNA fragmentation and transcription factor accessibility. Br J Cancer 134, 949–960 (2026). https://doi.org/10.1038/s41416-025-03301-0
الكلمات المفتاحية: سرطان البروستاتا, الخزعة السائلة, إصلاح الحمض النووي, الحمض النووي الورمي المتداول, مثبطات PARP