Clear Sky Science · ar
طيف ووظائف قنوات الأيونات والناقلات في الخلايا الهادمة للعظم
لماذا تحتاج عظامنا إلى حُراس صغار
هيكلنا العظمي يبدو صلباً وثابتاً، لكنه يتعرَّض باستمرار لهدم وإعادة بناء. خلايا متخصصة تُسمى الخلايا الهادمة للعظم تعمل كفريق هدم، إذ تذيب العظام القديمة ليتكوّن عظم جديد. تستعرض هذه المقالة العلمية طاقماً مخفياً من بروتينات «حراس البوابات» المجهرية — قنوات الأيونات والناقلات — التي تسمح للذرات المشحونة والمواد المغذية بالدخول والخروج من الخلايا الهادمة. من خلال فهم كيفية تحكّم هذه البوابات الدقيقة في تكسّر العظم، يأمل العلماء في تصميم علاجات أفضل لهشاشة العظام وأمراض العظام الأخرى.
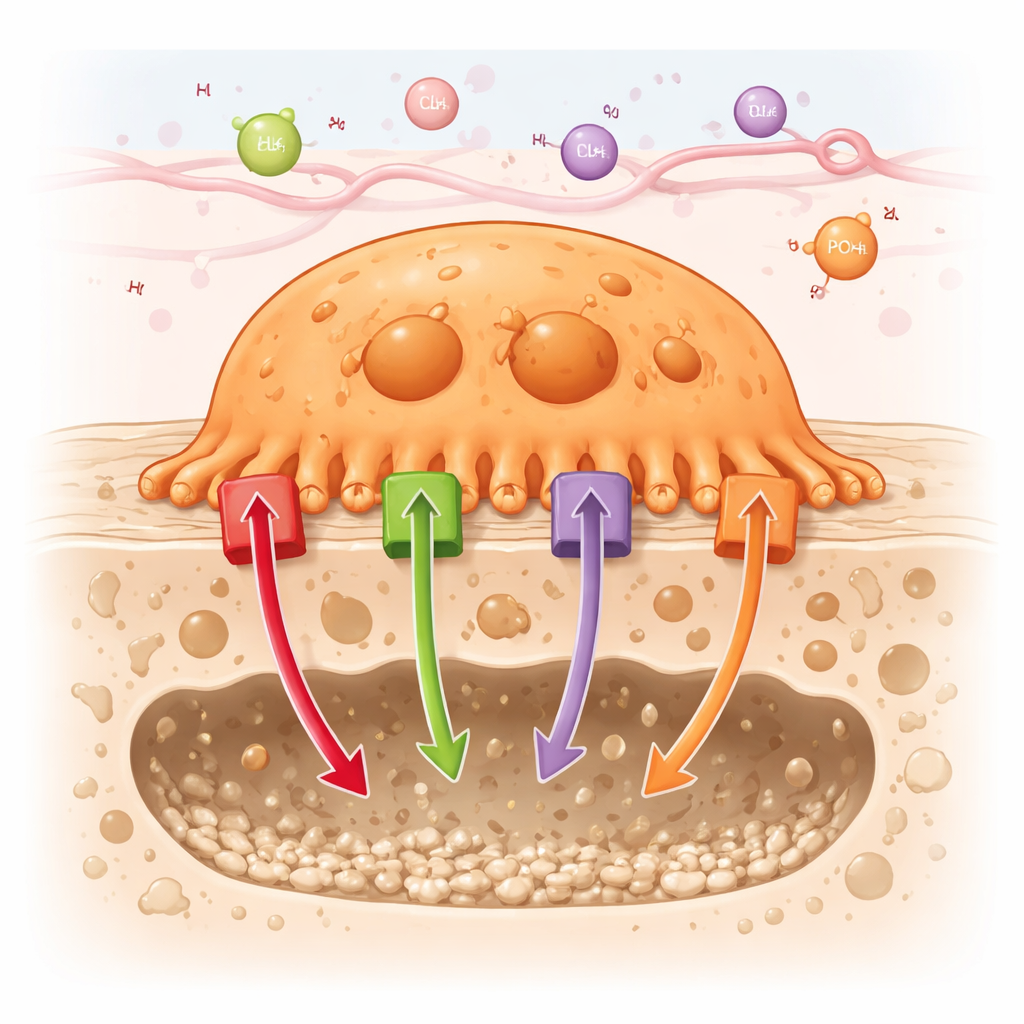
كيف تقوم خلايا أكل العظم بعملها
تعمل الخلايا الهادمة للعظم بالالتصاق بقوة بسطح العظم وخلق جيب معزول يمكنها فيه إذابة المعادن وهضم البروتينات بأمان. لجعل هذه «حجرة الهضم» الصغيرة شديدة الحموضة، تضخ الخلايا الهادمة أعداداً كبيرة من البروتونات (أيونات الهيدروجين) إلى الجيب. وفي الوقت نفسه، تنقل أيونات أخرى — مثل الكلور والكالسيوم والفوسفات — عبر أغشيتها والحجرات الداخلية. تستعرض المقالة نحو 90 قناة وناقلاً مختلفاً موجوداً في الخلايا الهادمة للعظم وتُصنّفها إلى ست عائلات، بما في ذلك المضخات المدفوعة بالطاقة (ATPases)، قنوات الكاتيونات والأنيونات، الناقلات المقترنة، ناقلات المغذيات، وناقلات مرَبِطة بمستقبلات ATP (ABC).
الحمض والملح والطاقة: الآلية الأساسية
يبرُز نظامان بروتينيان كعناصر مركزية في امتصاص العظم. أولاً، مضخات البروتون الحُبيبية المعروفة باسم V-ATPases تدفع البروتونات بنشاط إلى جيب الامتصاص، مما يجعل البيئة حامضية بما يكفي لإذابة المعادن العظمية وتنشيط الإنزيمات القاطعة للبروتينات. تُثبّت وحدات فرعية محددة من V‑ATPase، مثل a3 وd2 وعدد من مكوّنات V1، على الحدود المتموِّجة للخلايا الهادمة وفي الليزوسومات، ويمكن أن تؤدي العيوب الجينية في هذه الوحدات إلى ضعف العظم أو إلى سماكة عظمية مرضية. ثانياً، مُبادِل الكلور–بروتون المعروف باسم ClC‑7، الذي يتعاون مع بروتين يُدعى OSTM1، يُدخل أيونات الكلور إلى نفس المنطقة. هذا يوازن الشحنة الكهربائية ويسمح باستمرار ضخ البروتونات. عند حدوث طفرات في ClC‑7، يصاب البشر والفئران بمرض العظام الكثيفة (o steopetrosis)، وهي حالة تتميز بعظام كثيفة للغاية لكنها هشة، مما يوضّح مدى أهمية تدفّق الأيونات الصحيح لصحة الهيكل العظمي الطبيعية.
الكالسيوم والفوسفات واللاعبون المساعدون الآخرون
بعيداً عن إنتاج الحمض، تعتمد الخلايا الهادمة على تنظيم دقيق للتعامل مع الكالسيوم والفوسفات. شبكة من قنوات ومضخات الكالسيوم في غشاء الخلية والشبكة الإندوبلازمية والليزوسومات والميتوكندريا تولِّد «تذبذبات» دورية للكالسيوم تُفعّل الجينات الأساسية لتكوّن واندماج الخلايا الهادمة. تنقل ناقلات على الحدود المتموِّجة والجانب المقابل للخلية الكالسيوم والفوسفات الخارجَين من العظم المُذاب، إما لإعادة تدويرهما داخل الخلية أو إعادتهما إلى الدورة الدموية. كما تُتحكم ناقلات متخصصة في معادن ومعادن أثرية أخرى — مثل المنغنيز والمغنيسيوم والزنك والنحاس والحديد — وتؤثر على شدة قيام الخلايا الهادمة بامتصاص العظم. على سبيل المثال، يمكن للحديد وأشكال معينة من موت الخلية المرتبطة بالحديد أن ترفع أو تخفض نشاط الخلايا الهادمة، بينما تميل ناقلات الزنك إلى كبح فقدان العظم المفرط.
تنظيم الحركة داخل الخلية
ليست قنوات الأيونات محصورة بالغشاء الخارجي فحسب. فالكثير منها موجود على حجيرات داخلية مثل الليزوسومات والحويصلات الداخلية وجهاز غولجي والميتوكندريا، مكوّنة شبكة نقل متعددة الطبقات. تساعد هذه البوابات الداخلية في ضبط الأس الهيدروجيني في الحويصلات الهاضمة، وإنتاج الطاقة في الميتوكندريا، وحركة الإنزيمات والحطام. تبرز المراجعة كيف تتعاون أنظمة قنوات متعددة: مبادلات الصوديوم–الهيدروجين تُنظّم الحموضة الداخلية، ومشتركات البوتاسيوم–الكلور تساعد في الحفاظ على فرق الجهد وتوازن الكلور، وقنوات بورينيرجيك وحساسة ميكانيكياً تحول الإشارات الكيميائية أو الميكانيكية إلى تغييرات في امتصاص العظم. كما تدعم ناقلات المغذيات للجلوكوز والأحماض الأمينية والنوكليوزيدات وفيتامين C متطلبات الطاقة والتخليق الحيوي العالية للخلايا الهادمة النشطة.
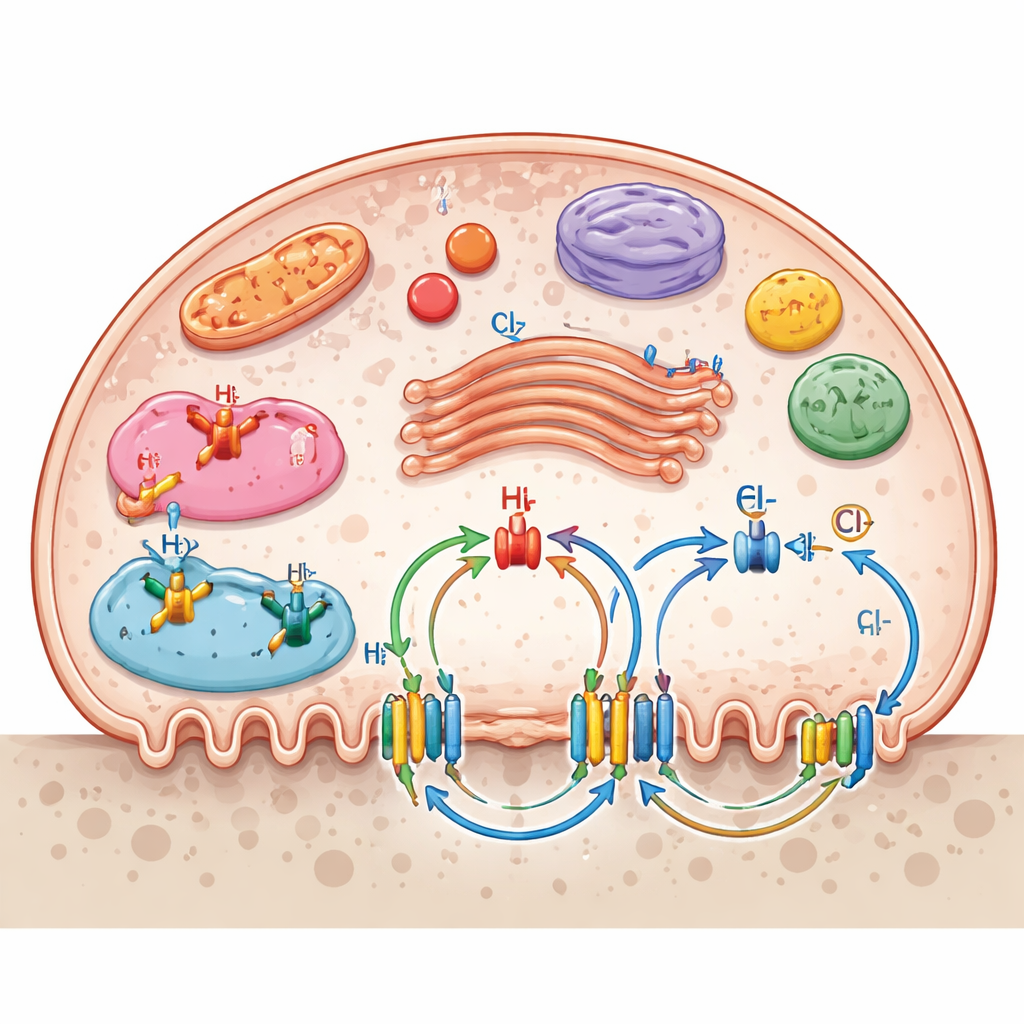
من البيولوجيا الأساسية إلى علاجات جديدة
لأن العديد من اضطرابات العظام تنشأ عندما تكون الخلايا الهادمة مفرطة النشاط أو ناقصة النشاط، فإن القنوات والناقلات التي توجّه سلوكها تمثّل أهدافاً دوائية جذابة. يستعرض المؤلفون مركبات موجودة وتجريبية تعيق V‑ATPases، قنوات TRP للكالسيوم، مبادلات الكلور، مستقبلات البورينيرجيك وناقلات أخرى، وكذلك أفكاراً أحدث مثل تعطيل تفاعلات وحدات فرعية محددة أو استخدام جُسيمات نانومترية موجهة لتوصيل الدواء مباشرة إلى العظم. ويؤكدون أن العديد من هذه البروتينات موجودة أيضاً في أنسجة أخرى، لذا يبقى تحقيق خصوصية فعلية للخلايا الهادمة تحدياً. ومع ذلك، مع تزايد أدوات الجينوم والتصوير التي تكشف المزيد عن مواقع هذه القنوات وكيفية تفاعلها، من المرجح أن يُنتج «خريطة الأيونات» المتوسعة للخلايا الهادمة علاجات أكثر دقة لهشاشة العظام وفقدان العظم الالتهابي والأمراض العظمية الوراثية النادرة.
الاستشهاد: Chen, H., Zhang, Y., Zhu, Y. et al. Spectrum and functions of ion channels and transporters in osteoclasts. Bone Res 14, 35 (2026). https://doi.org/10.1038/s41413-026-00513-9
الكلمات المفتاحية: الخلايا الهادمة للعظم, قنوات الأيونات, إعادة امتصاص العظم, V-ATPase, هشاشة العظام