Clear Sky Science · ar
C/EBPβ يحدد نسخ FSHβ بعد سن اليأس وعرقلة مسار AEP/C/EBPβ يخفّف هشاشة العظام
لماذا تهم هذه الدراسة الحياة بعد انقطاع الطمث
تُخبر الكثير من النساء أن انخفاض الإستروجين هو السبب الرئيسي وراء هشاشة العظام بعد انقطاع الطمث. تضيف هذه الدراسة قطعة جديدة إلى اللغز: هرمون آخر، الهرمون المحفز للجريب (FSH)، وزوج من البروتينات في الدماغ والعظام—C/EBPβ وAEP—يتعاونان لتسريع فقدان العظام. والأكثر إثارة، أن الباحثين أظهروا في الفئران أن حجب هذا المسار بحبوب تجريبية يمكن أن يحمي العظام بفعالية مشابهة لدواء معتمد لعلاج هشاشة العظام.
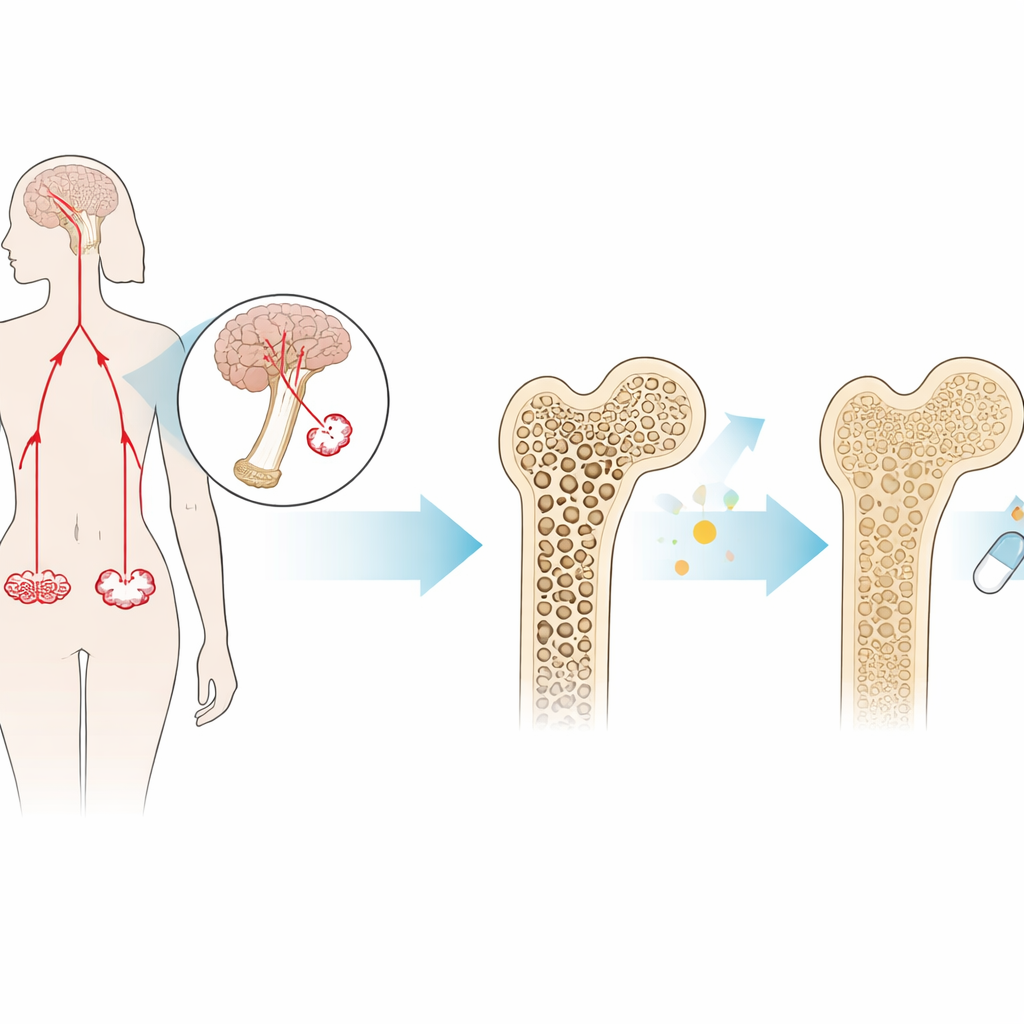
هرمون أقل شهرة لكن له تأثير كبير على العظام
يُنتَج FSH في غدة النخامية ويشتهر بدوره في الخصوبة. عند النساء اللاتي يقتربن من انقطاع الطمث، ترتفع مستويات FSH بشكل حاد قبل عدة سنوات من آخر دورة شهرية. بعيداً عن دوره التناسلي، يمكن أن يؤثر FSH مباشرة على العظام: يرتبط بمستقبلات على خلايا هاضمة للعظم (خلايا ناقضة العظم)، ويحفزها على تكسير العظم أسرع مما يُعاد بناؤه. أظهرت أعمال سابقة أن الفئران التي تفتقر إلى FSH أو إلى مستقبلاته تكون محمية من فقدان العظام، حتى عندما يكون الإستروجين منخفضاً. وهذا يوحي بأن FSH نفسه، وليس نقص الإستروجين وحده، يمكن أن يدفع هشاشة العظام بعد انقطاع الطمث.
مفتاح التحكم في النخامية
تركز الدراسة الجديدة على C/EBPβ، بروتين يرتبط بالحمض النووي ويشغّل أو يطفئ الجينات. اكتشف المؤلفون أن C/EBPβ يرتبط مباشرة بمنطقة التحكم في جين وحدة بيتا للـ FSH—الجزء من الهرمون الذي يحدد هويته—ويعزز إنتاجه في النخامية. في خلايا نخامية مزروعة، أدى رفع مستوى C/EBPβ إلى زيادة FSH، بينما أدى إسكات C/EBPβ إلى خفض FSH، لا سيما عندما حُفّزت الخلايا بإشارة التكاثر من الدماغ، GnRH. في فئران أُزيلت مبايضها، والتي تحاكي انقطاع الطمث عن طريق إزالة المبايض المفرزة للإستروجين، أنتجت الحيوانات ذات مستوى C/EBPβ المنخفض FSH أقل بكثير في غدة النخامية والدم. تكشف هذه التجارب عن C/EBPβ كمفتاح يحدد مقدار ارتفاع FSH بعد انخفاض الإستروجين.
حلقة تغذية راجعة وتعريف هدف دوائي جديد
يتحكم C/EBPβ أيضاً في بروتين آخر يسمى AEP، وهو إنزيم قاطع يمكنه تفعيل أو تعطيل جزيئات أخرى. في الدماغ، رُبطت سلسلة C/EBPβ–AEP بأضرار شبيهة بالألزهايمر. هنا، سأل الفريق ما إذا كانت هذه السلسلة نفسها تغذي FSH والعظام. في الفئران التي تفتقر إلى AEP، انخفضت مستويات كل من C/EBPβ وFSH في النخامية، وتقلّص فقدان العظام بعد استئصال المبايض. أدى حجب AEP بمركب صغير جزيئياً، أُطلق عليه #11a، إلى تأثير مماثل: بعد أشهر من العلاج، كان لدى الفئران المستأصلة مبايضها مستويات أقل من FSH، وعظام أقوى في الصور عالية الدقة، وعدد أقل من خلايا تآكل العظم المفرطة النشاط. فئة أخرى من المركبات—منشطات TrkB التي تقلل AEP بشكل غير مباشر—ساعدت خلايا العظام في التجارب المختبرية لكنها لم تتمكن من خفض FSH في الحيوانات، إلى حد كبير لأن مستقبلها الهدف نادر في النخامية. أكسب هذا التباين الاستنتاج أن تثبيط AEP مباشرة هو وسيلة أقوى لإيقاف محور C/EBPβ–FSH عند المصدر.
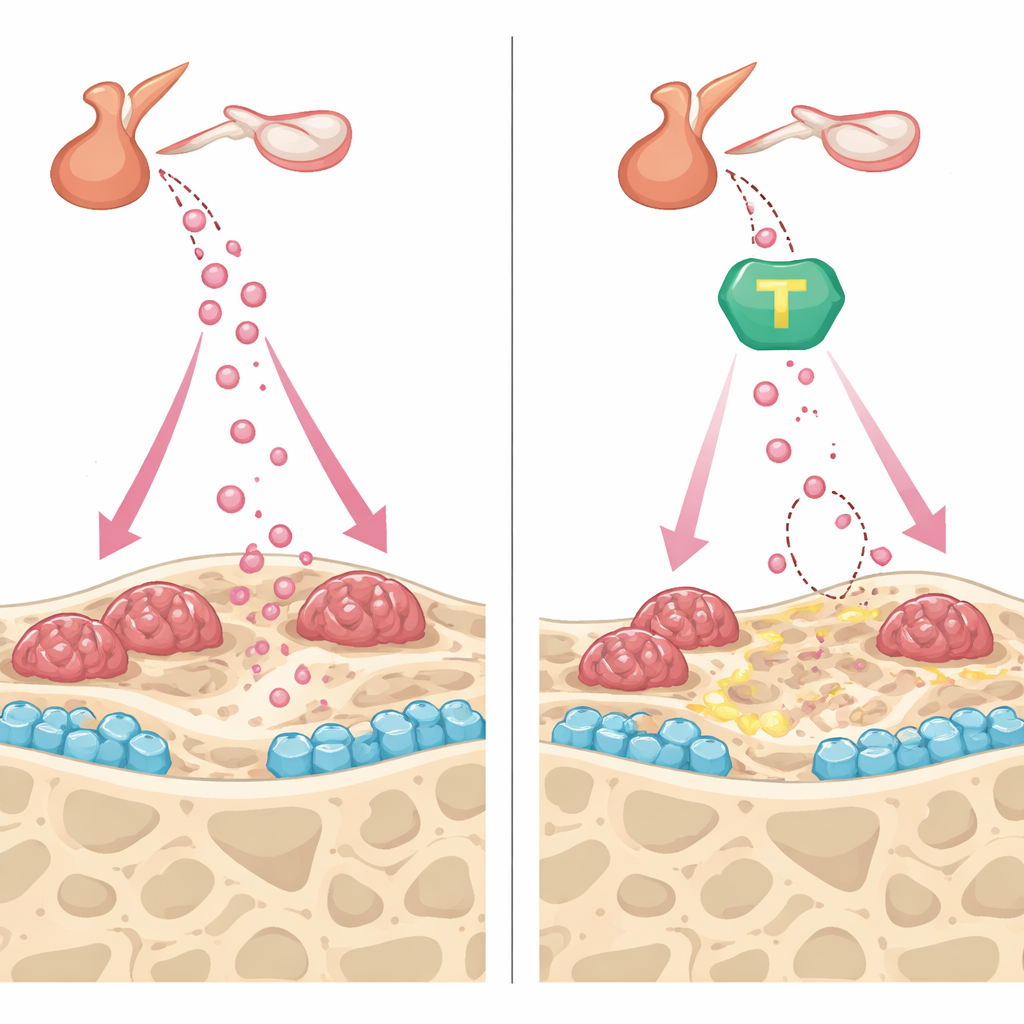
حماية العظام من زاويتين
بعيداً عن خفض FSH، أظهر كل من #11a ومنشط TrkB المسمّى CF3CN فوائد متكملة داخل العظم نفسه. في مزروعات خلايا مكوّنة للعظم، سرّعت المركبان النضج وترسيب المعادن، جزئياً عن طريق الحفاظ على الفيبرونيكتين، وهو بروتين هيكلي يقوم AEP عادة بقطعه، وعن طريق تعزيز إشارات داعمة للعظم مثل أوستيوبروتيجيرين. في خلايا تآكل العظم، خفّفت الأدوية تأثير إشارة رئيسية للتآكل، مما قلّل عدد الخلايا متعددة النوى الكبيرة وقدرتها على نحت فجوات في شرائح العظم. في الفئران الحية، كبح كل من #11a وCF3CN دوران العظام السريع الناجم عن استئصال المبايض، مثبتين كثافة العظم والبنية الميكروية. ولافت أن الحبة التجريبية #11a، عند مقارنتها مباشرةً بتيريباراتيد، الدواء المعتمد القابل للحقن الذي يبني العظم، حققت قدرة مماثلة لتركيب التيريباراتيد على استعادة حجم العظم وقوته في هذا النموذج.
ما الذي قد يعنيه هذا لرعاية هشاشة العظام المستقبلية
لغير المتخصص، الخلاصة أن هذا العمل يحدد مساراً ذا وظيفتين يربط بين الالتهاب المرتبط بانقطاع الطمث وارتفاع FSH وتلف العظم، ويظهر أن استهداف AEP يمكن أن يقطع هذه السلسلة. في الفئران، لم يقتصر مثبط AEP الفموي على خفض FSH الزائد الذي يغذي فقدان العظم، بل أعاد أيضاً توازن العمليات داخل العظم نحو البناء بدلاً من التفكك. وبينما تحتاج هذه النتائج إلى اختبارها في البشر، فإنها توحي بأن علاجات هشاشة العظام المستقبلية قد تتجاوز مجرد استبدال الإستروجين أو تحفيز بناء العظم، وبدلاً من ذلك تهدئ هذه الدائرة الهرمونية والإنزيمية الموصوفة حديثاً التي تسبّب هشاشة العظام بعد انقطاع الطمث.
الاستشهاد: Xie, Z., Liao, J., Xiong, J. et al. C/EBPβ dictates postmenopausal FSHβ transcription and blockade of AEP/C/EBPβ pathway alleviates osteoporosis. Bone Res 14, 31 (2026). https://doi.org/10.1038/s41413-026-00510-y
الكلمات المفتاحية: هشاشة العظام بعد انقطاع الطمث, الهرمون المحفز للجريب, مسار C/EBPβ AEP, إعادة تشكيل العظام, علاج موجه هرمونياً