Clear Sky Science · ar
تشكّل الندبة الليفية المحفز بواسطة TGF-β يقيّد تعافي إصابة الحبل الشوكي
لماذا تُهمّ الندوب في الحبل الشوكي
عندما يتعرض الحبل الشوكي لإصابة شديدة، يبقى كثيرون مشلولين بشكل دائم أو يفقدون الإحساس لأن ألياف الأعصاب المتضررة تفشل في النمو مجدداً. يطرح هذا البحث سؤالاً بسيطاً لكنه محوري: ما الذي يعيق هذا النمو بالضبط — وهل يمكننا إزالة العائق بأمان؟ عبر الكشف عن كيفية تشكّل نوع محدد من الندبة داخل النسيج المصاب، يشير الباحثون إلى نهج جديد لمساعدة الجهاز العصبي على إصلاح نفسه.
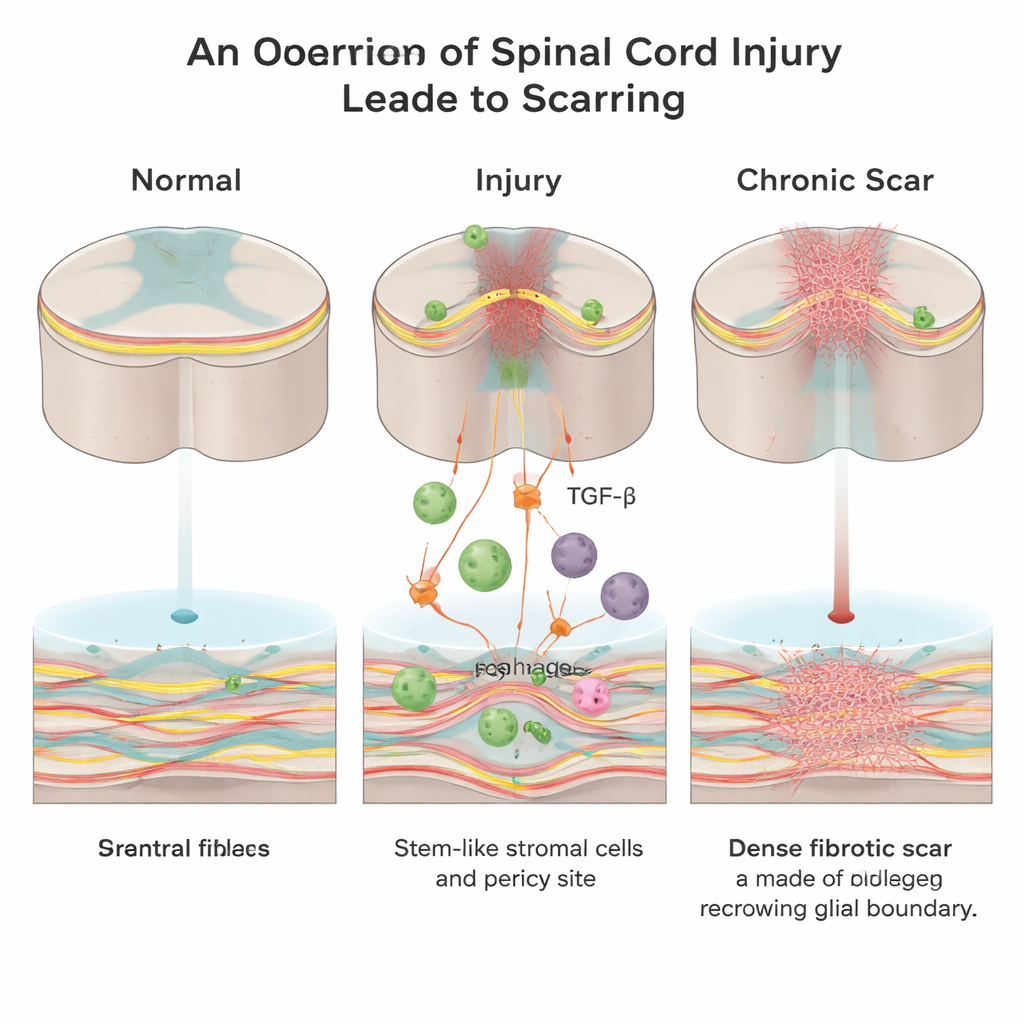
جدار مخفي داخل موقع الإصابة
بعد إصابة الحبل الشوكي، يتعجل الجسم لإغلاق الجرح. يتكوّن نوعان رئيسيان من نسيج الندبة: ندبة «نجمية» تصنعها خلايا داعمة تُسمى الخلايا النجمية، وندبة «ليفية» غنية بالكولاجين والفايبرونيكتين وخلايا الليفاضة. بينما قد تلعب الندبة النجمية أدواراً وقائية، تخلق الندبة الليفية جداراً مادياً وكيميائياً كثيفاً لا تستطيع ألياف الأعصاب النامية عبوره بسهولة. حتى الآن، كان العلماء يعرفون أقل بكثير عن كيفية ظهور هذا اللب الليفي وإي أي الإشارات تدفع تشكّله.
دور خلايا الجهاز المناعي وإشارة قوية
عمل الباحثون على فئران بالغة، وركزوا على جزيء إشاري يُسمى عامل نمو التحول بيتا (TGF‑β)، الذي يساعد على تنسيق إصلاح الجروح في أنحاء الجسم وغالباً ما يكون فرط نشاطه مرتبطاً بالأمراض الليفية. وجدوا أنه بعد إصابة الحبل الشوكي، تصبح الخلايا المناعية الوافدة المعروفة بالبلاعم مصدراً رئيسياً لـ TGF‑β1 النشط في موضع الآفة. هذا الارتفاع في TGF‑β1 يجتذب الخلايا الجذعية/التماسخية الميزنشيمية المحلية والخلايا المرتبطة بالأوعية المسماة البيريسايتات ويدفعها للتحوّل إلى خلايا ليفاضة — وهي الخلايا التي ترسب الكولاجين وتشكل الندبة الليفية.
خفض الإشارة لفتح ممر
لاختبار ما إذا كان هذا المسار يسبب الندب الضار فعلاً، استخدمت المجموعة عدة طرق جينية في الفئران. عندما أزالوا البلاعم، أو حذفوا جين TGF‑β1 فقط في خلايا سلالة البلاعم، انخفضت كمية النسيج الليفي في الحبل المصاب بشكل حاد، وتمكنت المزيد من الألياف العصبية والمسارات الحاملة للسيروتونين من عبور منطقة الإصابة. وبالمثل، أدى حذف مستقبل TGF‑β تحديداً في البيريسايتات إلى تقليل استجابتها لـ TGF‑β، وتقليل تراكم الكولاجين، وتحسّن في الحركة والإحساس في اختبارات السلوك. والأهم من ذلك أن البيريسايتات والخلايا الشبيهة بالجذعية بقيت موجودة لكنها أصبحت أقل ميلاً للتحول إلى خلايا ليفية مُشكِّلة للندبة.
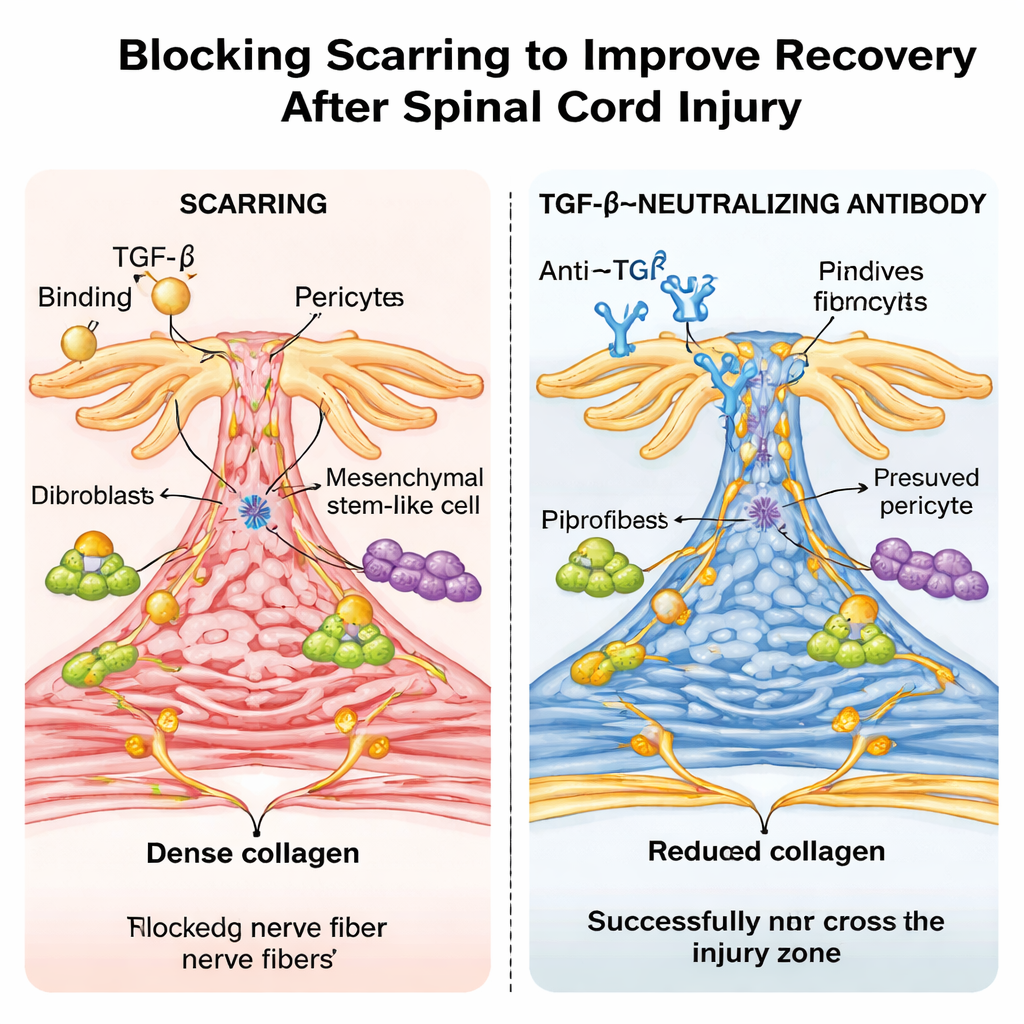
مضاد شبيه بالدواء وتأثير مفاجئ للعمر
ثم جرّب الباحثون نهجاً أكثر ملاءمة سريرياً: معالجة الفئران العادية بأجسام مضادة مخبرية تعادل TGF‑β. جرعات متكررة بعد الإصابة خفّضت مستويات TGF‑β النشط في الدم والحبل الشوكي، وصغّرت الندبة الليفية، ومكنت ألياف الأعصاب من ردم الفجوة عبر الآفة بشكل أفضل، مع مكاسب ملحوظة في المشي والوظيفة الحسية. أكدت تقنية تسلسل الحمض النووي الريبي أحادي الخلية أن الجينات المستجيبة لـ TGF‑β كانت عالية النشاط في أنواع الخلايا المكوِّنة للندبة في الفئران غير المعالجة، وأن الأجسام المضادة كبّحت نشاطها. اللافت أنه عندما أُجري نفس نوع سحق الحبل الشوكي في فئران حديثي الولادة، شُفيت الحيوانات تقريباً دون ندب ليفي، ولم يُرصد تفعيل لـ TGF‑β في موقع الإصابة، واستعادوا حركة قريبة من الطبيعية — على نحو يشبه الإصلاح الخالي من الندوب الذي يُرى في بعض الحيوانات غير الثديية.
ما الذي قد يعنيه هذا للعلاج المستقبلي
تلمح النتائج مجتمعة إلى أن فرط تفعيل TGF‑β بعد إصابة الحبل الشوكي يحرف خلايا الإصلاح المفيدة لتكوّن جدار ليفي جامد يعيق نمو الأعصاب والتعافي الوظيفي. من خلال منع هذا الإفراط في التفعيل — سواء باستهداف إنتاج TGF‑β في البلاعم، أو حجب مستقبلاته على البيريسايتات والخلايا اللحائية، أو باستخدام جسم مضاد معادِل — قد يكون من الممكن تقليل الندبة الضارة مع الحفاظ على أو حتى تعزيز أنواع أخرى من الاستجابة النسيجية المفيدة. وعلى الرغم من أن ترجمة هذه الاستراتيجيات إلى البشر ستتطلب دراسات حذرة لتجنب الآثار الجانبية، فإن هذا العمل يبرز التندب الليفي المحرَّك بواسطة TGF‑β كحاجز مركزي، وقابل للاستهداف دوائياً، أمام إصلاح الحبل الشوكي.
الاستشهاد: Pan, D., Wu, P., Noller, K. et al. TGF-β-induced fibrotic scar formation limits recovery of spinal cord injury. Bone Res 14, 27 (2026). https://doi.org/10.1038/s41413-026-00507-7
الكلمات المفتاحية: إصابة الحبل الشوكي, ندبة ليفية, TGF-بيتا, البلاعم, تجدد الأعصاب