Clear Sky Science · ar
HIF-1α و BMAL1 في تجدد العظم: تواصل بين استجابة نقص الأكسجين والإيقاع اليومي
لماذا تلتئم العظام المكسورة أفضل مما تظن
عندما نكسر عظمة أو يُقلع لنا سن، يطلق جسدنا بهدوء مشروع إصلاح منظم بشكل ملحوظ. في أعماق المنطقة المصابة، تنخفض مستويات الأكسجين ويستمر ساعتنا الداخلية البيولوجية في العمل. تستكشف هذه المقالة كيف يعمل مفتاحان رئيسيان — HIF‑1α، الذي يستشعر نقص الأكسجين، وBMAL1، أحد بروتينات الساعة الأساسية — معاً لتوجيه خلايا العظم عبر الالتهاب ونمو النسيج الجديد وحتى استعادة القوة النهائية. قد يؤدي فهم هذه الشراكة إلى تحسين علاجات الكسور، هشاشة العظام، التهاب المفاصل، وحتى الغرسات السنية.
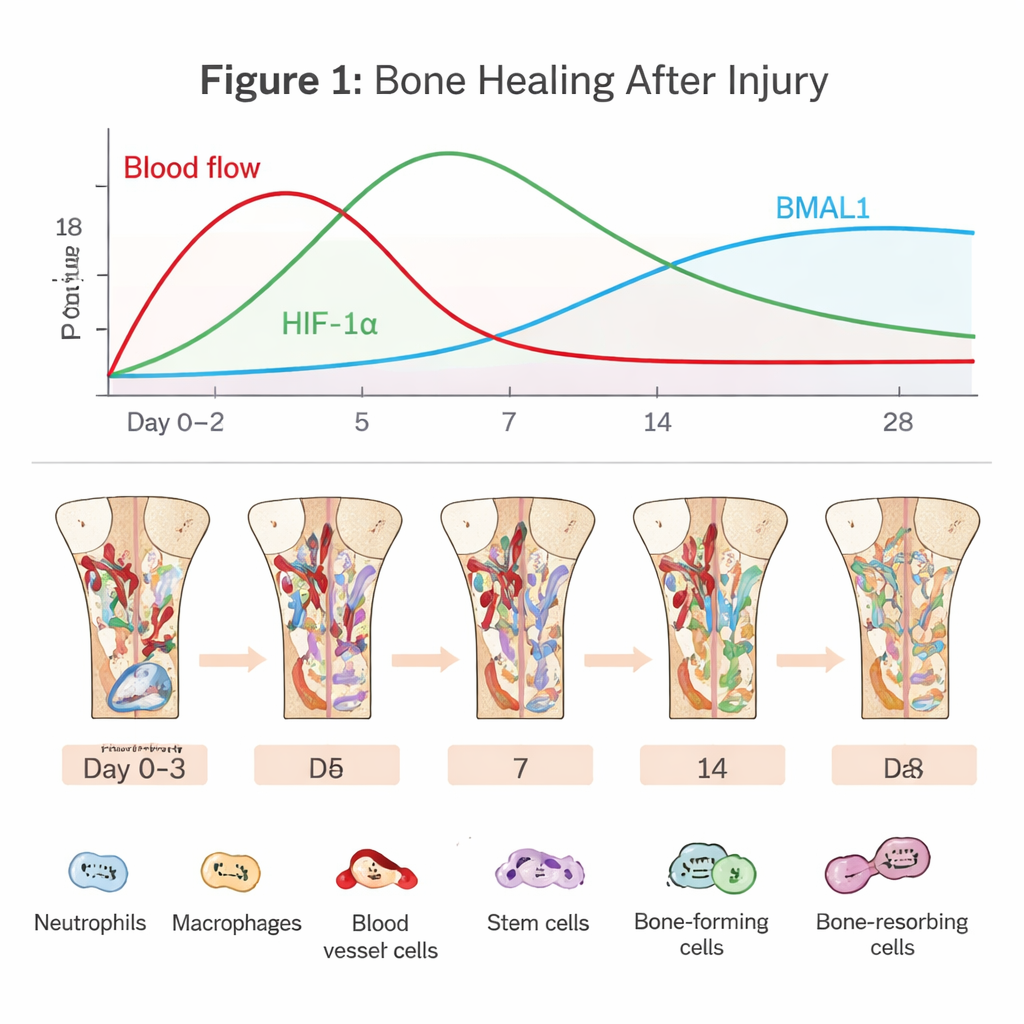
الدراما الخفية داخل عظم يلتئم
يبدأ تجدد العظم منذ اللحظة التي تتمزق فيها الأوعية الدموية. يتكوّن خثرة دموية تقطع معظم إمداد الأكسجين وتخلق جيباً قاسياً فقيراً بالأكسجين. تتدفق خلايا المناعة مثل العدلات والبلعميات لتنجِّي الحطام وتقاوم الميكروبات. في الوقت نفسه، تُستدعى خلايا جذعية من نخاع العظم وخلايا الأوعية الدموية لإعادة بناء المنطقة. تُعد مرحلة «الالتهاب» المبكرة سيفاً ذا حدين: دفعة قصيرة وموقوتة من الالتهاب تشعل الإصلاح، لكن إذا امتدت طويلاً أو كانت شديدة جداً فقد يتعثر الالتئام أو يفشل. تؤكد المقالة أن السير في هذا المسار الضيق يعتمد بدرجة كبيرة على كيفية استشعار الخلايا للأكسجين والوقت.
كيف تستغل الخلايا نقص الأكسجين لمصلحتها
في منطقة الكسر الفقيرة بالأكسجين، يستقر بروتين HIF‑1α ويشغّل جينات تساعد الخلايا على التكيّف. يدفع خلايا البطانة الوعائية إلى إنماء أوعية دموية جديدة، ما يضمن وصول أكسجين ومغذيات جديدة إلى العيب. كما يعيد برمجة أيض الخلايا نحو تحلل السكر (الجليكوليز)، طريقة لتوليد الطاقة تعمل حتى عندما يكون الأكسجين شحيحاً. بالنسبة للخلايا الجذعية والبناءة للعظم (الأوستيوبلست)، يمكن للتفعيل المعتدل لـ HIF‑1α أن يعزز التكاثر والهجرة ونمو العظم، جزئياً عن طريق زيادة عوامل مثل VEGF التي تربط تكوين الأوعية الدموية بالعظم الجديد. لكن إذا كان نقص الأكسجين شديداً أو ممتداً، تتراكم جزيئات الإجهاد وأنواع الأكسجين التفاعلية، مما يدفع الأوستيوبلستات نحو الموت ويحفز خلايا هادمة للعظم (الأوستيوكلاست). لذلك يمكن للإشارة النقصوية نفسها أن تدعم أو تقوّض الالتئام، بحسب شدتها ومدة استمرارها.
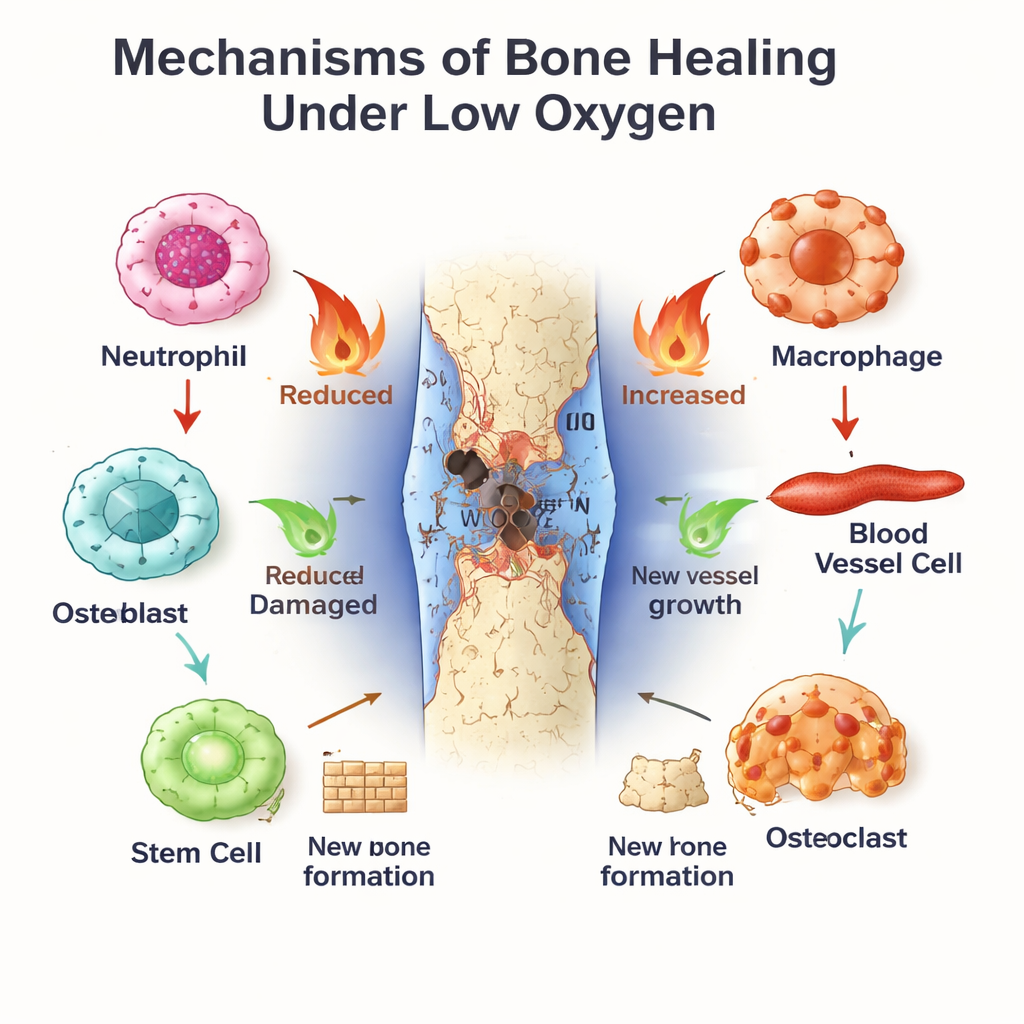
الساعة الداخلية للجسم كمدير لإصلاح العظم
يجري بالتوازي الإيقاع اليومي، ذلك المنظّم الجزيئي الزمني الموجود في كل خلية تقريباً. يساهم BMAL1، أحد مكوّناته المركزية، في ضبط الإيقاعات اليومية للنشاط المناعي وسلوك الأوعية الدموية وتمايز الخلايا الجذعية. تُظهر العدلات والبلعميات اختلافات حسب وقت اليوم في مدى استجابتها للإصابة وسرعة شيخوختها أو انتقالها من حالات التهابية (شبيهة M1) إلى حالات شافية (شبيهة M2). في خلايا الأوعية الدموية وخلايا نخاع العظم الجذعية، يعزز BMAL1 التكاثر الصحي وتشكيل العظم المنتظم، جزئياً عن طريق ضبط مسارات النمو مثل Wnt وTGF‑β/SMAD. عندما يتعطل BMAL1 — بسبب طفرات جينية أو العمل بنظام النوبات أو أمراض أيضية — تميل العظام إلى فقدان الكتلة، وتضعف قدرة الخلايا الجذعية، وينحرف التوازن بين التكوين وهدم العظم نحو الفقدان.
حوار بين استشعار الأكسجين والساعة البيولوجية
جوهر المراجعة هو «التواصل» الناشئ بين HIF‑1α وBMAL1. هذان البروتينان يشتركان في هياكل متشابهة ويمكن أن يتفاعلا جسدياً، وحتى يشكلا أزواجاً مختلطة ترتبط بالحمض النووي وتتحكم في مجموعات متداخلة من الجينات. يمكن لكل منهما أن يؤثر في إنتاج الآخر واستقراره، مما يخلق حلقات تغذية راجعة تربط توقيت الدورة اليومية بطريقة استجابة الخلايا لنقص الأكسجين. معاً يديران أيضاً توازن الأكسدة الخلوي — مقدار أنواع الأكسجين التفاعلية الضارة المنتجة مقابل القدرة المضادة للأكسدة المتاحة — ويتشاركان في تنظيم إنزيمات رئيسية تقرر ما إذا كانت الخلايا تعتمد أكثر على التنفس المعتمد على الأكسجين أو على الجليكوليز الخالي من الأكسجين. يساعد هذا التحكم المشترك في تحديد ما إذا كانت بيئة الكسر تفضّل إعادة بناء بناءة أو التهابية مفرطة وهدم العظم.
ماذا يعني هذا للأمراض والعلاج
تظهر شراكة HIF‑1α–BMAL1 نفسها في العديد من الحالات المرتبطة بالعظم. لدى العاملين بنظام النوبات، قد يغيّر اضطراب النوم والتعرّض للضوء BMAL1، ويزيد الإجهاد التأكسدي، ويعطل إصلاح HIF‑1α المُوجَّه، مما يسهم في هشاشة العظام. في مرضى السكري، يضعف ارتفاع سكر الدم وظيفة الساعة وإشارات نقص الأكسجين على حد سواء، ما يضعف نمو الأوعية الدموية وتكوين العظم المدفوع بالخلايا الجذعية. في التهاب المفاصل التنكسي، يؤدي فقدان BMAL1 في خلايا الغضروف إلى اضطراب إيقاعها وعلاقتها الوقائية مع HIF‑1α، مسرّعاً تكسّر الغضروف. حول غرسات التيتانيوم، يبدو أن نقص الأكسجين المُسيطر عليه وإيقاع يومي صحي يدعمان اندماجاً عظمياً أفضل، مما يوحي بأن طبقات مستقبلية للغرسات قد تُصمَّم لتنشيط HIF‑1α وBMAL1 بلطف. عموماً، تستنتج المقالة أن نجاح تجدد العظم لا يعتمد فقط على الخلايا الموجودة، بل على كيف تقرأ الأكسجين والوقت — وأن استهداف هذا الحوار قد يفتح طرقاً جديدة للشفاء الأسرع والأقوى.
الاستشهاد: Weng, Y., Xiong, J., Zhao, Q. et al. HIF-1α and BMAL1 in bone regeneration: crosstalk between hypoxia response and circadian rhythm. Bone Res 14, 25 (2026). https://doi.org/10.1038/s41413-026-00506-8
الكلمات المفتاحية: تجدد العظم, الإيقاع اليومي, نقص الأكسجين, هشاشة العظام, التئام الكسور