Clear Sky Science · ar
مواد بيوذكية ذكية لإصلاح وتجديد الهيكل العظمي مع التقدم في العمر
عظام أقوى في عالم يشيخ
يتوقع كثير من الناس أن ضعف العظام وآلام المفاصل أمور لا مفرّ منها مع التقدّم في العمر. لكن العلماء يصمّمون الآن مواد «ذكية» تستطيع استشعار متى وأين تتدهور العظام ثم تُساعدها على شفاء نفسها. تهدف هذه المواد إلى إصلاح الكسور بمصداقية أكبر، وإبطاء أو عكس هشاشة العظام والتهاب المفاصل التنكسي، وتقليل الحاجة إلى عمليات جراحية متكررة — مما يمنح كبار السن فرصة أفضل للبقاء نشطين ومستقلين.
كيف يشيخ العظم ولماذا يصبح أكثر عرضة للكسر
العظم نسيج حي يعيد بنائه باستمرار، لكن مع التقدّم في العمر يختل هذا التوازن. تتحوّل الخلايا الجذعية داخل نخاع العظم من إنتاج خلايا بناءة للعظم إلى إنتاج المزيد من خلايا الدهون؛ تتعب الخلايا البانية للعظم وتزداد نشاطاً خلايا هاضمة للعظم. تصبح الطبقة الداعمة من الكولاجين والمعدن أكثر جفافاً وهشاشة، وتترقّق «الهياكل المجهرية» الداعمة. تضيف تغيرات الهرمونات، والالتهاب المزمن منخفض الدرجة، وفرط الجذور المؤكسدة الضارة، وبيئة محلية حمضية مزيداً من الإجهاد. خارجياً يظهر ذلك على شكل عظام أنحف وأكثر مسامية، ومفاصل أقدر على التيبس، وعمود فقري مقوّس، ومخاطر أعلى للكسور وحالات مثل هشاشة العظام والتهاب المفاصل التنكسي.
لماذا العلاجات الحالية غير كافية
تشمل العلاجات الرئيسة اليوم أدوية تبطئ فقدان العظم أو تحفّز تكوينه، إلى جانب جراحات وزرعات معدنية أو خزفية لتثبيت الكسور أو استبدال المفاصل التالفة. أنقذت هذه الأساليب العديد من الأرواح لكنها تحمل سلبيات مهمة. غالباً ما تصل الأدوية الجهازية إلى جزء ضئيل جداً من نسيج العظم وقد تسبّب آثاراً جانبية مثل مشاكل في الفك، جلطات دموية، أو حتى زيادة خطر السرطان مع الاستخدام الطويل. تُظهر علاجات الخلايا الجذعية وعوداً في الحيوانات لكنها تواجه مشكلات بقاء الخلايا، وسلوكها غير المتوقّع، واحتمال تكوين أورام. توفر الزرعات التقليدية قوة لكنها كائنات «غبية»: لا تستشعر محيطها، ولا تستطيع ضبط إفراز الدواء، وقد تفشل في عظم هش وكبير السن.
حاملات أدوية ذكية تجوب الجسم
تدخل المواد البيلوجية الذكية لتُضفي عنصراً من الذكاء على هذا المجال. إحدى الاستراتيجيات الرئيسة هي «التوصيل الذكي» المنهجي للأدوية باستخدام جزيئات نانوية أو هلامات مرنة تدور في مجرى الدم وتتفعل فقط في بؤر المشكلة. يمكن بناء هذه الحاملات لتستجيب لإشارات داخلية مثل الحموضة، أو مستويات عالية من الجذور المؤكسدة الضارة، أو إنزيمات محللة للعظم؛ أو لمؤثرات خارجية مثل الضوء، الموجات فوق الصوتية، الحرارة، أو المجالات المغناطيسية. على سبيل المثال، تبقى بعض الجسيمات سليمة في الأنسجة الطبيعية لكنها تُفتح وتفرج عن حمولة الدواء في الجيوب الحمضية الغنية بالإنزيمات حيث تقوم خلايا هاضمة للعظم مفرطة النشاط بتآكل العظم. البعض الآخر يلتقط فائض الجذور المؤكسدة ويحرر تدريجياً دواءً مضاداً للالتهاب، أو يحمل صبغات تصويرية حتى يتمكن الأطباء من رؤية توزعه في الوقت الفعلي. عبر تراكيب محفزات متعددة — مثلاً كل من الرقم الهيدروجيني والمؤكسدات — يستطيع الباحثون تحسين الاستهداف وتقليل الآثار الجانبية.
هياكل محلية تتصرف كعظام ذكية مؤقتة
عندما تعاني العظام المسنة من عيوب كبيرة أو كسور معقّدة، يمكن زَرع «هياكل ذكية» محلية مباشرة في الفراغ. تُصنع هذه الهياكل ثلاثية الأبعاد من معادن أو مواد خزفية أو بوليمرات أو مجموعات منها، ومهندَسة لمطابقة قوة العظم، ومساميته، ومرونته. تسمح بنيتها الإسفنجية للأوعية الدموية والنسيج العظمي الجديد بالنمو داخلها، بينما يتحلل المادّة تدريجياً ويستبدلها نسيج المريض الخاص. 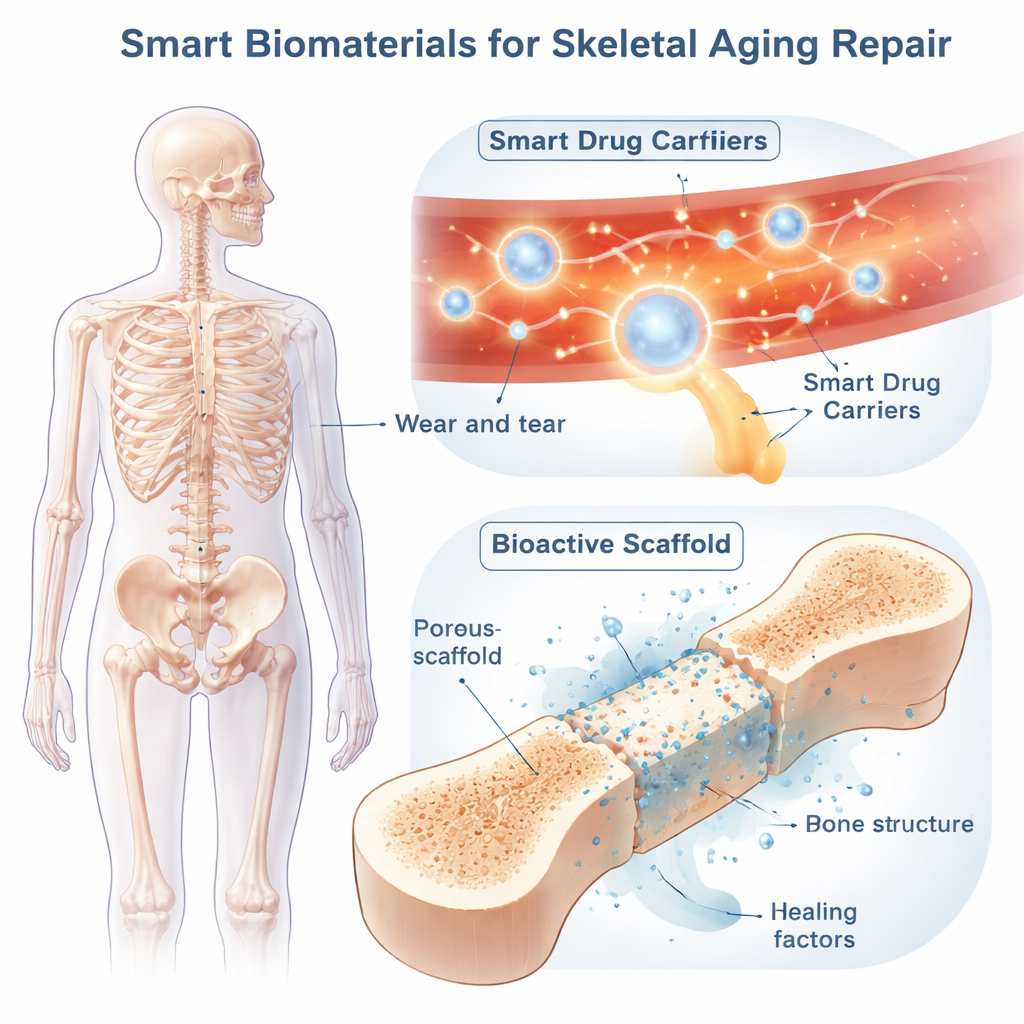
من المختبر إلى العيادة: الأدوات والعقبات والاتجاهات المستقبلية
لصنع هذه الأنظمة المعقّدة، يستخدم العلماء تقنيات تصنيع متقدمة مثل الطباعة ثلاثية الأبعاد والتصنيع الإضافي لضبط حجم المسام، والصلابة، وحمل الدواء بدقة عالية. ومع ذلك، فإن تحويل المواد البيلوجية الذكية إلى علاجات روتينية يمثل تحدياً. لا تزال معظم الجسيمات المحقونة تتراكم في أعضاء مثل الكبد والطحال بدلاً من العظم، وتفشل العديد من نماذج الحيوانات في محاكاة تعقيد الشيخوخة البشرية. الإنتاج واسع النطاق، وضبط الجودة، والموافقة التنظيمية، والتكلفة كلها عقبات رئيسية. يرى الباحثون أملاً في الجمع بين المواد الذكية والذكاء الاصطناعي لتخصيص تصميم الهياكل وجرعات الأدوية، وكذلك في إضافة حساسات مدمجة يمكنها تتبّع الشفاء وضبط العلاج تلقائياً في نمط «الحلقة المغلقة». 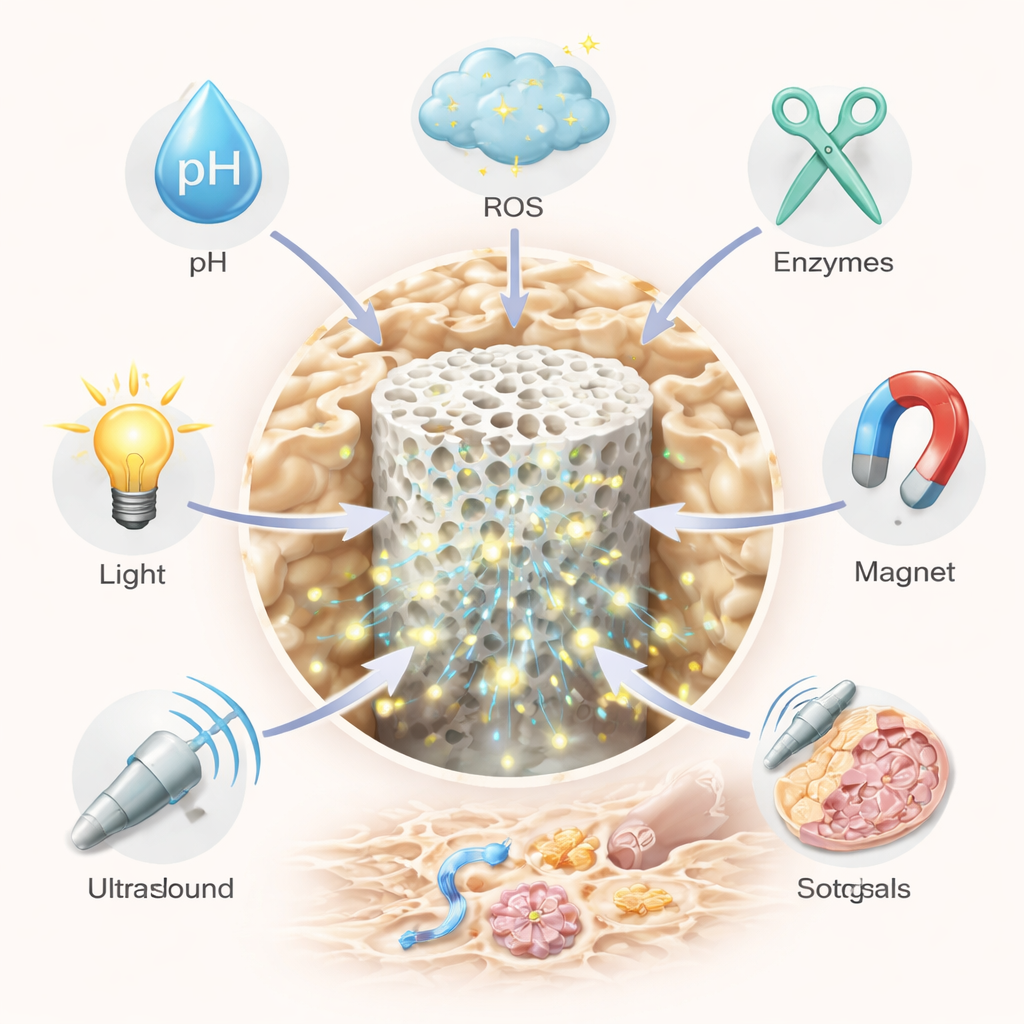
ماذا قد يعني هذا للمرضى
باختصار، تُظهر هذه الجهود أن هشاشة العظام في الشيخوخة ليست تدهوراً أحادي الاتجاه فحسب، بل مشكلة هندسية معقّدة قد تكون قابلة للحل. تعمل المواد البيلوجية الذكية كفرق إصلاح صغيرة قابلة للبرمجة: تجوب مجرى الدم، وتستقر في المواقع التالفة، وتفرج عما يلزم بالضبط، عندما يلزم، لاستعادة بنية العظم ووظيفته. رغم أن هذه التقنيات ما تزال إلى حد كبير في مرحلة البحث، فإنها تشير إلى مستقبل تلتئم فيه الكسور أسرع، وتدوم الزرعات لفترة أطول، وتُفصّل العلاجات بحسب بيولوجيا عظم كل شخص — مما يساعد مزيداً من الناس على البقاء قادرين على الحركة ومستقلين حتى سن متقدمة.
الاستشهاد: Liang, D., Wang, H., Jiang, Y. et al. Smart biomaterials for skeletal aging repair and regeneration. Bone Res 14, 24 (2026). https://doi.org/10.1038/s41413-026-00505-9
الكلمات المفتاحية: المواد البيلوجية الذكية, شيخوخة الهيكل العظمي, تجديد العظام, هشاشة العظام, هياكل قابلة للاستجابة للمؤثرات