Clear Sky Science · ar
تعبير APOE3-Christchurch في الخلايا النجمية يحسّن مَرَضية أميلويد-β في أدمغة فئران 5xFAD
لماذا يهم هذا النمط الجيني الدماغي
عادةً ما يُعرض مرض الزهايمر على أنه تراكم لا يمكن وقفه من كتل بروتينية ضارة في الدماغ. ومع ذلك، يبدو أن مجموعة صغيرة من الأشخاص تتحلّى بمقاومة غير عادية، محافظةً على مهاراتهم العقلية رغم حملهم عوامل جينية قوية للخطر. تركز هذه الدراسة على إحدى الطفرات الواقية في جين شائع يتعامل مع الكوليسترول، وتطرح سؤالًا عمليًا: إذا زوّدنا الدماغ بمزيد من هذا النسق الوقائي—تحديدًا من خلايا الدعم المسماة الخلايا النجمية—هل يمكن أن نجعل التغيرات الشبيهة بالزهايمر أقل ضررًا؟
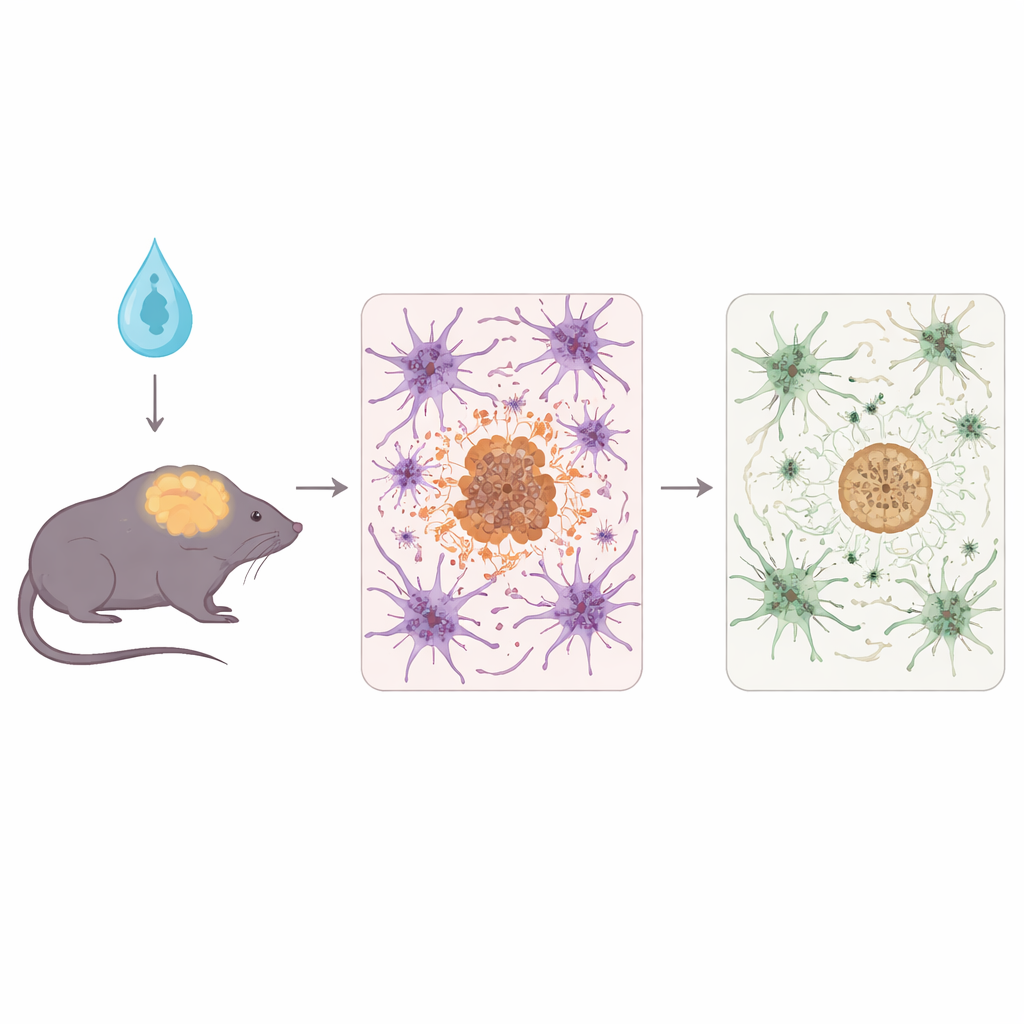
نسخة جينية وقائية تحت الأضواء
تركّز العمل على نسخة نادرة من جين APOE تُسمى APOE3-Christchurch. في حالة واقعية استثنائية، بقيت امرأة تحمل طفرة قوية تسبب الزهايمر مبكرًا محافظة على قدراتها الإدراكية لعقود أطول مما كان متوقعًا، وبدا أن هذه النسخة من APOE كانت سببًا رئيسيًا. أشارت دراسات سابقة في الحيوانات إلى أن APOE3-Christchurch يمكن أن يبطئ انتشار بروتين آخر مميِّز للزهايمر، تاو. لكن تأثيره على أميلويد-بيتا، البروتين الذي يشكل اللويحات التقليدية في أدمغة المصابين بالزهايمر، لم يكن واضحًا بالكامل بعد. سعى الباحثون لمعرفة كيف يتصرّف هذا النمط عندما يُعبر عنه خصيصًا بواسطة الخلايا النجمية، وهي الخلايا النجميّة الشكل التي تغذي وتحمِي العصبونات.
اختبار الطفرة في فأر يشبه الزهايمر
لاستكشاف ذلك، استخدم الفريق فئران 5xFAD، وهو نموذج معروف يتطور فيه تراكم أميلويد بسرعة وتظهر أضرار دماغية مرتبطة بذلك. بعد الولادة بوقت قصير، حصلت الفئران على ناقل فيروسي غير ضار دفع خلاياها النجمية لصناعة إما APOE3 البشري العادي، أو النسخة الوقائية APOE3-Christchurch، أو بروتين ضابط محايد. ثم فحص العلماء الحيوانات في مرحلة متقدمة من المرض، محللين أنسجة الدماغ بفحوصات بيوكيميائية، ومجهر فلوري، وتسلسل RNA لرصد كيف تغيّر أميلويد، والألياف العصبية المحيطة، والاستجابات المناعية.
جعل اللويحات أقل سمّية، وليس فقط أقلَّ عددًا
كلتا نسختي APOE المنتجة بواسطة الخلايا النجمية قلّلتا العبء العام للّويحات الأميلويدية وعلامات التلف المحيطة بتلك اللويحات مقارنةً بالمجموعات الضابطة. لكن APOE3-Christchurch أظهر تحسينات مهمة. فقد حوّل الأميلويد إلى لويحات أكثر تماسُكًا وكرويةً وشُعيرية الشكل وخفَّض مستويات أشكال معينة من أميلويد-بيتا القابلة للذوبان والمتجمِّعة—وهي أشكال يُعتقد أنها سامة بشكل خاص للمشابك العصبية. أظهرت النويات العصبية، وهي الزوائد الرقيقة للخلايا العصبية القريبة من اللويحات، تشوّهًا وإصابات أقل عندما كان APOE3-Christchurch حاضرًا. وبالتوازي، كانت خلايا المناعة الدماغية المسماة الميكروغليا والخلايا النجمية أقل نشاطًا التهابيًا عمومًا، وكشفت تحليلات النسخ الجيني عن تراجع في مسارات المناعة والضغط البروتيني، ما يوحي ببيئة أكثر هدوءًا وأقل عدائية للعصبونات.
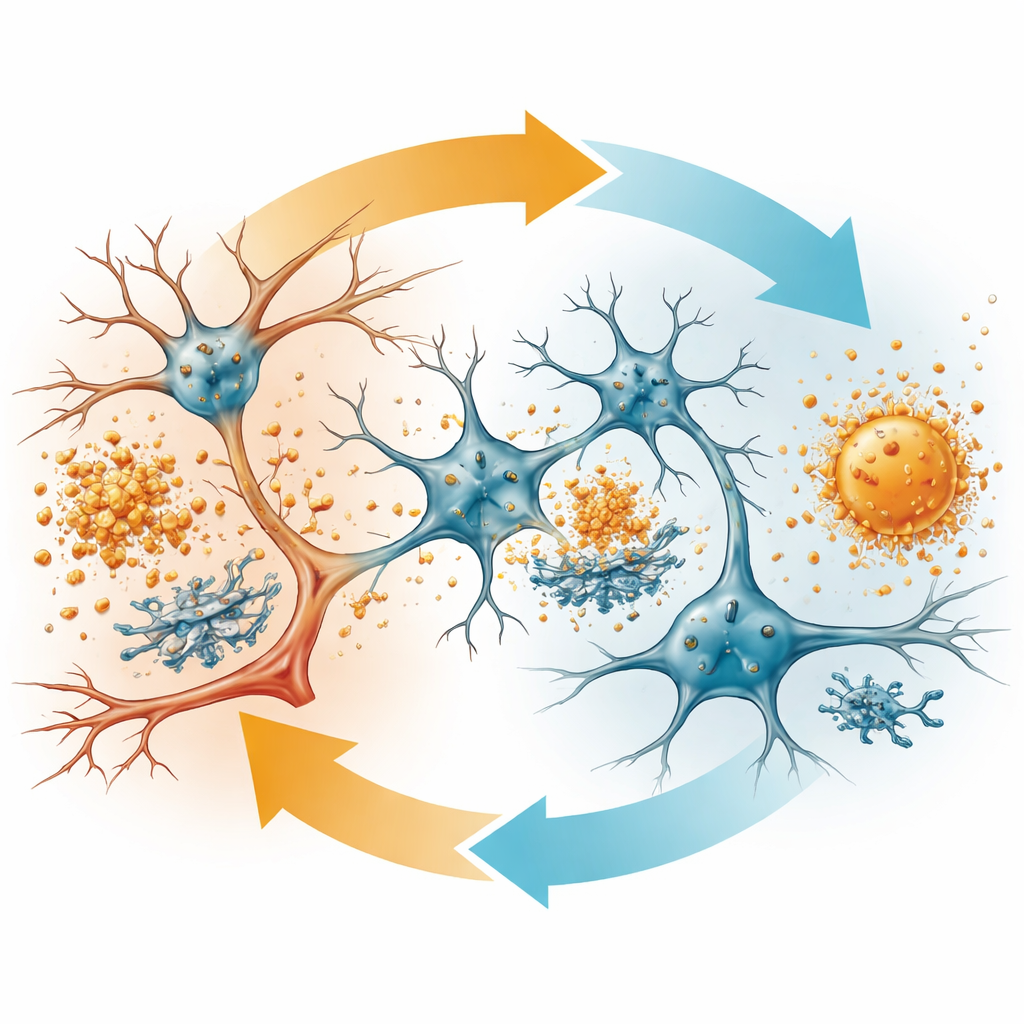
دلائل من أطباق الخلايا ونشاط الجينات
لتأكيد أن هذه التأثيرات لم تقتصر على الفئران، استخدم الفريق أيضًا خلايا نجمية بشرية مشتقة من الخلايا الجذعية ومهندَسة لتحمل إما APOE3 أو النسخة Christchurch. خلايا نجمية تحمل APOE3-Christchurch أفرزت كمية أكبر من بروتين APOE، وكانت الوسطية المشروطة لها تقلل تكوّن مجمّعات أميلويد-بيتا في نظام اختبار أنبوبي مضبوط. في أدمغة الفئران، غيّر تعبير APOE3-Christchurch شبكات من الجينات المعنية بطي البروتين، والضغط الخلوي، وإشارات المناعة، وقلل مستويات بروتينات مرتبطة باستجابات الضغط وتعطّل التعامل مع الدهون. مجتمعةً، تشير هذه الأدلة إلى أن APOE3-Christchurch لا يغيّر كمية الأميلويد فحسب—بل يغيّر شكله وطريقة استجابة خلايا الدماغ له.
ماذا قد يعني هذا للعلاجات المستقبلية
بينما كانت التأثيرات الوقائية التي لوحظت هنا متواضعة وليست معجزية، فهي غنية بالمعلومات. تُظهر الدراسة أن زيادة APOE3-Christchurch خصيصًا في الخلايا النجمية يمكن أن تجعل ترسبات الأميلويد أكثر تماسُكًا ويبدو أقل سمّية، وتقلل التلف العصبي القريب، وتخفّف الإشارات الالتهابية وإشارات الضغط، حتى دون القضاء على الأميلويد تمامًا. للخلاصة للقارئ العام: ليست كل اللويحات ضارة بنفس الدرجة—إعادة تشكيلها وتحييدها قد تكون مهمة بقدر إزالتها. تدعم هذه النتائج فكرة أن علاجات مستوحاة من APOE3-Christchurch—ربما تُقدَّم عبر العلاج الجيني أو أدوية تحاكي سلوكها—قد تساعد الدماغ على التعايش مع الأميلويد بسلام أكبر، وربما تبطئ أو تخفف مسار مرض الزهايمر.
الاستشهاد: Raulin, AC., Alnobani, A., Rodriguez-Martinez, P. et al. Astrocytic APOE3-Christchurch expression ameliorates brain amyloid-β pathology in 5xFAD mice. Transl Psychiatry 16, 224 (2026). https://doi.org/10.1038/s41398-026-04002-9
الكلمات المفتاحية: مرض الزهايمر, APOE3-Christchurch, أميلويد-بيتا, الخلايا النجمية, علاج جيني