Clear Sky Science · ar
الميكروRNA-132/212 يقللان مكافأة الأفيونات عبر استهداف ناقل الدوبامين في المنطقة الإجمالية البطنية
لماذا يهم هذا البحث في الحياة اليومية
مسكنات الألم الأفيونية والأدوية المشابهة قد توفر الراحة لكنها تحمل أيضاً خطر الإدمان الجدي. ينقّب هذا البحث في آليات نظام المكافأة في الدماغ ليحدد مفاتيح جينية بسيطة تُؤثر في مدى شعور الأفيونات بالمكافأة. من خلال فهم هذه المفاتيح، يأمل العلماء تصميم علاجات أذكى تخفف الألم أو تقلل الاعتماد دون أن تسيطر على دوائر المتعة في الدماغ.
جزيئات صغيرة ذات تأثير كبير
يعتمد دماغنا على مادة كيميائية تسمى الدوبامين لإشارة المتعة وتحفيزنا على السعي نحو تجارب مجزية، من الطعام اللذيذ إلى المخدرات المسببة للإدمان. تُتحكم قوة هذه الإشارة ومدتها جزئياً ببروتين يسمى ناقل الدوبامين، الذي يعمل مثل مكنسة كهربائية تمتص الدوبامين إلى داخل الخلايا العصبية. ركز الباحثون على قطعتين صغيرتين جداً من المادة الجينية، الميكروRNA-132 والميكروRNA-212، اللتين يمكن أن تخفضا إنتاج بروتينات محددة. ربطت دراسات سابقة هذه الميكروRNAs بالاستخدام الكوكايين والضغط النفسي. هنا، تساءل الفريق عما إذا كانت هذه الميكروRNAs تشكل أيضاً استجابة الدماغ للأفيونات، وبالتحديد للمورفين.
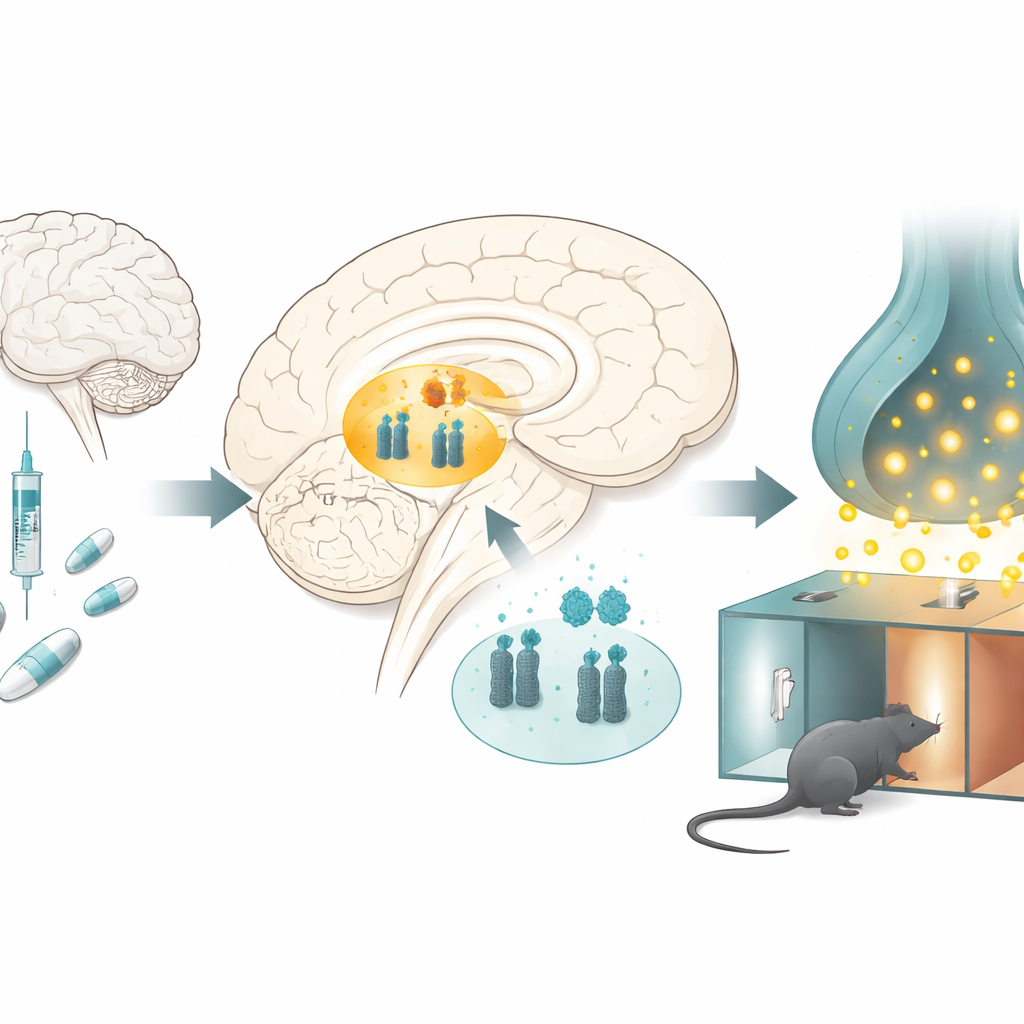
كيف تغير الأفيونات مركز المكافأة في الدماغ
درس الباحثون جرذاناً تتلقى جرعات متكررة من المورفين في اختبار كلاسيكي لمكافأة المخدر، حيث تتعلم الحيوانات تفضيل غرفة مرتبطة بالمخدر. بعد عدة أيام، قضت الجرذان المعالجة بالمورفين وقتاً أطول في الحجرة المقرونة بالمورفين، ما يظهر أن المخدر أصبح مكمِّلاً. عند فحص منطقة رئيسية للمكافأة عميقة في الدماغ تُسمى المنطقة الإجمالية البطنية، وجدوا نمطاً لافتاً: مستويات الميكروRNA-132 والميكروRNA-212 انخفضت، بينما ارتفعت مستويات ناقل الدوبامين. ظهرت تغييرات مماثلة عندما تلقى الجرذان المورفين دون مهمة تعلم المكان، مما يشير إلى أن التعرض المزمن للمخدر نفسه يزيح هذا التوازن الجزيئي.
تحديد رابط جزيئي مباشر
للبحث عما إذا كانت هذه الميكروRNAs تتحكم فعلاً في ناقل الدوبامين، توجه الفريق إلى خلايا بشرية شبيهة بالعصبونات في المختبر. بزيادة الميكروRNA-132 أو الميكروRNA-212 صناعياً، لاحظوا انخفاضاً في كل من الرسالة الجينية والبروتين الناقل. وإعاقة هذه الميكروRNAs أعطت التأثير المعاكس. ثم صمّموا بناء تقريرياً حيث ارتبط إنزيم منتج للضوء بذيل التنظيم الخاص بالناقلة. أضعفت إضافة الميكروRNAs إشارة الضوء، لكن هذا التأثير اختفى عندما طُورت بعض القواعد الأساسية في موقع الارتباط. معاً، أظهرت هذه التجارب أن الميكروRNA-132 والميكروRNA-212 تلتصقان مباشرة برسالة الناقلة وتثبطان إنتاجها.
من الجزيئات إلى مستويات الدوبامين والسلوك
بعد ذلك سأل الباحثون كيف يتجلى هذا التحكم الجزيئي في خلايا الدماغ الحية. في خلايا عصبية مزروعة، قلل رفع مستوى الميكروRNAs من امتصاص الدوبامين، بينما عزز تعطيلها تطهير الدوبامين. عندما زادوا أو خفضوا مستويات ناقل الدوبامين صناعياً، ارتفعت أو انخفضت تأثيرات الميكروRNAs تبعاً لذلك، مؤكدة أن الناقلة هي الوسيط الرئيسي. في جرذان حية، أدت زيادة الميكروRNA-132 في المنطقة الإجمالية البطنية إلى ارتفاع مستويات الدوبامين المتسربة إلى مناطق متصلة، مما يعكس نشاط ناقل أضعف. سلوكياً، جعلت أدوات فيروسية تمتص («إسفنجة») الميكروRNA-132 أو الميكروRNA-212 في هذه المنطقة الجرذان تتعلم تفضيلاً أقوى للمورفين، مصحوباً بارتفاع مستويات الناقلة. على النقيض، أدت فرض زيادة الميكروRNA-132 في نفس المنطقة إلى خفض مستويات الناقلة وتراجع تفضيل المورفين في ذكور وإناث وحيوانات مراهقة، دون أن تؤثر على الحركة أو الاستمتاع بالمكافآت الطبيعية مثل ماء محلى بالسكر.
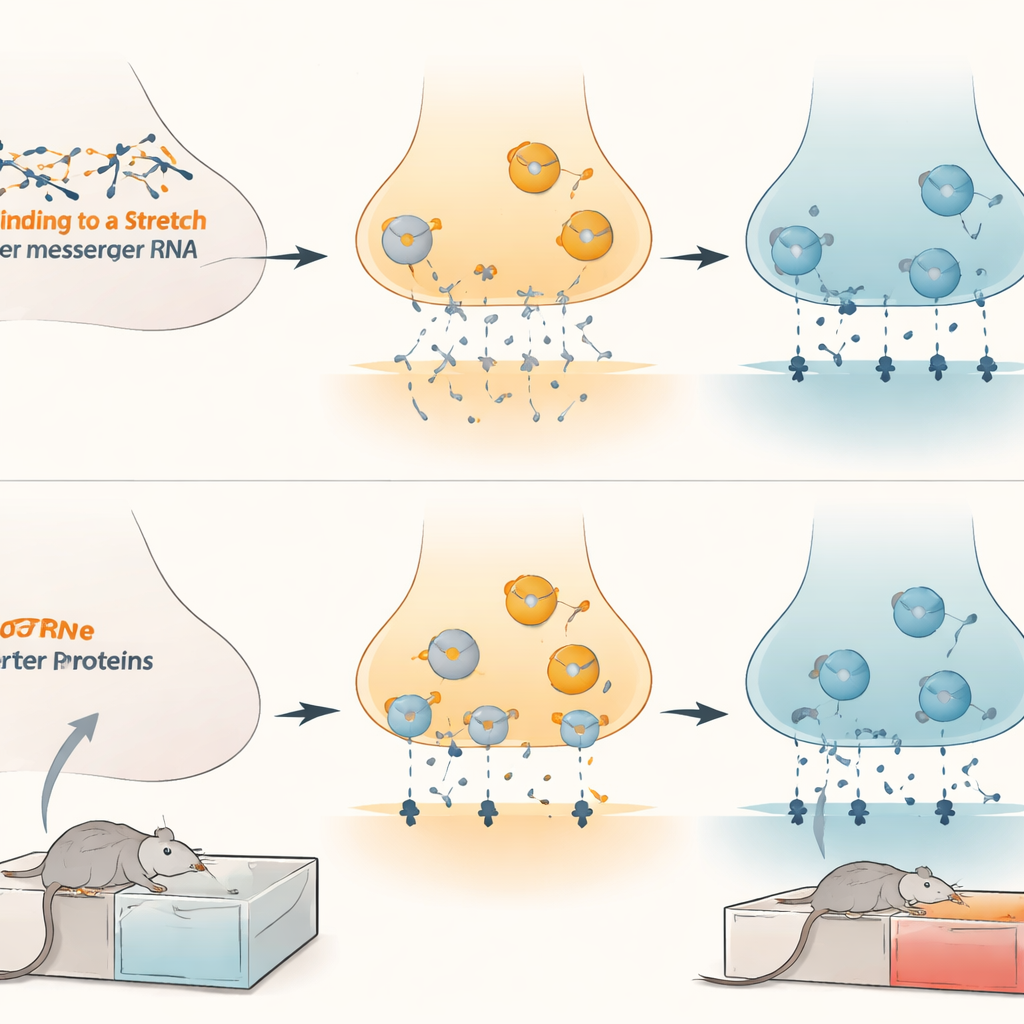
دلالات لعلاج إدمان الأفيونات
تكشف هذه النتائج عن نظام فرملة مضبوط بدقة داخل دوائر المكافأة في الدماغ: الميكروRNA-132 والميكروRNA-212 يحافظان على ضبط ناقل الدوبامين، مشكلين كيفية تجربة الأفيونات كمكافأة بقوة. يبدو أن المورفين المزمن يرفع هذا القفل عبر خفض الميكروRNAs، مما يسمح لمستويات الناقلة بالارتفاع ويساعد في ترسيخ إشارات المكافأة المرتبطة بالمخدر. عبر استعادة أو محاكاة عمل هذه الميكروRNAs بشكل محدد في المنطقة الإجمالية البطنية، قد يصبح ممكناً تليين قبضة مكافأة الأفيونات دون كبح المتعة أو الحركة بشكل واسع. وبينما يبقى الكثير من العمل قبل اختبار مثل هذه الاستراتيجيات في البشر، يشير هذا البحث إلى مسار جديد ومحدد للغاية للعلاجات المستقبلية التي تتعامل مع الإدمان على مستوى مقابض الدماغ الجزيئية نفسها.
الاستشهاد: Meng, J., Li, Z., Zhang, Y. et al. MicroRNA-132/212 negatively modulates opioid reward by targeting dopamine transporter in the ventral tegmental area. Transl Psychiatry 16, 152 (2026). https://doi.org/10.1038/s41398-026-03915-9
الكلمات المفتاحية: إدمان الأفيونات, ناقلة الدوبامين, الميكروRNA-132, المنطقة الإجمالية البطنية, مكافأة المورفين