Clear Sky Science · ar
تركيزات منخفضة من أوليغومرات أميلويد-بي تحث التكوّن المشابكي الذي يميّز ضعف الإدراك الخفيف وتغيّر البروتِومة المؤلفة حديثًا
تغيّرات مبكرة قد تشير إلى مشكلات في الذاكرة
قبل أن يسلب مرض الزهايمر الذاكرة من الأشخاص، يمر الدماغ بمنطقة وسطية غامضة تُعرف بضعف الإدراك الخفيف. في هذه المرحلة، تُصبح مشاكل التفكير ملحوظة لكن الحياة اليومية تستمر غالبًا. ومن الغريب أن بعض مناطق الدماغ في هذه المرحلة تُظهر المزيد، وليس القليل، من الاتصالات بين الخلايا العصبية. يسأل هذا البحث عما إذا كانت كميات صغيرة من جزيء سام مرتبط بالزهايمر قد تدفع هذا التفجّر في الاتصالات الجديدة، وما إذا كان دواء تم اختباره بالفعل على مرضى السرطان قد يخفف هذه التغيرات المبكرة جدًا.
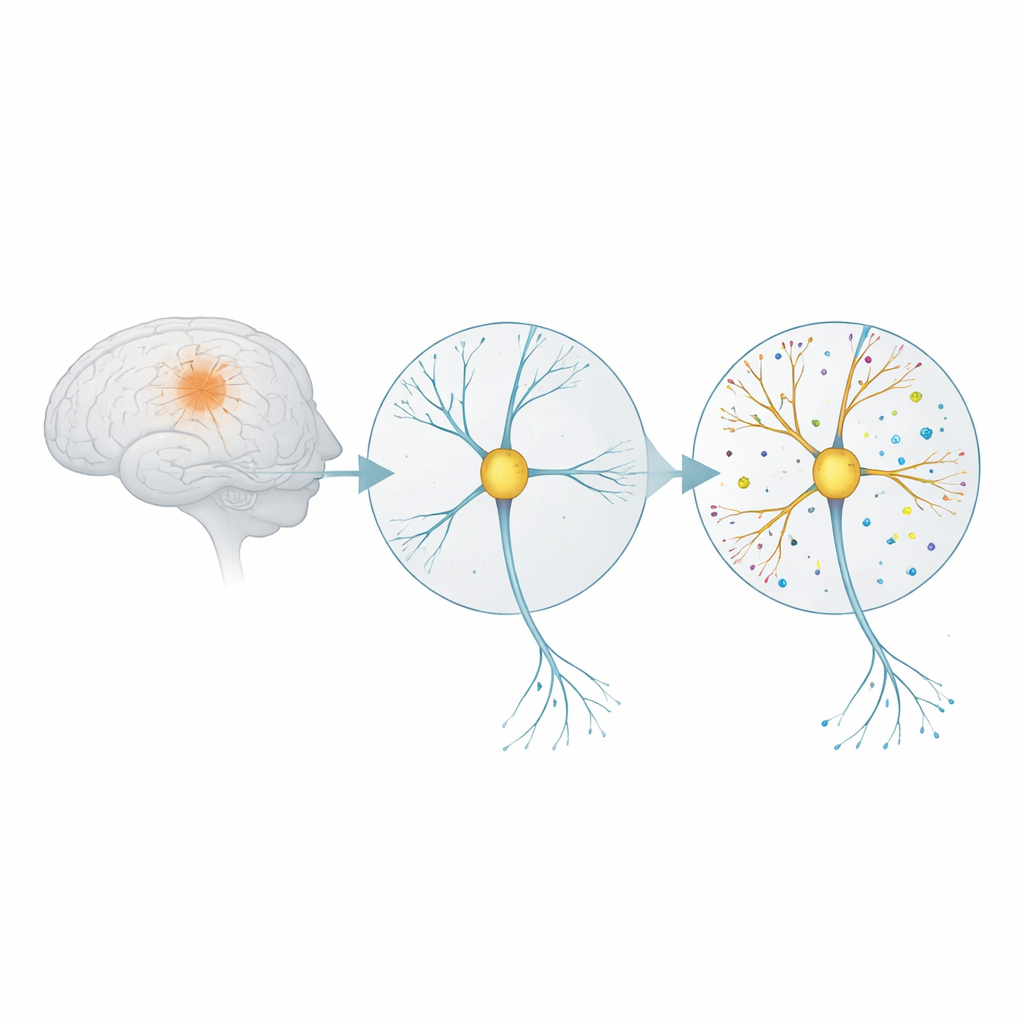
كيف تستجيب الاتصالات العصبية لمَحفّز سام
يرتبط مرض الزهايمر ارتباطًا وثيقًا بتكتلات صغيرة لقطعة بروتينية تسمى أميلويد-بي. في شكله الأوليغوميري، يكون هذا الجزء ضارًا بشكل خاص للمشابك—نقاط الاتصال التي تتواصل عبرها الخلايا العصبية. نما الباحثون خلايا دماغية من جرذان في طبق حتى كونت شبكات ناضجة، ثم عرّضوها لمدة خمسة أيام لجرعة منخفضة من أوليغومرات أميلويد-بي. كما اختبروا ما حدث عند إضافة مركب يُدعى eFT508، الذي يثبط إنزيم إشارة (MNK) مشارك في بدء تخليق البروتين داخل الخلايا. صُمِّم هذا الإعداد لمحاكاة مراحل المرض المبكرة جدًا، قبل حدوث موت خلوي واسع النطاق.
رؤية تفاصيل خفيّة للمشابك الجديدة
لفحص كيف تغيّرت الاتصالات، استخدم الفريق «المجهر التوسعي»، وهي تقنية تقوم بتوسيع الخلايا المحفوظة داخل جل لين بحيث يمكن رؤية الهياكل الدقيقة بتفصيل أدق بكثير. وضعوا علامات فلورية على الألياف العصبية وجانبي كل مشبك وأعادوا بنائها ثلاثي الأبعاد. سبّبت معالجة أميلويد-بي زيادة واضحة في عدد المشابك على امتدادات الخلايا العصبية. على وجه الخصوص، كان هناك المزيد من البُقع المفردة—اتصالات بسيطة واحد إلى واحد—و«الأشواك ذات التَّعصُّب المتعدد» النادرة، حيث يتقارب أكثر من ليف وارد إلى موقع استقبال واحد. تشبه هذه الأنماط الزيادات المشبكية المبلغ عنها لدى أشخاص يعانون من ضعف الإدراك الخفيف. عندما وُجد eFT508، انخفض عدد المشابك باتجاه المستويات الطبيعية، مما يوحي بأن الدواء قد يعاكس هذا الإفراط المبكر في النمو.
تغيّرات في البروتينات الجديدة، حتى وإن لم تتغير الكميات الإجمالية
تُعاد تشكيل المشابك باستمرار عبر صنع وتفكيك البروتينات. ثم نظر الفريق إلى أي البروتينات صُنعت حديثًا أثناء تعرّض الخلايا لأميلويد-بي وبعده. زودوا الخلايا العصبية بحمض أميني صناعي غير ضار يُدمَج في البروتينات الجديدة، ثم استخدموا تفاعلات كيميائية «نقر» والتحليل الطيفي الكتلي لاستخراج هذه الجزيئات وتحديدها. وبشكل مفاجئ، لم يتغير إجمالي مقدار البروتين الجديد المصنوع بعد عدة أيام من التعرض لجرعة منخفضة من أميلويد-بي، سواء بوجود eFT508 أو بدونه. لكن عند فحص أي البروتينات المحددة صُنعت، كانت الصورة مختلفة جدًا: تم اكتشاف أكثر من ألف بروتين جديد، وتبدلت عشرات منها صعودًا أو هبوطًا استجابةً لأميلويد-بي. كان الكثير منها مشاركًا في التواصل المشبكي، والهياكل الداخلية للخلايا، والميتوكندريا المنتجة للطاقة، وأنظمة تنظيف النفايات، وآليات مراقبة جودة البروتين.
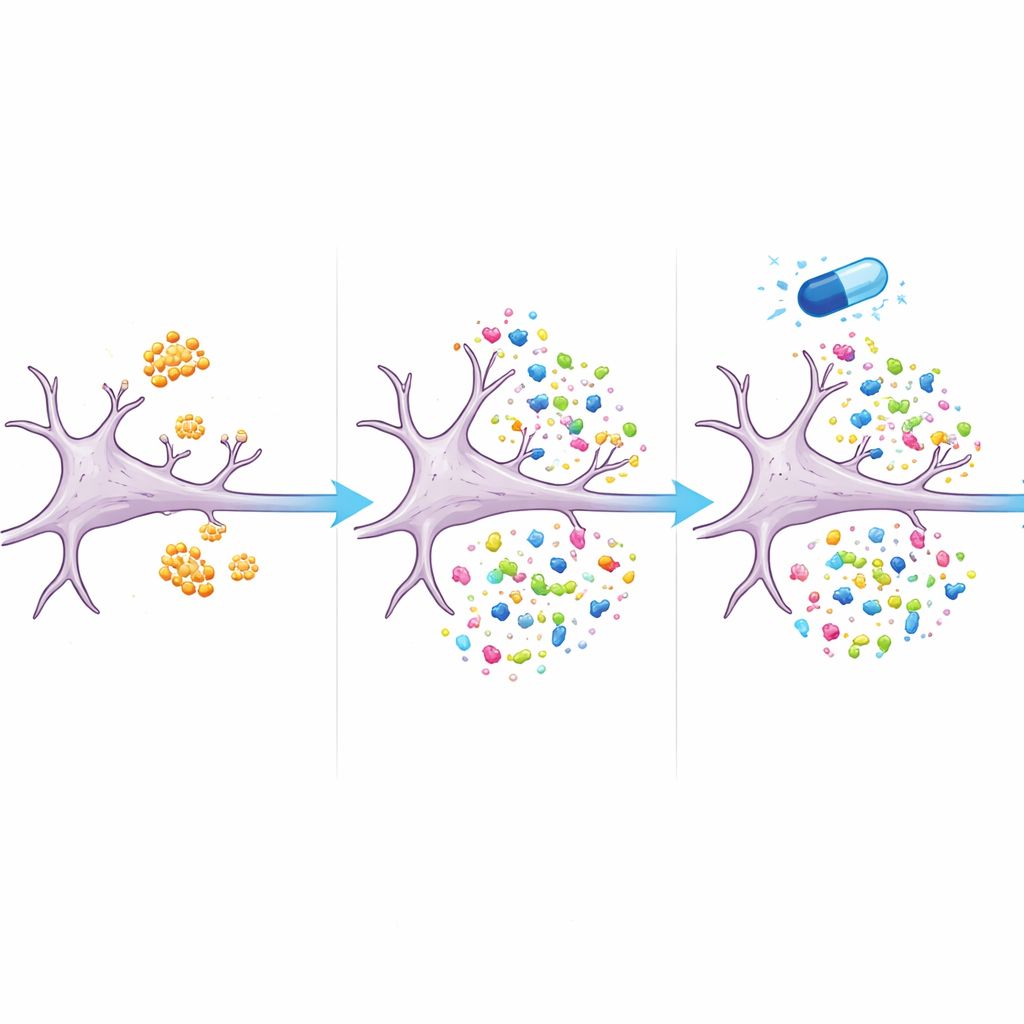
دواء يعيد توازن البروتينات
من المهم أن كثيرًا من البروتينات المضطربة عادت نحو المستويات الطبيعية عندما عولجت الخلايا بـ eFT508 مع أميلويد-بي. أكثر من ثلثي البروتينات التي غيّرها أميلويد-بي وحده لم تعد مختلفة بشكل معنوي عن الخلايا غير المعالجة حين وُجد الدواء. شملت هذه بروتينات مرتبطة ببنية ووظيفة المشابك، فضلاً عن مكونات أنظمة إعادة التدوير وإنتاج الطاقة داخل الخلايا. تشير النتائج إلى أن eFT508 لا يوقف تخليق البروتين ببساطة؛ بل يبدو أنه يعيد تشكيل أي البروتينات تُصنع، مائلًا النظام بعيدًا عن نمط شبيه بالزهايمر ونحو توازن أكثر صحة.
ما الذي قد يعنيه هذا لعلاج المستقبل
تقدّم هذه الدراسة صورة للضرر المبكر المرتبط بالزهايمر كمرحلة من الإفراط في التشابك وسوء إدارة بروتينية دقيق بدلًا من خسارة صريحة. تحفّز مستويات منخفضة من أميلويد-بي تكوّن مشابك إضافية، وأحيانًا غير اعتيادية، وتشوّه بشكل انتقائي مزيج البروتينات التي تصنعها الخلايا العصبية. في هذا النموذج القلائدي (الطبق)، يستطيع eFT508 كلًّا من تطبيع أعداد المشابك وتصحيح العديد من تغيّرات البروتين، مما يوحي بأن ضبط تخليق البروتين بعناية قد يبطئ أو يمنع الانتقال من ضعف الإدراك الخفيف إلى الخرف الكامل. وبينما يبقى الكثير ليُختبر في الحيوانات الحية والبشر، تبرز الدراسة طريقة جديدة للتفكير—وربما للتدخل—في المراحل الأولى من مرض الزهايمر.
الاستشهاد: Wu, K., Lee, S., Martinez-Serra, R. et al. Low concentrations of amyloid-beta oligomers induce synaptogenesis characteristic for mild cognitive impairment and alter the de novo proteome. Transl Psychiatry 16, 132 (2026). https://doi.org/10.1038/s41398-026-03905-x
الكلمات المفتاحية: مرض الزهايمر, تغيّرات المشابك, أوليغومرات أميلويد بيتا, تخليق البروتين, الانحلال العصبي المبكر